Clear Sky Science · fr
KIN17 facilite l'initiation et la progression des tumeurs rénales via la voie PI3K-AKT-mTOR
Pourquoi cette étude sur le cancer du rein est importante
Le cancer du rein est de plus en plus souvent dépisté, mais pour de nombreux patients la maladie reste difficile à contrôler une fois qu'elle s'est propagée. Cette étude scrute le problème à l'échelle moléculaire — jusqu'au niveau des molécules individuelles à l'intérieur des cellules cancéreuses — pour comprendre ce qui pousse les tumeurs rénales à croître et à envahir, et si un médicament expérimental peut freiner ce processus. Les résultats désignent une protéine peu connue, KIN17, comme un nouveau fauteur de troubles dans le cancer du rein et suggèrent une manière de la cibler indirectement par un traitement oral.
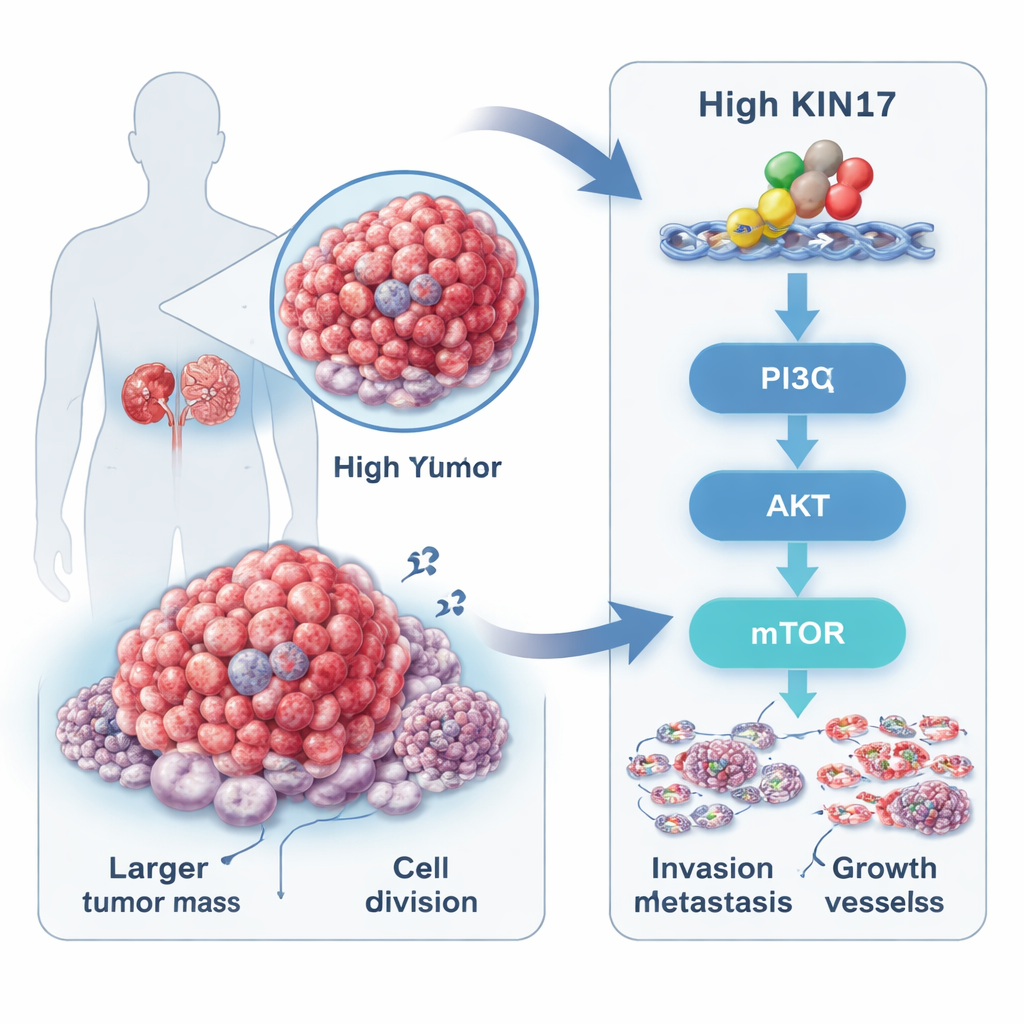
Un moteur caché au sein des tumeurs rénales
Le carcinome rénal, forme la plus fréquente de cancer du rein, débute souvent sans symptômes et est fréquemment découvert tardivement. Les chercheurs se sont concentrés sur une protéine appelée KIN17, connue depuis longtemps pour son rôle dans la protection et la réplication de l'ADN, mais récemment associée à plusieurs autres cancers. En analysant des bases de données publiques sur le cancer et des prélèvements tumoraux de 88 patients, ils ont constaté que les niveaux de KIN17 étaient beaucoup plus élevés dans les tumeurs rénales que dans les tissus non cancéreux adjacents. Les patients dont les tumeurs contenaient davantage de KIN17 avaient tendance à présenter des cancers plus volumineux, des lésions de grade plus élevé, un stade plus avancé et des métastases à distance, et leur survie était plus courte que chez ceux présentant de faibles niveaux de KIN17. Ce schéma suggère que KIN17 n'est pas un simple spectateur, mais est étroitement lié à l'agressivité tumorale.
Tester KIN17 dans des cellules cancéreuses
Pour déterminer ce que KIN17 fait réellement dans les cellules du cancer du rein, l'équipe a modifié des lignées cellulaires de laboratoire pour diminuer ou augmenter son expression. Lorsque KIN17 a été réduit, les cellules croissaient plus lentement, formaient moins de colonies et étaient moins aptes à migrer et à envahir à travers des membranes artificielles. Un plus grand nombre de ces cellules restaient bloquées en phase de repos du cycle cellulaire et mouraient davantage, montrant des taux accrus d'apoptose. L'inverse s'est produit lorsque KIN17 était surproduit : les cellules se multipliaient plus rapidement, répliquaient leur ADN plus facilement, refermaient plus vite des lacunes de type « scratch » dans les monocouches et envahissaient plus agressivement. Ces expériences montrent que KIN17 agit comme un accélérateur de la croissance et de la dispersion des cellules du cancer rénal.
Une voie de croissance prise sur le fait
Les chercheurs ont ensuite cherché à savoir comment KIN17 exerce cette influence. Leurs analyses d'activité génique et de protéines ont pointé vers un réseau de croissance et de survie bien connu à l'intérieur des cellules : la voie PI3K–AKT–mTOR. Cette voie est souvent comparée à un centre de contrôle central qui indique aux cellules quand croître, se diviser et éviter la mort. Les cellules de cancer du rein riches en KIN17 présentaient des signaux d'activation plus élevés — des marques chimiques appelées phosphates — sur des composants clés de cette voie, alors que la quantité totale de ces protéines ne changeait pas. Lorsque KIN17 était supprimé, ces marques d'activation diminuèrent, et les molécules associées à la mobilité et à l'invasion cellulaire évoluèrent aussi. Dans des expériences chez la souris, les tumeurs issues de cellules riches en KIN17 croissaient plus volumineuses et plus rapidement, et des colorations tissulaires montrèrent que la même voie de croissance était fortement activée dans ces tumeurs.
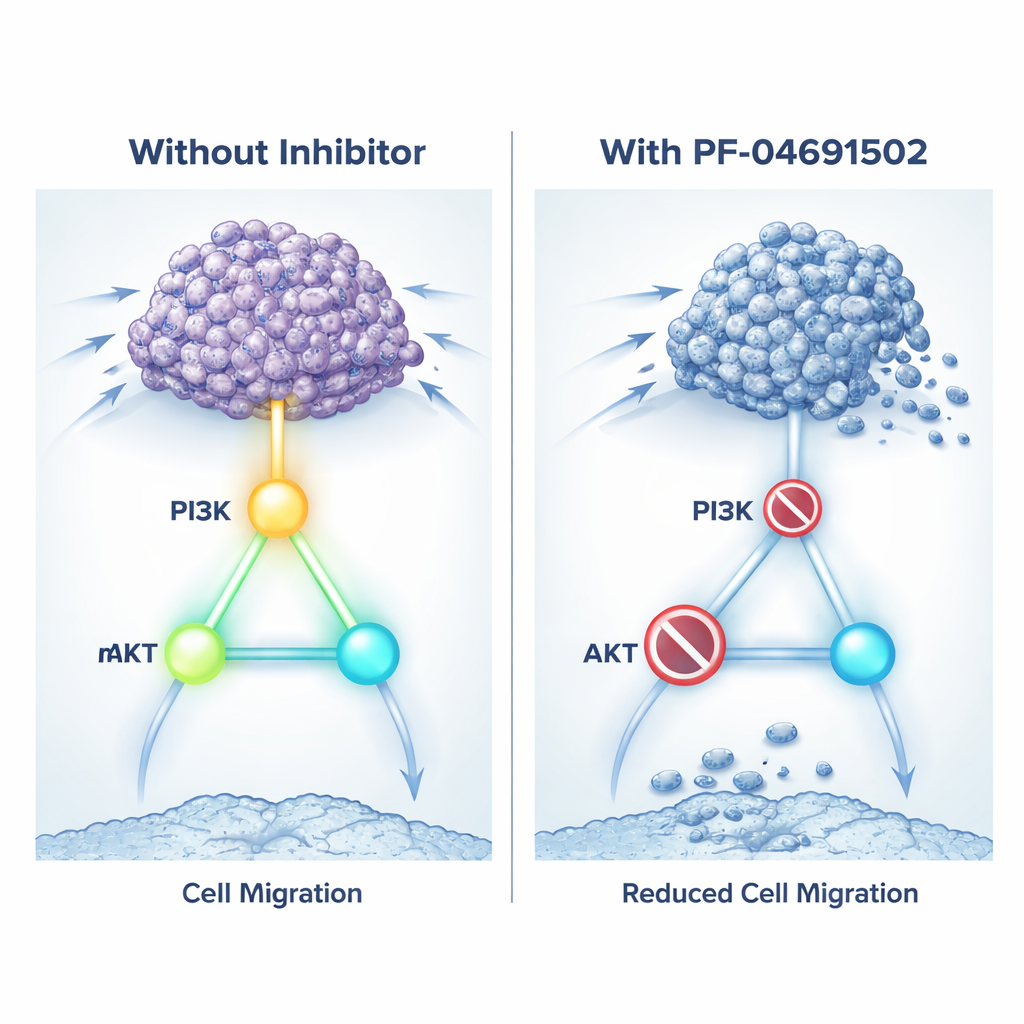
Atténuer le signal avec un médicament à double cible
Parce qu'il n'est pas encore possible de bloquer directement KIN17 avec les médicaments disponibles, l'équipe a testé une autre tactique : couper la voie de croissance qu'il semble contrôler. Ils ont utilisé PF‑04691502, un médicament expérimental qui inhibe à la fois PI3K et mTOR, deux interrupteurs clés de la voie. En culture, le traitement des cellules de cancer rénal à forte expression de KIN17 avec cet inhibiteur ralentissait leur croissance, réduisait leur capacité à migrer et à former des colonies, et augmentait les taux de mort cellulaire. Le médicament a aussi diminué les marques d'activation sur PI3K, AKT et mTOR et abaissé les niveaux de protéines liées à l'invasion. Chez des souris porteuses de tumeurs rénales, des doses quotidiennes de PF‑04691502 réduisirent les tumeurs surproduisant KIN17 et diminuèrent les marqueurs de division cellulaire tout en augmentant les signaux de mort cellulaire. En substance, le médicament a pu atténuer les effets nocifs de KIN17 en silencant sa voie de croissance privilégiée.
Ce que cela pourrait signifier pour les patients
Pour les personnes confrontées au cancer du rein, ces résultats suggèrent deux idées porteuses d'espoir. Premièrement, mesurer KIN17 dans les échantillons tumoraux pourrait aider les médecins à estimer l'agressivité d'une tumeur et son risque de dissémination. Deuxièmement, les tumeurs qui dépendent fortement de KIN17 pourraient être particulièrement vulnérables aux médicaments ciblant la voie PI3K–AKT–mTOR, tels que PF‑04691502 ou des inhibiteurs similaires à double cible déjà en essais cliniques pour d'autres cancers. Bien que de nombreux travaux restent nécessaires avant qu'un nouveau traitement n'arrive en clinique, cette étude trace une chaîne d'événements claire — de KIN17, via une voie de croissance clé, à l'expansion tumorale incontrôlée — et montre que rompre cette chaîne peut ralentir le cancer du rein en laboratoire et chez l'animal.
Citation: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
Mots-clés: carcinome rénal, KIN17, PI3K AKT mTOR, thérapie ciblée, PF-04691502