Clear Sky Science · fr
Détection de la drépanocytose en conditions de ressources limitées via transfer-learning et contrastive-learning couplés à l’XAI
Pourquoi des tests sanguins plus intelligents comptent
La drépanocytose est une maladie sanguine chronique pouvant provoquer d’intenses douleurs, des infections et une mortalité précoce, notamment dans certaines régions d’Afrique et d’Inde où les ressources médicales sont rares. Un diagnostic précoce peut sauver des vies, mais les tests traditionnels demandent du personnel qualifié, des appareils spécialisés et du temps que beaucoup de cliniques n’ont pas. Cet article explore comment l’intelligence artificielle (IA) peut transformer de simples images microscopiques de sang en outils de dépistage rapides et fiables, facilitant la détection de la drépanocytose même en milieu à ressources limitées.
Un examen approfondi d’un trouble sanguin dangereux
Dans la drépanocytose, une petite modification du gène de l’hémoglobine — la protéine qui transporte l’oxygène — fait que les globules rouges se plient en formes rigides en croissant ou « en faucille » au lieu de rester souples et ronds. Ces cellules déformées peuvent obstruer les petits vaisseaux sanguins, interrompant le flux sanguin et endommageant les organes. 
Des laboratoires surchargés aux assistants IA
Les méthodes classiques de confirmation de la drépanocytose — comme l’électrophorèse de l’hémoglobine ou les tests génétiques — sont précises mais souvent coûteuses, gourmandes en équipement et lentes. En revanche, de nombreuses cliniques disposent déjà de microscopes basiques, et des caméras modernes peuvent capturer des images haute résolution des frottis sanguins. Les auteurs s’appuient sur cette réalité : au lieu de modifier la collecte du sang, ils changent la manière dont les images sont analysées. Ils alimentent des images numérisées de frottis sanguins dans des modèles d’IA qui ont déjà appris à reconnaître des motifs à partir de millions de photographies courantes, puis adaptent ces modèles pour distinguer les globules rouges normaux des cellules falciformes. Cette réutilisation de connaissances préalables, appelée transfer learning, est cruciale lorsque seules quelques centaines d’images médicales sont disponibles pour l’entraînement.
Apprendre aux machines à discerner des formes subtiles
Toutes les méthodes d’entraînement de l’IA ne se valent pas, surtout quand les données sont limitées. Les chercheurs comparent trois réseaux de reconnaissance d’images populaires — ResNet-50, DenseNet-121 et EfficientNet-B0 — et trois façons de les entraîner. Deux méthodes traitent le problème comme une simple question oui/non (falciforme ou non) et cherchent à améliorer la précision brute de classification. La troisième, appelée triplet loss, apprend plutôt au réseau à organiser les images dans un « espace des formes » où les images de cellules falciformes se regroupent et s’éloignent des images de cellules normales. Cet apprentissage centré sur le contraste transforme le modèle en spécialiste pour repérer de petites différences basées sur la forme, précisément ce qui importe en microscopie de la drépanocytose.
Rendre le processus de décision visible
Les médecins et le personnel de laboratoire doivent pouvoir faire confiance à tout système automatisé influençant les soins aux patients. Pour ouvrir la « boîte noire » de l’IA, les auteurs utilisent une méthode d’IA explicable appelée Grad-CAM, qui superpose une carte de chaleur sur l’image microscopique originale pour montrer quelles régions ont le plus influencé la décision. 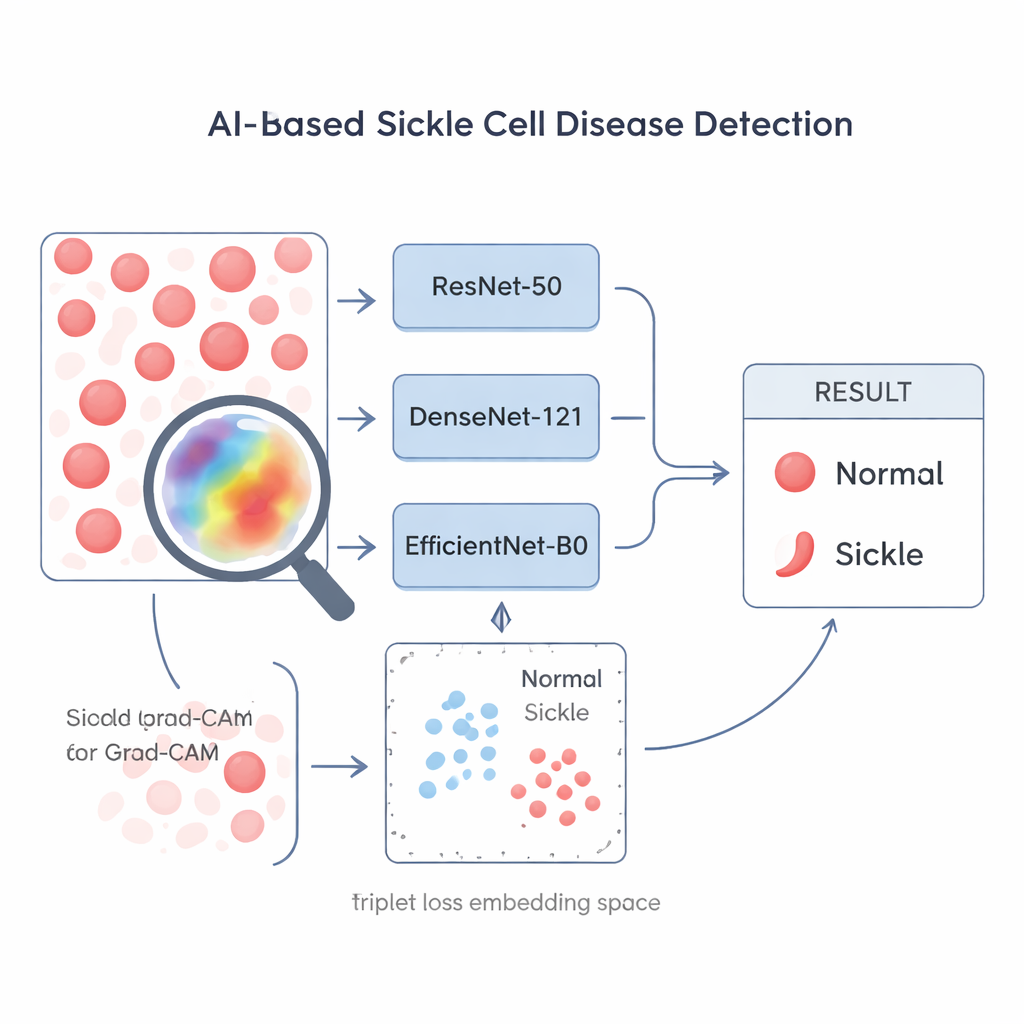
De la recherche aux cliniques sur le terrain
L’étude conclut que la réutilisation intelligente de réseaux de reconnaissance d’images existants, combinée à l’entraînement par triplet loss et à des explications visuelles, peut fournir une détection précise et transparente de la drépanocytose à partir d’un nombre relativement réduit d’images. En termes simples, un microscope standard associé à une caméra et un ordinateur portable pourrait aider les cliniques de première ligne à repérer rapidement les patients susceptibles d’avoir la drépanocytose, même sans tests de laboratoire sophistiqués. Bien que des jeux de données plus larges et plus diversifiés soient encore nécessaires avant un déploiement à grande échelle, ce travail trace une voie claire vers un dépistage assisté par IA à faible coût qui pourrait faire une réelle différence dans les régions où la drépanocytose est fréquente mais où les ressources diagnostiques sont limitées.
Citation: Patel, J., Muralikrishna, H., Chadaga, K. et al. Sickle cell disease detection in low-resource conditions using transfer-learning and contrastive-learning coupled with XAI. Sci Rep 16, 6104 (2026). https://doi.org/10.1038/s41598-026-35831-9
Mots-clés: drépanocytose, imagerie médicale, apprentissage profond, diagnostic en ressources limitées, IA explicable