Clear Sky Science · fr
Cadre intégratif en cellule unique et apprentissage automatique révélant des sous-types de fibroblastes pronostiques et construisant une signature de risque liée aux fibroblastes dans l’adénocarcinome pulmonaire
Pourquoi les cellules « assistantes » autour des tumeurs pulmonaires comptent
L’adénocarcinome pulmonaire est l’une des formes les plus fréquentes et mortelles de cancer du poumon, pourtant des patients présentant des tumeurs apparemment similaires peuvent avoir des issues et des réponses aux traitements très différentes. Cette étude se penche au‑delà des cellules cancéreuses elles‑mêmes pour se concentrer sur les cellules « assistantes » environnantes appelées fibroblastes, qui participent à la construction et au remodelage des tissus. En observant ces cellules une par une puis en utilisant des modèles informatiques avancés, les chercheurs montrent que les fibroblastes existent en différentes variantes capables de prévoir le pronostic des patients et la réponse possible de leurs tumeurs aux immunothérapies modernes.
Observer de près le voisinage tumoral
À l’aide du séquençage ARN monocellulaire de pointe, l’équipe a analysé plus de 140 000 cellules individuelles provenant d’échantillons d’adénocarcinome pulmonaire non traités. Cette technique révèle quels gènes sont actifs dans chaque cellule, permettant aux auteurs de classer la tumeur en principaux résidents : cellules immunitaires, cellules cancéreuses, cellules vasculaires et fibroblastes. Ils ont constaté que les tumeurs varient grandement dans la proportion de chaque type cellulaire. Certaines tumeurs sont riches en cellules immunitaires, tandis que d’autres sont dominées par les fibroblastes et le tissu structurel. Des analyses complémentaires ont montré que chacun de ces types cellulaires remplit des rôles spécialisés, depuis l’orchestration d’attaques immunitaires jusqu’à la construction de l’armature structurelle de la tumeur.
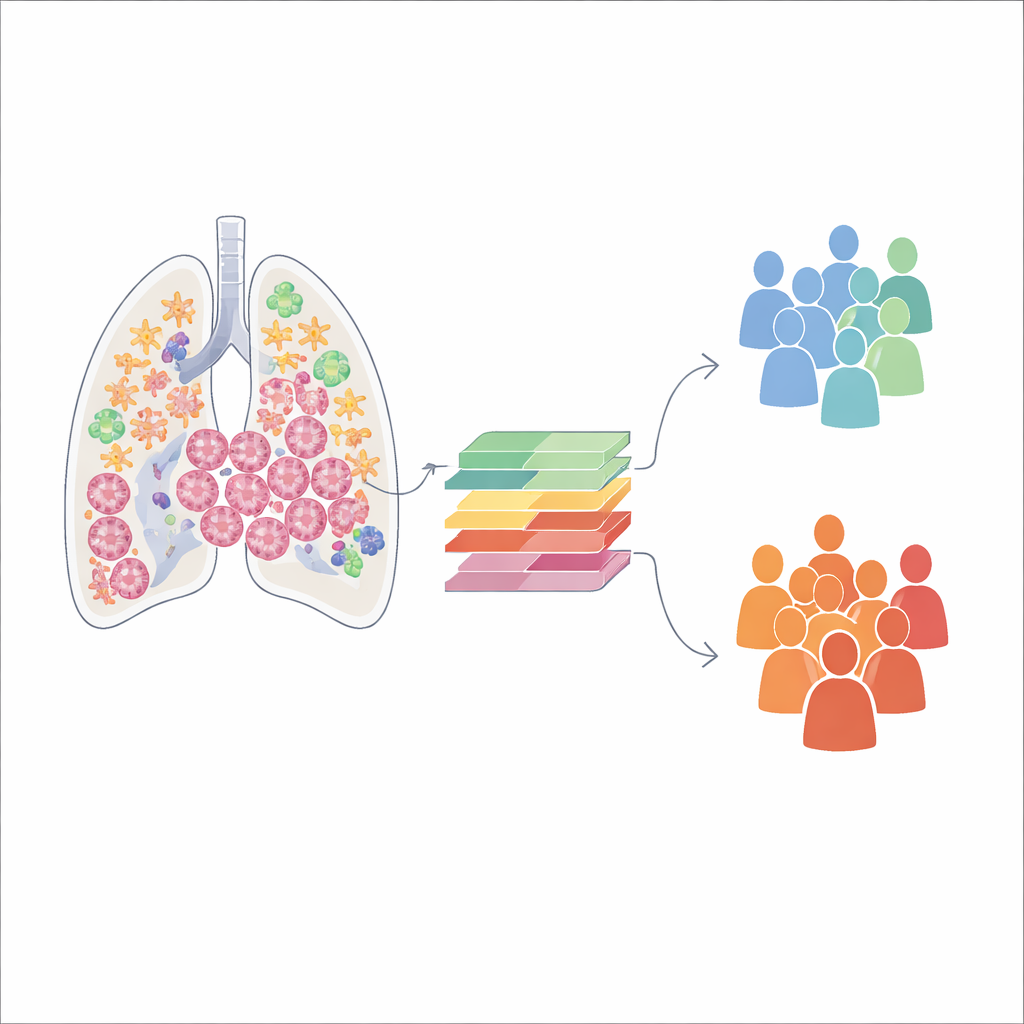
Les fibroblastes ne sont pas tous identiques
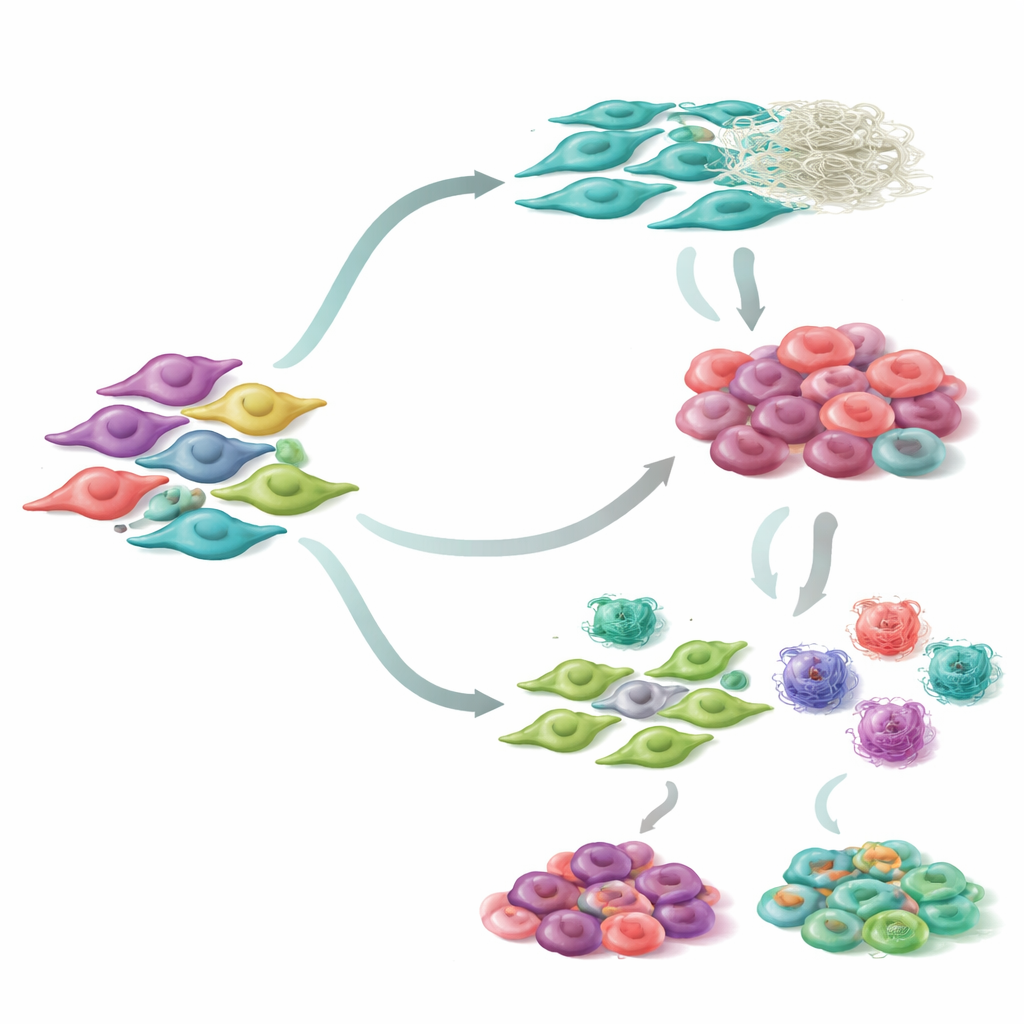
En se concentrant spécifiquement sur les fibroblastes, les chercheurs ont identifié sept sous‑groupes distincts de fibroblastes au sein des tumeurs pulmonaires. En reconstruisant les trajectoires temporelles de ces cellules, ils ont observé deux voies de différenciation principales. Sur une voie, les fibroblastes acquièrent progressivement des caractéristiques de cellules contractiles et rigidifiantes du tissu qui remodèlent l’environnement tumoral. Sur l’autre, les fibroblastes deviennent davantage impliqués dans les interactions avec le système immunitaire, soit en attirant soit en réprimant les cellules immunitaires. Chaque sous‑groupe présentait des profils d’activité génique propres et était associé à des fonctions biologiques différentes telles que la contraction de type musculaire, la migration ou la régulation immunitaire. De manière importante, les patients dont les tumeurs étaient enrichies en certains sous‑types de fibroblastes avaient tendance à vivre plus longtemps, ce qui montre que la répartition des états des fibroblastes n’est pas une simple curiosité mais se relie à des issues cliniques réelles.
Construire un score de risque à partir des signaux des fibroblastes
Pour transformer ces connaissances biologiques en un outil clinique utile, l’équipe a combiné les gènes marqueurs des fibroblastes issus des données monocellulaires avec des données en masse provenant de centaines de patients dans de larges bases publiques. Ils ont ensuite appliqué une batterie de 10 méthodes d’apprentissage automatique, testant 101 combinaisons de modèles, afin de découvrir quel ensemble de gènes liés aux fibroblastes prédit le mieux la survie des patients. Le modèle gagnant, appelé signature liée aux fibroblastes, ou FRS, utilise 29 gènes pour attribuer à chaque patient un score de risque. Dans le jeu de données principal et six cohortes indépendantes, les personnes avec un score FRS élevé présentaient systématiquement une survie plus mauvaise que celles avec un score bas. La FRS est aussi restée un prédicteur robuste même après ajustement pour l’âge, le sexe et le stade tumoral, et elle a amélioré la prédiction lorsqu’elle était combinée au système de stadification TNM standard.
Indices d’échappement immunitaire et de réponse au traitement
Comme de nombreux patients reçoivent désormais des immunothérapies, les auteurs se sont demandés si le score basé sur les fibroblastes reflète des caractéristiques du microenvironnement immunitaire tumoral. Ils ont constaté que les tumeurs avec des scores FRS faibles présentaient une infiltration plus importante par des cellules immunitaires anti‑cancer telles que les cellules T CD8 et les cellules NK, ainsi qu’une expression plus élevée de gènes impliqués dans la présentation d’antigènes tumoraux au système immunitaire. À l’inverse, les tumeurs à FRS élevé montraient moins de cellules immunitaires utiles, une plus grande proportion de cellules tumorales, une instabilité génétique accrue et des signes d’exclusion immunitaire, c’est‑à‑dire que les cellules immunitaires sont tenues à distance. Des mesures simulant la probabilité de réponse aux inhibiteurs de points de contrôle immunitaire suggèrent que les patients avec des FRS faibles pourraient bénéficier davantage de ces traitements, tandis que les patients à FRS élevé pourraient être plus résistants.
Mettre en lumière un gène cible prometteur
Parmi les gènes constituant la FRS, l’équipe a mis en avant un gène nommé TIMP1 comme marqueur particulièrement fort de mauvais pronostic. TIMP1 était présent à des niveaux élevés dans de nombreux types de cancers et particulièrement augmenté dans les tissus d’adénocarcinome pulmonaire comparés au poumon normal adjacent. Dans des expériences en laboratoire, la réduction des niveaux de TIMP1 dans des lignées cellulaires de cancer du poumon a diminué la capacité des cellules à envahir une matrice et à former de nouvelles colonies, suggérant que TIMP1 favorise la croissance tumorale et la dissémination. Ces résultats désignent TIMP1 comme une cible potentielle pour des médicaments futurs visant à affaiblir la machinerie structurale et immunomodulatrice de la tumeur.
Ce que cela signifie pour les patients
Ce travail montre que la chorale de cellules de soutien autour d’une tumeur pulmonaire, en particulier les fibroblastes, contient des informations précieuses sur le comportement de la maladie et sur sa réponse possible aux traitements. En combinant des mesures monocellulaires et l’apprentissage automatique, les auteurs ont créé un score de risque basé sur les fibroblastes capable de classer les patients en groupes à risque plus élevé ou plus faible et d’indiquer quelles tumeurs sont plus susceptibles de résister à l’immunothérapie. Bien que des validations supplémentaires soient nécessaires avant qu’un tel score puisse guider la pratique clinique quotidienne, l’étude souligne que traiter efficacement le cancer du poumon requerra non seulement d’attaquer les cellules tumorales elles‑mêmes mais aussi de maîtriser les fibroblastes environnants qui aident la tumeur à croître et à se dissimuler.
Citation: Cheng, S., Zhang, H., Mu, Q. et al. Integrative single-cell and machine learning framework reveals prognostic fibroblast subtypes and constructs a fibroblast-related risk signature in lung adenocarcinoma. Sci Rep 16, 7965 (2026). https://doi.org/10.1038/s41598-026-35830-w
Mots-clés: adénocarcinome pulmonaire, fibroblastes associés au cancer, séquençage monocellulaire, microenvironnement tumoral, réponse à l’immunothérapie