Clear Sky Science · fr
Points communs dans les changements d'expression génique et de méthylation de l'ADN dans deux modèles de rat d'épilepsie acquise
Pourquoi les changements génétiques importent pour les crises
L’épilepsie touche des millions de personnes et, pour environ une personne sur trois, les médicaments actuels ne contrôlent pas complètement les crises. La plupart des traitements atténuent simplement les tempêtes électriques dans le cerveau sans empêcher l’apparition de l’épilepsie. Cette étude examine si des marques chimiques durables sur l’ADN et la façon dont les gènes sont activés ou désactivés peuvent expliquer comment un cerveau sain devient épileptique — et si ces modifications sont communes à différentes formes de la maladie.
Deux voies différentes vers la même maladie
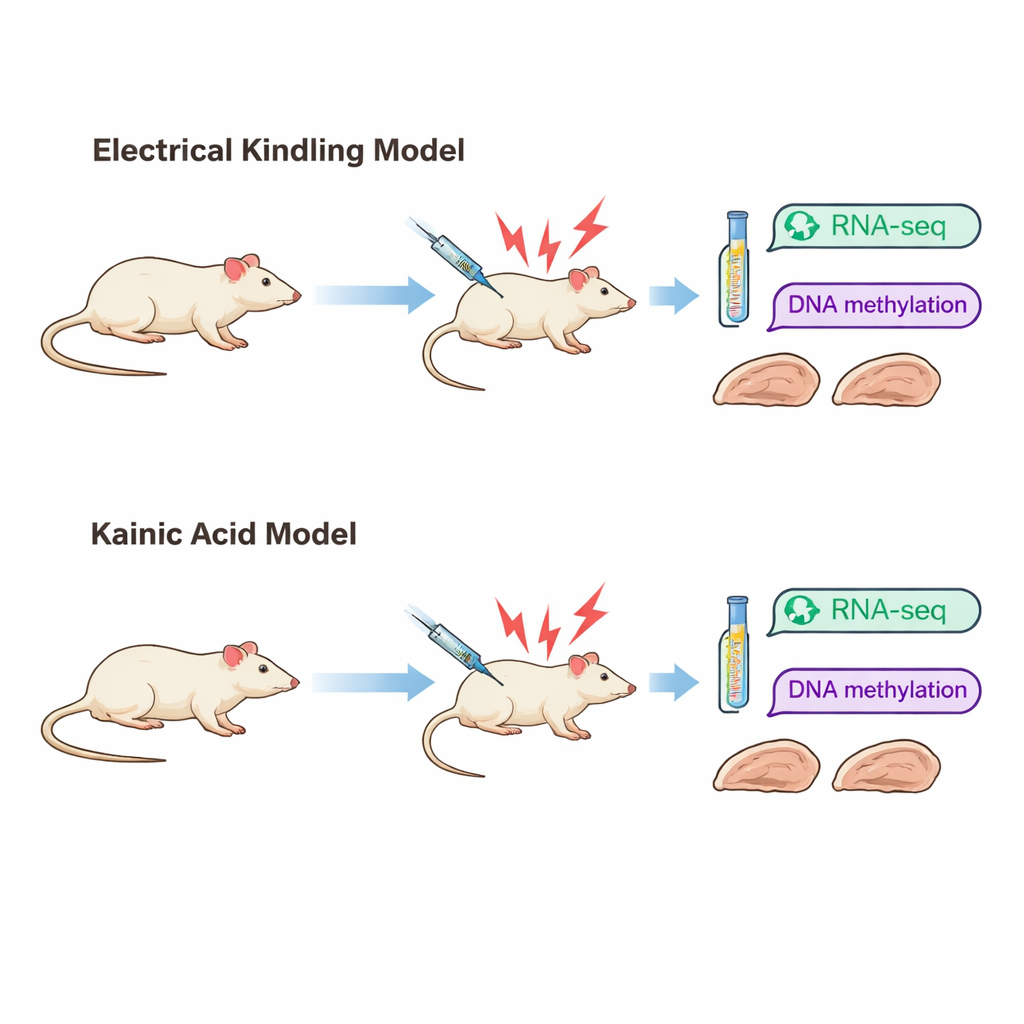
Les chercheurs se sont concentrés sur l’épilepsie du lobe temporal, une forme courante de la maladie qui résiste souvent au traitement. Ils ont utilisé deux modèles de rat bien établis qui reproduisent différentes façons dont l’épilepsie peut apparaître. Dans le modèle de « kindling », de brèves impulsions électriques sont délivrées à une partie de l’hippocampe au fil du temps jusqu’à ce que les crises deviennent faciles à déclencher. Dans le modèle par « acide kainique », une substance chimique provoque un épisode intense de crises, suivi plus tard par l’apparition de crises spontanées. Bien que les deux modèles produisent en fin de compte un comportement externe similaire — des convulsions sévères — les lésions cérébrales observées sont très différentes. Les rats soumis au kindling conservent globalement la structure tissulaire, tandis que les rats traités par acide kainique présentent une perte cellulaire marquée et des cicatrices dans des régions clés de l’hippocampe.
Lire l’activité génétique du cerveau
Pour voir comment ces chemins divergents vers l’épilepsie modifient le cerveau au niveau moléculaire, l’équipe a examiné l’hippocampe après que des rats de chaque modèle eurent subi trois crises sévères. Ils ont mesuré quels gènes étaient plus ou moins actifs par séquençage de l’ARN, et ont cartographié des marques chimiques appelées groupes méthyle sur l’ADN à l’aide d’une méthode connue sous le nom de bisulfite réduit représentatif. Les changements d’activité des gènes reflètent la manière dont les cellules répondent et s’adaptent, tandis que les marques de méthylation sont souvent vues comme une « mémoire » à plus long terme pouvant influencer l’activation ou la répression des gènes.
Les changements d’activité génique dépassent les marques d’ADN
Les deux modèles ont produit des schémas d’activité génique remarquablement différents. Le modèle de kindling a montré des changements dans plus de dix fois plus de gènes que le modèle par acide kainique. Pourtant, lorsque les chercheurs ont recoupé les deux listes, ils ont tout de même trouvé plus d’une centaine de gènes modifiés dans les deux modèles, et la plupart évoluaient dans la même direction. Un exemple est Mmp9, un gène lié à la restructuration des connexions neuronales et aux dommages associés aux crises ; il était fortement augmenté dans les deux modèles. Ces changements partagés suggèrent l’existence de réponses génétiques fondamentales à l’épileptogenèse, même lorsque le déclencheur initial et les lésions visibles diffèrent.
Les marques d’ADN racontent une autre histoire
Lorsque l’équipe a examiné la méthylation de l’ADN, le tableau a changé. Les deux modèles présentaient de nombreux gènes avec une méthylation altérée, et il existait un recoupement conséquent entre eux. Cependant, seule une sous-partie modeste de gènes présentait à la fois une méthylation altérée et une activité modifiée au sein du même modèle, et encore moins se comportaient ainsi dans les deux modèles. Pour certains de ces gènes communs, comme Nedd9 et Ptpre, l’expression augmentait dans les deux modèles, mais la direction du changement de la méthylation de l’ADN à des sites individuels pouvait être opposée entre les modèles. Dans l’ensemble, il n’y avait pas de règle simple du type « plus de méthylation = moins d’activité génique » ou l’inverse. Cela suggère que, dans ces modèles d’épilepsie, la plupart des modifications de l’activité des gènes ne sont pas directement entraînées par des changements étendus de la méthylation de l’ADN.
Ce que cela signifie pour les traitements futurs
Pour ceux qui espèrent de meilleurs traitements contre l’épilepsie, ces résultats apportent à la fois prudence et orientation. Les travaux montrent que les programmes génétiques activés lors du développement de l’épilepsie peuvent être assez spécifiques au modèle, et que la méthylation de l’ADN n’est qu’une partie d’un tableau de régulation plus vaste et plus complexe. Les cibles géniques prometteuses identifiées dans un seul modèle animal peuvent ne pas se généraliser, elles doivent donc être testées dans plusieurs modèles avant d’envisager une traduction vers l’homme. En même temps, le petit ensemble de gènes qui change à la fois en expression et en méthylation à travers les modèles peut représenter des points de départ particulièrement robustes pour développer des thérapies modifiant la maladie, visant non seulement à calmer les crises mais aussi à prévenir l’installation de l’épilepsie.
Citation: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Mots-clés: épileptogenèse, méthylation de l'ADN, expression génique, épilepsie du lobe temporal, modèles de rat