Clear Sky Science · fr
Réponses bioénergétiques et migratoires des fibroblastes gingivaux humains à la photobiomodulation par diode laser 940 nm
La lumière pour aider les blessures buccales à cicatriser
Quiconque s’est fait arracher une dent ou a subi une chirurgie gingivale connaît l’inconfort de la cicatrisation dans la bouche. Les tissus subissent en permanence des sollicitations liées à la mastication, la parole et la présence de bactéries ; tout ce qui peut accélérer la réparation en toute sécurité intéresse donc beaucoup les dentistes et les patients. Cette étude a exploré si un laser dentaire courant, utilisé à très faible puissance, peut « guider » en douceur les cellules gingivales pour qu’elles travaillent davantage et se déplacent plus vite lors de la reconstruction du tissu lésé, sans les brûler ni les endommager.
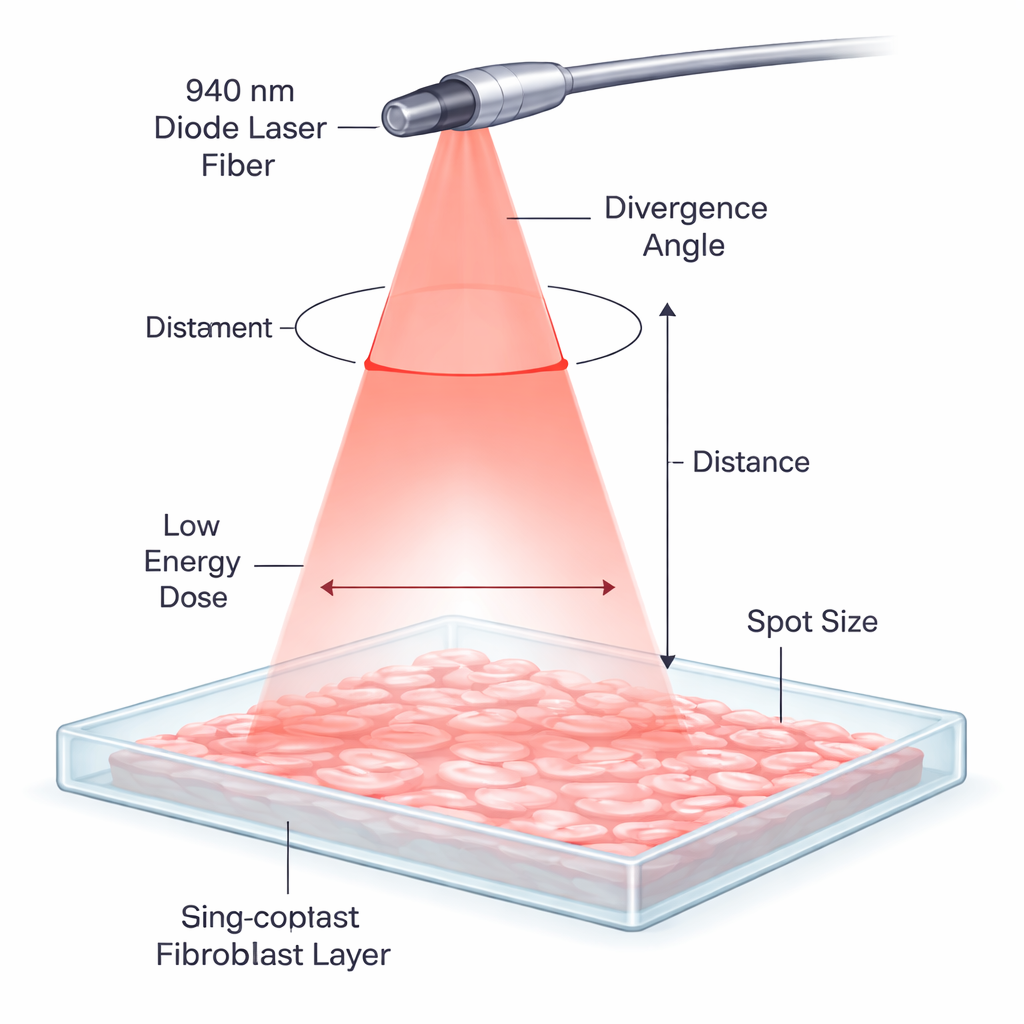
En quoi un laser doux diffère d’un laser de coupe
Dans de nombreux cabinets dentaires, des lasers à diode sont couramment employés pour couper ou remodeler les tissus mous en générant de la chaleur. Ici, le même type de laser de 940 nanomètres a été réglé à faible puissance et utilisé d’une manière très différente. Au lieu de toucher et de brûler le tissu, la lumière a été délivrée pendant une seconde seulement depuis une courte distance, se diffusant en un cône doux au-dessus d’une fine couche de cellules gingivales humaines cultivées en plaque. À ces doses faibles, l’objectif n’est pas de couper mais de stimuler légèrement les rouages internes des cellules, un processus appelé photobiomodulation, afin qu’elles réparent et réorganisent plus efficacement leur structure.
Évaluer l’énergie et la sécurité des cellules gingivales
Les chercheurs se sont concentrés sur les fibroblastes, les cellules principales responsables de la production des fibres et de la matrice qui confèrent leur résistance aux tissus gingivaux. Des fibroblastes gingivaux humains d’origine commerciale ont été cultivés en couches uniformes et exposés à trois doses d’énergie différentes du laser 940 nm, tandis qu’un quatrième groupe n’a reçu aucune lumière. L’équipe a ensuite mesuré plusieurs marqueurs : l’activité métabolique des cellules, l’intégrité de leur membrane externe, la quantité de carburant cellulaire (ATP) produite, et la libération d’oxyde nitrique, une molécule associée à l’inflammation. Pour toutes les doses de laser testées, les cellules n’ont montré aucun signe de fuite ou de blessure et n’ont pas déclenché de signal inflammatoire, indiquant que l’exposition lumineuse brève était douce et biologiquement compatible dans les conditions expérimentales.
Plus de « carburant » cellulaire et un point optimal pour le mouvement
Bien que les cellules soient restées saines dans tous les groupes, leur production d’énergie a évolué de façon dépendante de la dose et du temps. À des niveaux lumineux modérés, les fibroblastes ont augmenté la production d’ATP, la monnaie énergétique universelle des cellules, d’environ un quart par rapport aux cellules non traitées après 24 heures. Leur activité métabolique globale a également augmenté modérément, en particulier à la dose la plus élevée. Pour vérifier si cette énergie supplémentaire se traduisait par un meilleur comportement réparateur, les scientifiques ont pratiqué une « éraflure » droite dans la couche cellulaire et ont utilisé l’imagerie holographique numérique pour observer la vitesse à laquelle les cellules rampent pour combler l’écart. Ils ont constaté qu’une dose de laser plus faible augmentait légèrement la vitesse de migration et conduisait à la fermeture la plus rapide, tandis que la dose la plus élevée ralentissait en fait le mouvement et retardait la fermeture, même si les niveaux d’énergie restaient élevés. Ce schéma, où une stimulation légère aide mais un excès commence à gêner, est connu sous le nom de réponse biphasique.
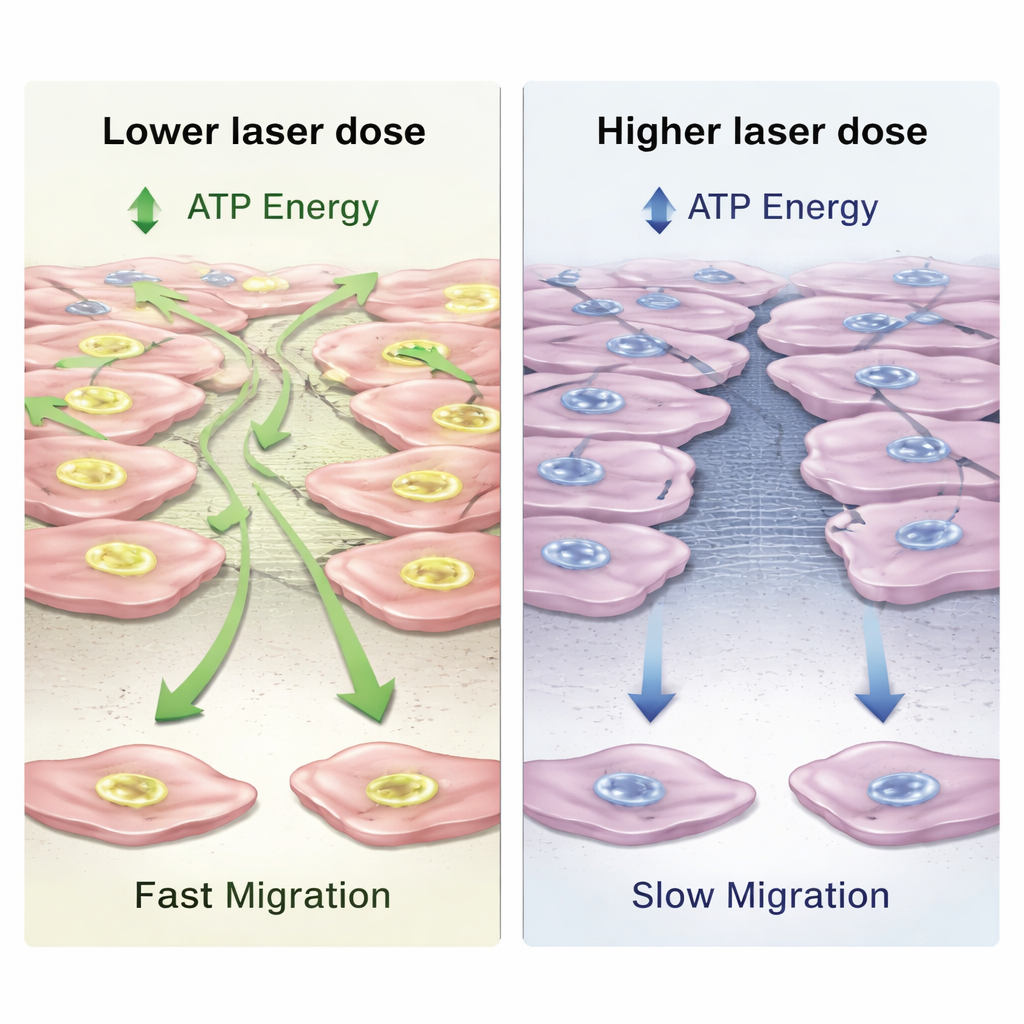
Ce que cela pourrait signifier pour la cicatrisation dentaire
Parce que ces expériences ont été réalisées dans un modèle simplifié en plaque, elles ne peuvent pas capturer pleinement la complexité d’une plaie en cours de cicatrisation dans une bouche vivante, où la circulation sanguine, les cellules immunitaires et les bactéries jouent des rôles majeurs. Néanmoins, les résultats délimitent une fenêtre de doses lumineuses prometteuse dans laquelle un laser dentaire de 940 nm peut stimuler l’énergie des cellules gingivales et orienter leur mouvement sans causer de dommage ni d’inflammation. Le travail montre aussi que l’ajustement fin de la dose est important : les conditions qui maximisaient le « carburant » cellulaire n’étaient pas exactement les mêmes que celles qui produisaient la fermeture la plus rapide de la plaie artificielle.
Message essentiel pour patients et cliniciens
Pour les non-spécialistes, le message principal est que la lumière laser de faible intensité, soigneusement contrôlée, pourrait un jour aider les gencives à cicatriser plus rapidement et de façon plus prévisible après des interventions telles que greffes, implants ou extractions. Dans cette étude, une exposition très brève et sans contact à un laser à diode de 940 nm a encouragé des cellules gingivales en culture à rester saines, à produire plus d’énergie et — dans une plage de doses appropriée — à migrer plus rapidement pour sceller un espace ressemblant à une plaie. Ces paramètres ne sont pas encore prêts à être appliqués directement en clinique, mais ils fournissent une base scientifique pour de futures études animales et humaines visant à transformer un laser dentaire courant en un outil précis pour favoriser la réparation tissulaire naturelle plutôt que de se limiter à la coupe.
Citation: Mizrahi, I.K., Neculau, C., Balasea, B.V. et al. Cellular bioenergetic and migratory responses of human gingival fibroblasts to 940 nm diode laser photobiomodulation. Sci Rep 16, 5972 (2026). https://doi.org/10.1038/s41598-026-35824-8
Mots-clés: guérison des blessures gingivales, thérapie laser de faible intensité, rétablissement après chirurgie buccale, photobiomodulation, fibroblastes gingivaux