Clear Sky Science · fr
Le stress mécanique favorise la migration hétérogène de cellules du cancer du poumon dans des canaux confinés et étudie la croissance de sphéroïdes tumoraux issus de cellules migrantes en espace confiné
Pourquoi il est important que les cellules cancéreuses se faufilent
Le cancer ne se propage pas dans l’espace dégagé. Quand des cellules tumorales quittent leur site d’origine, elles doivent se comprimer pour traverser de minuscules interstices dans les tissus, les parois des vaisseaux sanguins et d’autres structures encombrées. Cette étude pose une question simple mais puissante : parmi une population mixte de cellules du cancer du poumon, lesquelles parviennent réellement à franchir ces passages étroits, et quel type de tumeurs forment-elles par la suite ? Les réponses peuvent aider à expliquer pourquoi certaines cellules cancéreuses sont plus dangereuses que d’autres et pourraient guider de nouvelles façons de prédire ou de ralentir les métastases.
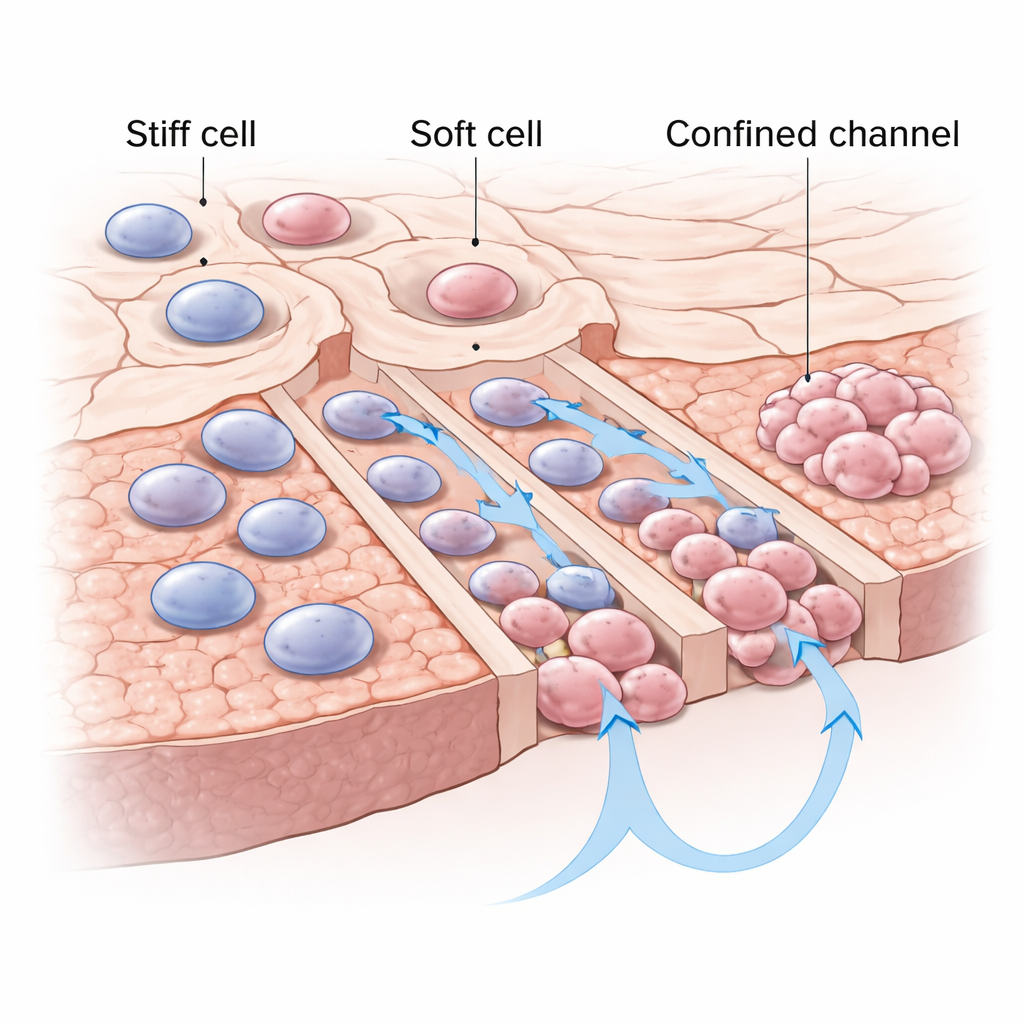
Les cellules plus molles gagnent dans les espaces étroits
Les auteurs se sont concentrés sur un trait physique des cellules que peu de gens connaissent : la raideur. Certaines cellules cancéreuses sont relativement rigides, tandis que d’autres sont molles et facilement déformables. En utilisant des puces microfluidiques spécialement conçues — de petits dispositifs en plastique gravés de canaux plus étroits qu’une cellule typique — ils ont piégé des cellules du cancer du poumon individuelles à l’entrée de canaux étroits (confinés) et de canaux hauts (non confinés). Après 24 heures, plus de cellules individuelles ont choisi et réussi à traverser les canaux étroits et confinés que les voies plus ouvertes, et elles se déplaçaient plus rapidement à l’intérieur de ces passages serrés. Lorsque les chercheurs ont ensuite sondé la mécanique des cellules avec un microscope à force atomique (une sorte de « doigt » à l’échelle nanométrique), ils ont constaté que les migrantes des canaux confinés étaient systématiquement plus molles que leurs homologues qui étaient restées ou avaient migré dans des canaux non confinés.
Une signature moléculaire de la douceur
Pour comprendre ce qui rendait certaines cellules plus molles, l’équipe a examiné une protéine structurale appelée vimentine et une protéine de soutien nucléaire codée par le gène LMNA. La vimentine fait partie de l’armature interne qui aide la cellule à résister à la déformation. Les cellules ayant traversé des canaux confinés montraient des niveaux de vimentine plus faibles comparées aux cellules dans des canaux spacieux ou en cultures classiques. L’imagerie haute résolution a révélé que, chez les migrantes confinées, le réseau de vimentine était disposé de façon plus lâche autour du corps cellulaire et près du noyau, plutôt que fortement en faisceaux. Des tests d’expression génique au niveau de la cellule unique ont confirmé que le gène de la vimentine (VIM) et LMNA, qui contribue à la robustesse mécanique du noyau, étaient régulés à la baisse dans les cellules préférant les trajets confinés.
Rendre les cellules plus molles favorise la migration confinée
Les chercheurs ont ensuite cherché à savoir s’ils pouvaient intentionnellement assouplir les cellules et observer un changement de comportement. Ils ont utilisé deux approches : un traitement biochimique (TGF-β1) connu pour remodeler le cytosquelette, et une compression mécanique douce à l’aide de plaques de silicone souple pressant sur les cellules. Les deux méthodes ont réduit la raideur et diminué les niveaux de vimentine sans tuer les cellules. Lorsque ces cellules pré-assouplies ont été introduites dans le dispositif microfluidique, une fraction encore plus importante a migré dans les canaux étroits comparativement aux cellules non traitées. Cela suggère que la douceur n’est pas seulement un effet secondaire du confinement ; c’est une propriété qui peut être ajustée et qui influence fortement la capacité d’une cellule à pénétrer et traverser de petites ouvertures.
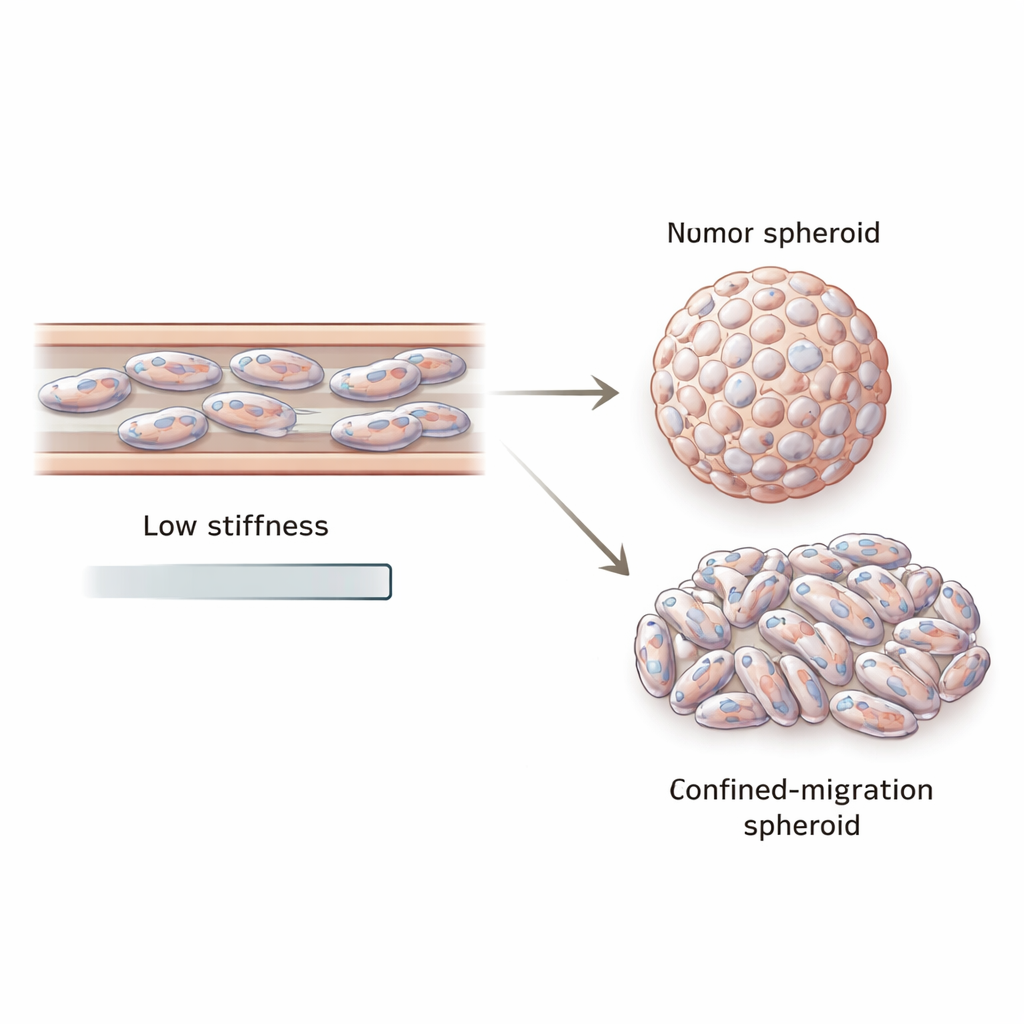
De cellules comprimées à des boules tumorales déformées
La métastase, toutefois, ne se résume pas au mouvement. Les cellules échappées doivent aussi repousser pour former de nouvelles tumeurs. Pour imiter cette étape, l’équipe a utilisé un second système confiné appelé trans-well, où les cellules migrent à travers de minuscules pores avant d’être collectées et cultivées dans des puits antiadhésifs pour former des « sphéroïdes » tumoraux tridimensionnels. Les sphéroïdes issus de cellules ayant migré en conditions confinées étaient plus petits et visiblement moins ronds que ceux issus des mêmes lignées cellulaires sans compression préalable. Leurs noyaux cellulaires étaient plus allongés et déformés, et ces sphéroïdes présentaient toujours une expression réduite de VIM et LMNA. Même au sein de sphéroïdes individuels, les niveaux de vimentine variaient du centre vers le bord, suggérant une diversité mécanique et génétique dans la tumeur fille.
Ce que cela signifie pour la compréhension des métastases
En termes simples, cette étude montre que, parmi de nombreuses cellules du cancer du poumon, les plus molles sont plus susceptibles de se glisser à travers des espaces étroits, de survivre au trajet et de former par la suite des amas tumoraux de forme étrange et mécaniquement fragiles avec des noyaux déformés. Ces cellules portent et conservent une signature moléculaire distincte — des niveaux faibles de gènes structuraux clés — qui relie leur mode de déplacement à leur mode de croissance. Bien que le travail ait été réalisé dans des dispositifs de laboratoire soigneusement contrôlés plutôt que chez des patients, il offre une feuille de route physique et génétique d’une cellule cancéreuse « migrante en confinement ». À long terme, mesurer ou cibler la douceur cellulaire et ses marqueurs moléculaires pourrait devenir une stratégie pour mieux comprendre, suivre ou éventuellement perturber les sous-populations cellulaires cancéreuses les plus invasives.
Citation: Alam, M.K., Ma, Y., Zhai, J. et al. Mechano-stress endorsing heterogeneous lung cancer cells migration into confined channels and investigating tumor spheroids growth of confined space migrating cells. Sci Rep 16, 6649 (2026). https://doi.org/10.1038/s41598-026-35818-6
Mots-clés: raideur des cellules cancéreuses, migration cellulaire confinée, sphéroïdes du cancer du poumon, vimentine et LMNA, mécanique tumorale