Clear Sky Science · fr
La fonte musculaire associée à la septicémie est atténuée par l’inhibition pharmacologique de la voie de signalisation STAT3 chez la souris
Pourquoi les infections sévères peuvent vous voler votre force
Survivre à une infection mettant la vie en danger comme la septicémie n’est qu’une partie du combat. Beaucoup de patients quittent les soins intensifs si affaiblis que marcher, monter des escaliers ou même lever les bras devient un effort. Cette étude pose une question simple mais urgente : peut‑on empêcher le corps de dégrader ses propres muscles pendant la septicémie, et si oui, comment ? À l’aide de souris, de cellules musculaires en culture et d’observations chez des patients en réanimation, les chercheurs tracent une voie de signalisation clé qui conduit à la perte musculaire — et montrent qu’un médicament ciblé peut en bloquer en partie les effets.
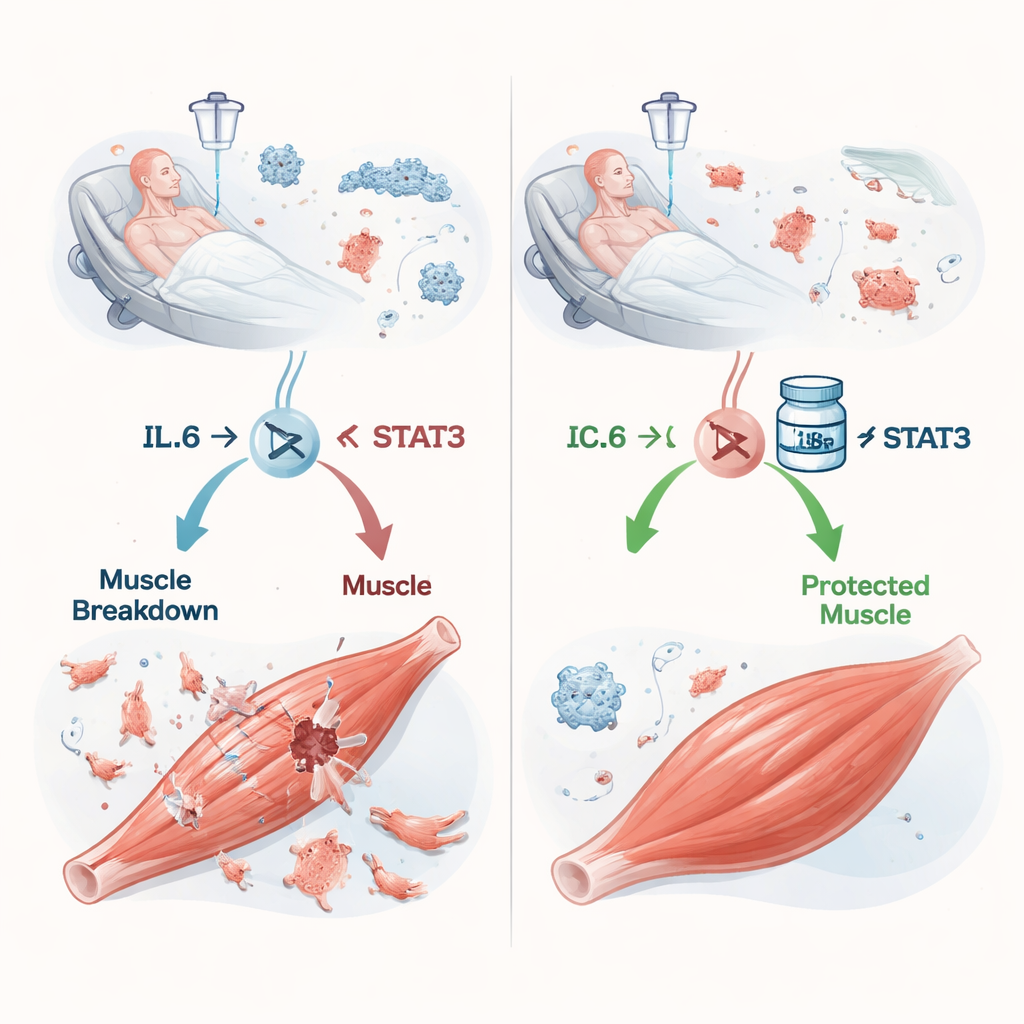
Une réaction en chaîne de l’infection à la perte musculaire
La septicémie survient lorsque la réponse de l’organisme à une infection se dérègle, inondant le sang de molécules inflammatoires. L’une des plus importantes est l’interleukine‑6 (IL‑6). Des travaux antérieurs suggéraient que l’IL‑6 peut ordonner aux muscles de dégrader leurs propres protéines, mais les détails restaient flous. Les auteurs se sont concentrés sur STAT3, une protéine intracellulaire qui relaie le signal de l’IL‑6 vers le noyau, où les gènes sont activés ou réprimés. Chez des souris recevant un culot cécal — essentiellement une infection contrôlée à bactéries mixtes — les taux d’IL‑6 dans le sang et dans les muscles des pattes ont augmenté à mesure que la septicémie s’aggravait. Parallèlement, STAT3 s’est activé dans le muscle, et les animaux ont perdu du poids, de la masse musculaire et de la force d’agrippement selon une sévérité qui reproduit étroitement ce que l’on observe chez les patients en état critique.
Comment la septicémie reprogramme les cellules musculaires
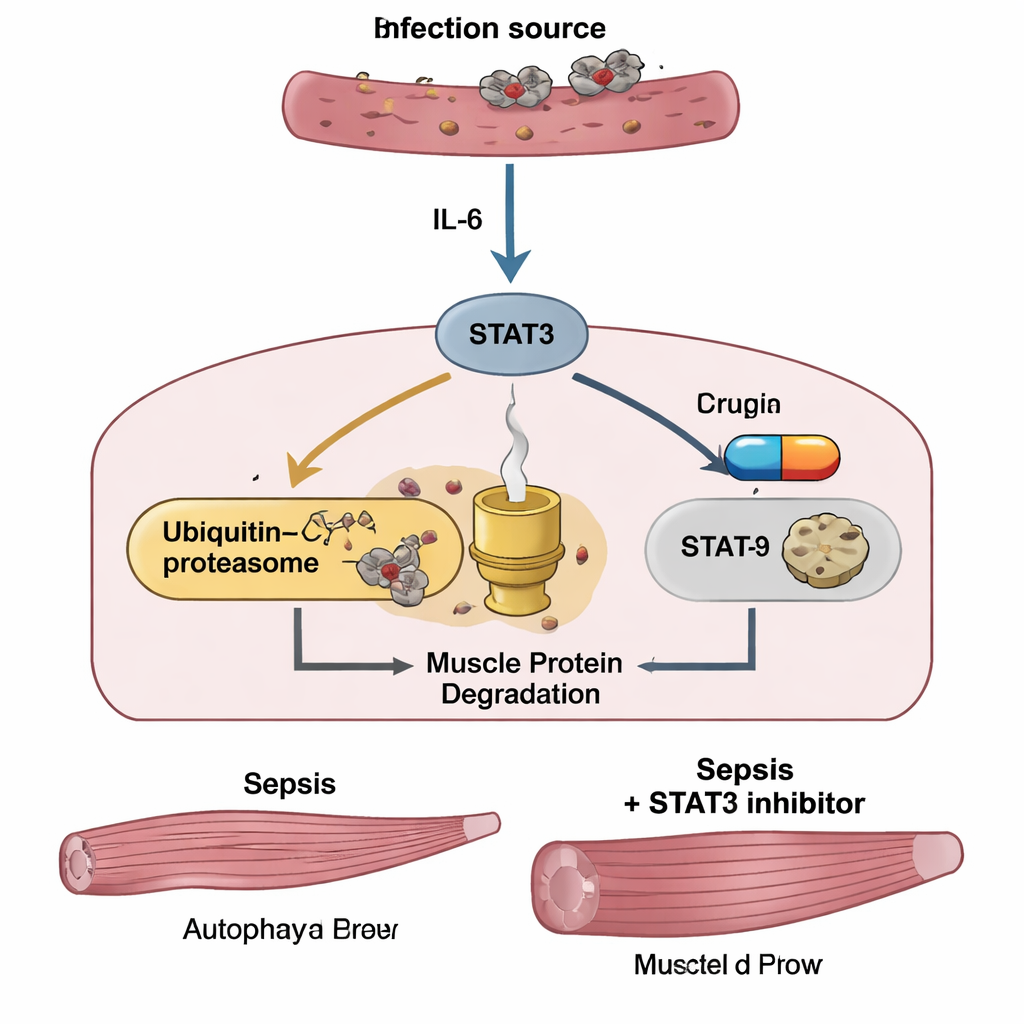
Pour comprendre ce que faisait la septicémie à l’intérieur des fibres musculaires, l’équipe a analysé l’activité génique du tibial antérieur, un muscle majeur de la jambe. Des milliers de gènes ont modifié leur expression chez les souris septiques comparées aux témoins sains. Des voies impliquées dans l’inflammation, le stress cellulaire et, en particulier, la signalisation IL‑6/STAT3 ont été activées. Deux systèmes majeurs d’élimination des protéines se sont renforcés : le système ubiquitine‑protéasome, qui étiquette des protéines musculaires spécifiques pour destruction, et l’autophagie, un processus de recyclage plus général. Les principales enzymes de « démontage musculaire », MuRF1 et atrogin‑1, ont fortement augmenté, tandis que les voies favorisant la croissance et les signaux classiques de mort cellulaire sont restés largement inchangés. Dans des expériences parallèles, des cellules musculaires de souris en culture exposées au lipopolysaccharide (LPS), un composant des parois des bactéries à Gram négatif, ont montré le même schéma : activation de l’IL‑6 et de STAT3, montée de MuRF1 et atrogin‑1, augmentation de l’autophagie et amincissement visible des fibres musculaires.
Bloquer un interrupteur clé pour protéger le muscle
L’expérience centrale a testé si l’arrêt de STAT3 pouvait épargner le muscle. Des souris séptiques ont reçu un petit inhibiteur moléculaire de STAT3 appelé C188‑9, à partir d’une heure après l’infection puis quotidiennement. Le médicament n’a pas atténué la « tempête cytokinique » initiale : les taux sanguins d’IL‑6 et d’un autre facteur inflammatoire, le TNF‑α, sont restés élevés, et le poids corporel et l’appétit ne se sont pas rapidement rétablis. Pourtant C188‑9 a clairement protégé le muscle squelettique : les souris traitées ont conservé davantage de masse du tibial, eu une prise plus forte et présenté des fibres musculaires plus volumineuses au microscope que les souris septiques non traitées. Dans les muscles, C188‑9 a fortement réduit STAT3 activé et abaissé les niveaux de MuRF1 et atrogin‑1, tout en laissant les marqueurs de l’autophagie pour l’essentiel inchangés. Dans les expériences sur gélule, le prétraitement des cellules musculaires par C188‑9 a de la même manière atténué l’activation de STAT3 et la hausse de MuRF1 et atrogin‑1, et empêché le rétrécissement des fibres induit par le LPS, encore une fois sans inhiber l’autophagie.
Indices tirés des patients en unité de soins intensifs
Pour savoir si ces mécanismes sont pertinents chez l’homme, les chercheurs ont suivi 67 adultes atteints de septicémie admis en réanimation au Japon. Les analyses sanguines à l’admission ont montré que les patients en choc septique avaient des taux d’IL‑6 particulièrement élevés. Dans l’ensemble du groupe, l’IL‑6 — mais pas le TNF‑α — corrélait étroitement avec les scores de sévérité de la septicémie et avec les marqueurs sanguins d’inflammation et de dommage musculaire. Dans un sous‑groupe de 45 patients ayant subi deux scanners abdominaux, les taux d’IL‑6 à l’admission ont prédit l’ampleur de la réduction du muscle psoas au bas de la colonne vertébrale sur les 1 à 3 semaines suivantes. Ceux qui ont perdu le plus de muscle présentaient une survie à deux ans nettement pire que ceux qui ont conservé davantage de masse musculaire, soulignant que la fonte liée à la septicémie n’est pas qu’une question esthétique : elle est associée à une mortalité à long terme.
Ce que cela pourrait signifier pour de futurs traitements
En rassemblant les données issues des souris, des cellules et des patients, une histoire plausible émerge : pendant la septicémie, l’IL‑6 en forte hausse active STAT3 dans le muscle, ce qui à son tour amplifie un système de dégradation des protéines qui dépouille les fibres musculaires de leur machinerie contractile. L’autophagie augmente également mais semble moins directement contrôlée par STAT3. En bloquant pharmacologiquement STAT3 avec C188‑9, les chercheurs ont pu interrompre cette voie d’« autocannibalisme » chez la souris et dans les cellules musculaires en culture, préservant la force même si l’infection et l’inflammation persistaient. Bien que ce travail soit encore préclinique et n’établisse pas que les inhibiteurs de STAT3 aideront les patients humains, il désigne l’axe IL‑6/STAT3 comme une cible prometteuse pour des médicaments visant à prévenir ou réduire l’affaiblissement musculaire profond qui affecte de nombreux survivants de la septicémie.
Citation: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Mots-clés: septicémie, fonte musculaire, STAT3, inflammation, rétablissement après maladie critique