Clear Sky Science · fr
Aromaticité hyperconjugative de type Schleyer dans les isomères CH des diazoles révélée par DFT et analyse NBO
Pourquoi les molécules en anneau comptent
Les chimistes savent depuis longtemps que certaines molécules en anneau sont exceptionnellement stables et se comportent de façon particulière. Cette propriété, appelée aromaticité, sous-tend tout, de l’odeur de l’essence au fonctionnement de nombreux médicaments. Dans cette étude, les chercheurs ont examiné comment de petites attaches chimiques, ou substituants, peuvent augmenter ou diminuer cette stabilité au sein d’une famille d’anneaux contenant de l’azote, les diazoles. En comprenant et en maîtrisant cet effet subtil, les scientifiques peuvent concevoir des molécules dont la réactivité est plus prévisible, ce qui est crucial pour la découverte de médicaments et pour les matériaux avancés.
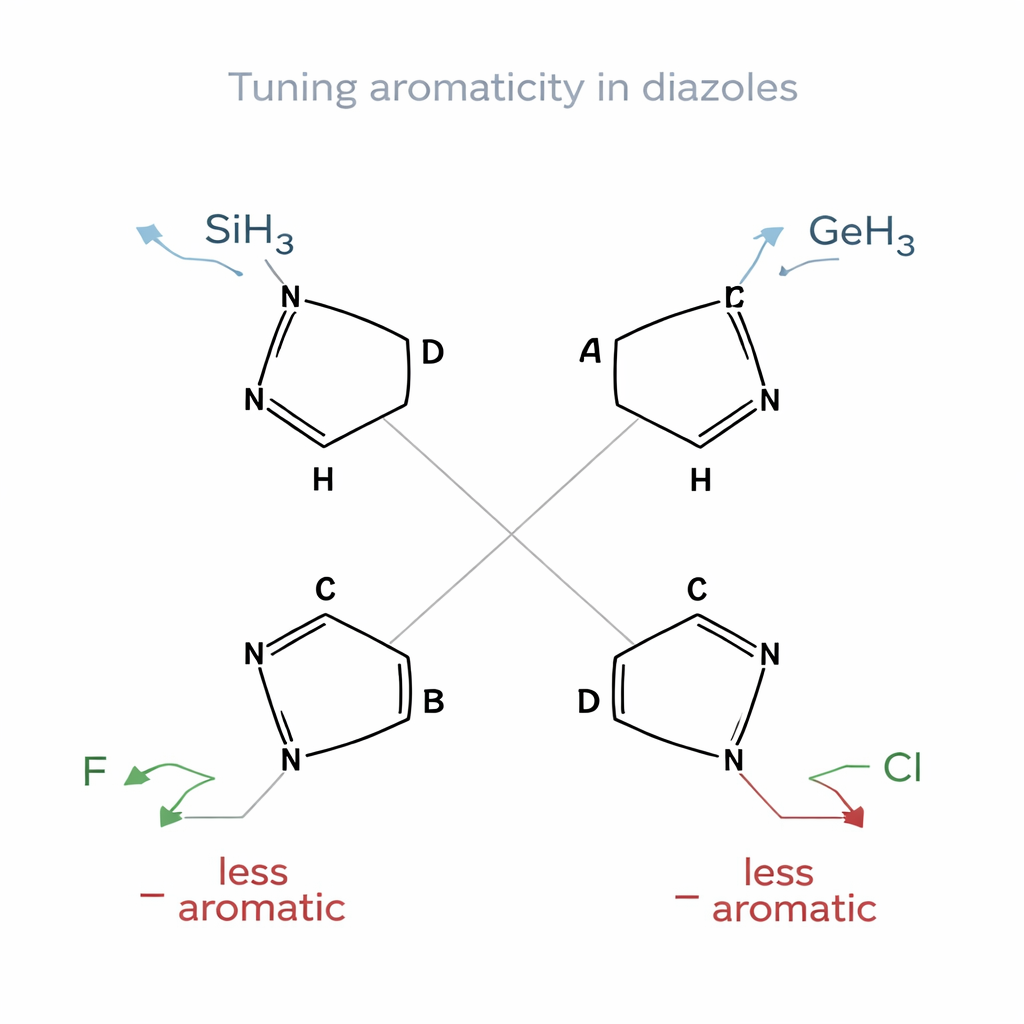
Façonner la stabilité par de petits changements
Les diazoles sont des cycles à cinq atomes contenant deux azotes et trois carbones ; ici, les auteurs se sont concentrés sur les tautomères « CH » moins courants, où une position du cycle est un groupe carbone–hydrogène au lieu de la forme habituelle azote–hydrogène. Ils ont étudié quatre dispositions différentes des atomes d’azote, étiquetées A à D, chacune modifiant la distribution électronique autour de l’anneau. Sur ces échafaudages, ils ont greffé une série de groupes simples, comme l’hydrogène, le méthyle, des halogènes tels que le fluor et le chlore, des atomes plus lourds comme le silicium et le germanium, et des donneurs ou accepteurs classiques tels que l’amino (–NH₂), l’hydroxy (–OH), le cyano (–CN) et l’hydrure de bore (–BH₂). Grâce à des calculs de chimie quantique, ils ont évalué comment chaque substituant modifiait le caractère aromatique de l’anneau et sa stabilité globale.
Comment l’équipe a mesuré l’aromaticité
L’aromaticité ne se mesure pas directement, aussi l’équipe a-t-elle utilisé plusieurs métriques complémentaires. Des indices structuraux, tels que HOMED et l’indice de Bird, suivent l’uniformité des longueurs de liaison dans l’anneau ; des liaisons plus égales signalent généralement un caractère aromatique plus marqué. Des indices magnétiques, connus sous le nom de valeurs NICS, sondent de faibles champs magnétiques générés par les électrons en circulation, signature des anneaux aromatiques. Enfin, une méthode électronique appelée analyse Natural Bond Orbital (NBO) quantifie l’ampleur du flux électronique d’une liaison vers une autre, donnant une mesure de la stabilisation hyperconjugative. En comparant ces différents indicateurs, les chercheurs ont construit une image multidimensionnelle de la façon dont chaque substituant affecte la délocalisation électronique dans les diazoles.
Gagnants et perdants pour renforcer les courants de ring
Un schéma clair est apparu. Les substituants contenant du silicium (–SiH₃) et du germanium (–GeH₃) ont systématiquement renforcé l’aromaticité dans les quatre familles de diazoles. Les cycles portant ces groupes présentaient des longueurs de liaison plus uniformes, des courants de ring calculés plus intenses et de grandes énergies de stabilisation issues du don électronique vers le système de l’anneau. Ce comportement s’accorde avec le concept d’aromaticité hyperconjugative de type Schleyer, où certaines liaisons σ agissent comme de puissants donneurs vers le circuit aromatique. Un petit pont contraint de type cyclopropyle (–CH₂–CH₂–) a également renforcé l’aromaticité, agissant comme un donneur de force intermédiaire. À l’opposé, le fluor, et dans une moindre mesure le chlore, ont eu tendance à drainer la densité électronique de l’anneau, atténuant les courants et, dans certains cas, effaçant presque complètement le caractère aromatique.
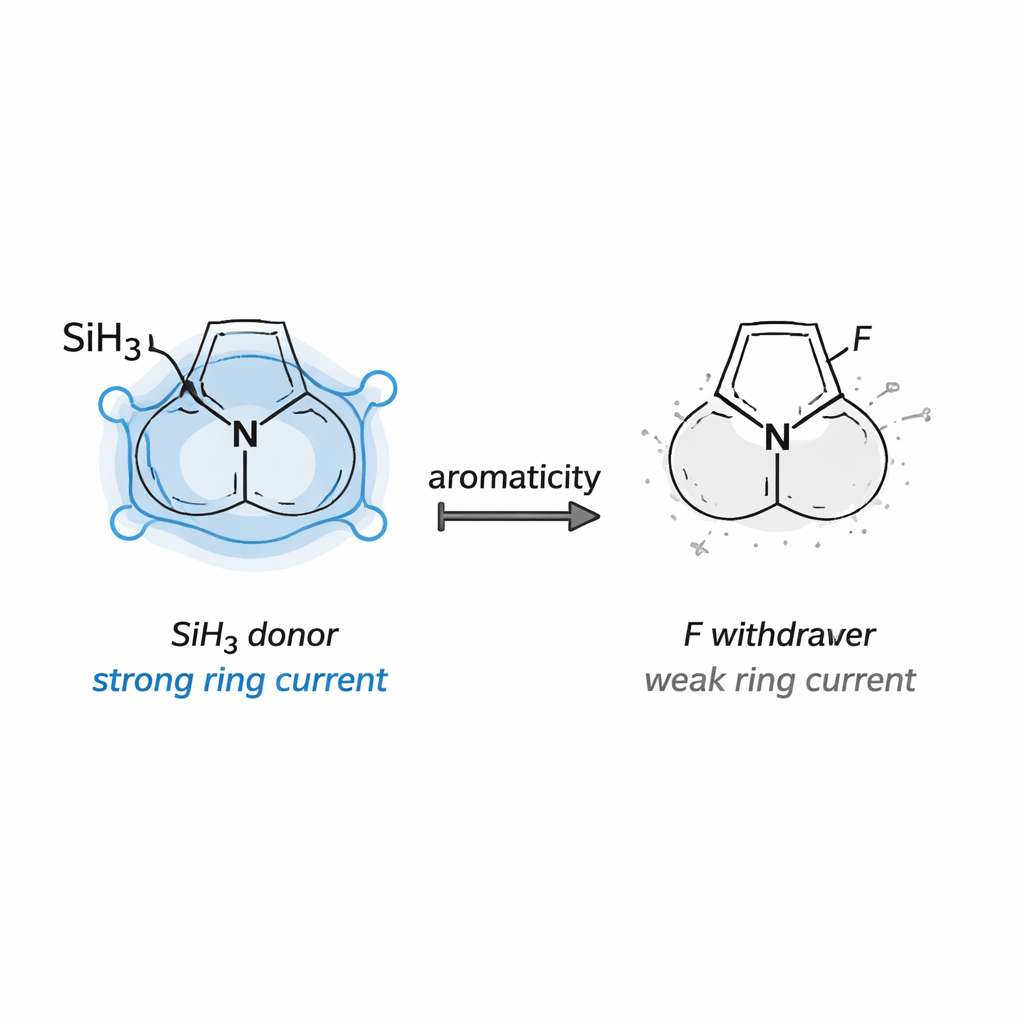
Surprises venant des donneurs et accepteurs classiques
Des groupes donneurs π classiques tels que –NH₂ et –OH, souvent utilisés pour enrichir la densité électronique dans les systèmes aromatiques, n’ont eu ici que des effets modestes. Ils ont légèrement amélioré l’égalisation des liaisons et les courants de ring, mais n’ont jamais égalé l’impact des substituants silicium et germanium. Encore plus frappante est la différence entre le cyano (–CN) et l’hydrure de bore (–BH₂). Les deux sont formellement pauvres en électrons, mais ils se sont comportés très différemment. Le groupe cyano a généralement affaibli l’aromaticité en attirant la densité électronique hors de l’anneau. En revanche, –BH₂ s’est révélé être un promoteur d’aromaticité surprenamment puissant : ses liaisons ont donné de la densité électronique au réseau de l’anneau, à l’instar de –SiH₃ et –GeH₃, générant une stabilisation hyperconjugative importante.
Une histoire confirmée par de nombreuses mesures
Lorsque les auteurs ont comparé tous leurs indices, le message était cohérent. Mesures structurales, réponses magnétiques et énergies de stabilisation électronique évoluaient de concert : les anneaux qui apparaissaient géométriquement plus proches du benzène étaient aussi ceux présentant les courants de ring calculés les plus forts et la plus grande stabilisation hyperconjugative. Les systèmes fluorés se regroupaient à l’extrémité de faible aromaticité sur toutes les échelles, tandis que les anneaux substitués par le silicium, le germanium, le groupe cyclopropyle et –BH₂ occupaient l’extrémité de forte aromaticité. Pour un lecteur généraliste, l’idée principale est qu’en choisissant les bons substituants et les bonnes positions sur un anneau, les chimistes peuvent ajuster le flux électronique dans de petits circuits moléculaires. Ce travail cartographie comment s’opère ce réglage dans les échafaudages diazole, offrant des règles de conception pratiques pour créer des molécules aromatiques plus stables, plus réactives ou plus contrôlables.
Citation: Dehkordi, P.N., Saeidian, H., Mirjafary, Z. et al. Schleyer-type hyperconjugative aromaticity in CH isomers of diazoles revealed by DFT and NBO analysis. Sci Rep 16, 7131 (2026). https://doi.org/10.1038/s41598-026-35776-z
Mots-clés: aromaticité, diazoles, hyperconjugaison, effets de substituants, chimie computationnelle