Clear Sky Science · fr
Exploration préliminaire de l'analyse radiomique mammographique dans le cancer du sein triple négatif en relation avec le profil BRCA
Pourquoi les images mammaires peuvent en dire plus qu’il n’y paraît
Quand la plupart des gens pensent à une mammographie, ils imaginent un médecin cherchant des masses évidentes ou des zones suspectes. Cette étude pose une question plus profonde : les motifs subtils présents sur une radiographie mammaire standard pourraient‑ils aussi révéler si une femme porte des mutations héréditaires à haut risque, comme dans les gènes BRCA, avant même l’intervention d’un pathologiste ou d’un test génétique ? Si c’est le cas, les images courantes utilisées pour détecter le cancer pourraient également aider à signaler des femmes à risque héréditaire accru, orientant vers un suivi plus rapproché ou un conseil génétique.
Un type agressif de cancer du sein et le risque héréditaire
Les chercheurs se sont concentrés sur le cancer du sein triple négatif, une forme particulièrement agressive qui n’exprime pas trois marqueurs hormonaux et de croissance courants et pour laquelle les options de traitement personnalisées sont actuellement plus limitées. Les tumeurs triple négatives sont plus fréquentes chez les femmes porteuses de variantes délétères des gènes BRCA1 ou BRCA2, impliqués dans la réparation de l’ADN endommagé. Cependant, aujourd’hui, la confirmation de ces mutations nécessite encore un test génétique. L’équipe s’est demandé si les mammographies elles‑mêmes pourraient contenir des indices cachés — trop subtils pour l’œil humain — distinguant, parmi des patientes déjà diagnostiquées de triple négatif, celles qui portent ou non une mutation BRCA.
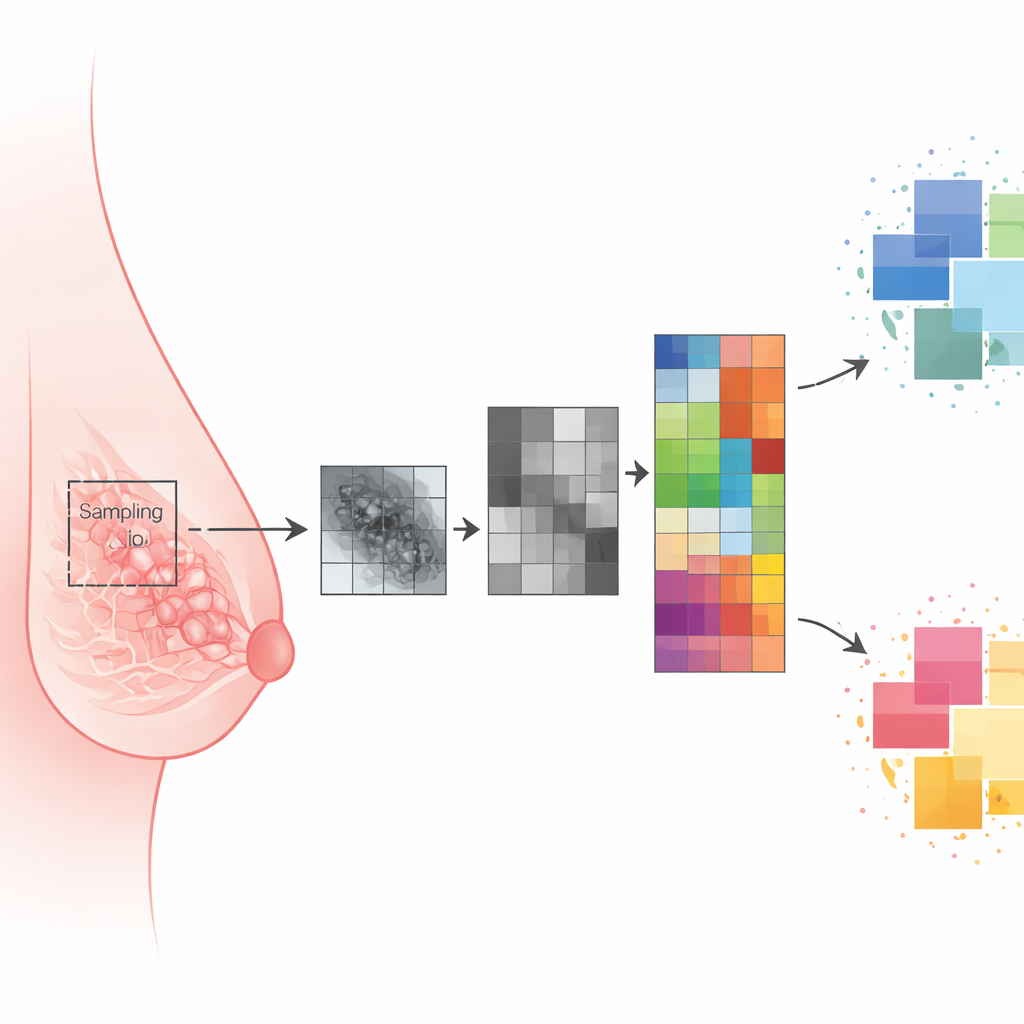
Transformer des mammographies en chiffres
Pour explorer cette hypothèse, les scientifiques ont réalisé une analyse rétrospective de 52 femmes atteintes d’un cancer du sein triple négatif ayant subi une mammographie numérique avant tout traitement et dont le statut BRCA était connu. Treize femmes étaient porteuses de mutations BRCA et 39 ne l’étaient pas. Des radiologues ont délimité manuellement chaque tumeur visible sur la mammographie et ont également tracé une région ovale de taille standard dans la zone la plus homogène du sein opposé apparemment sain. À l’aide d’un logiciel open source, ils ont converti chaque région délimitée en 195 descripteurs numériques, ou « caractéristiques », qui capturent la luminosité, le contraste et la texture à petite échelle — des motifs de clair et d’obscur suggérant l’organisation tissulaire au niveau microscopique.
Laisser les algorithmes chercher des motifs significatifs
Parce que des centaines de mesures peuvent être redondantes, l’équipe a utilisé des outils statistiques pour réduire la liste à quelques caractéristiques les plus informatives et non fortement superposées. Ils ont ensuite construit trois types de modèles : un basé uniquement sur les caractéristiques du tissu mammaire sain, un utilisant uniquement les caractéristiques tumorales et un combinant les deux. Plusieurs classifieurs d’apprentissage automatique prêts à l’emploi — incluant la régression logistique, les machines à vecteurs de support et les arbres de décision — ont été entraînés et testés de manière répétée sur des sous‑ensembles aléatoires des données afin d’estimer leur capacité à distinguer les patientes porteuses de mutations BRCA des non‑porteuses.
Le tissu mammaire apparemment sain parle le plus fort
De manière surprenante, les modèles les plus précis ne provenaient pas des tumeurs elles‑mêmes mais du tissu glandulaire d’aspect normal du sein opposé. Un modèle linéaire simple fondé uniquement sur trois caractéristiques de ce tissu sain a obtenu une bonne discrimination entre porteuses et non‑porteuses de mutations, avec une spécificité élevée — c’est‑à‑dire peu de faux positifs. Une mesure de texture, dite « somme d’entropie », qui reflète le caractère aléatoire ou la complexité des motifs de pixels, était systématiquement plus élevée chez les femmes porteuses de mutations BRCA. Les auteurs suggèrent que des défauts héréditaires dans la réparation de l’ADN peuvent altérer subtilement l’architecture microscopique du tissu mammaire bien avant, ou au‑delà, de ce qui apparaît comme une masse distincte, et que cette architecture modifiée se traduit par une texture plus irrégulière sur la mammographie.
Ce que cela pourrait signifier pour les contrôles futurs
Pour le grand public, la conclusion principale est que les mammographies standard peuvent contenir beaucoup plus d’informations que celles que les radiologues exploitent actuellement. Dans cette étude préliminaire, l’analyse informatique du tissu mammaire de « fond » — pas seulement de la tumeur — a aidé à distinguer, au sein d’un groupe déjà atteint de cancer triple négatif, les femmes porteuses de mutations BRCA à haut risque de celles qui ne l’étaient pas. Si des études de plus grande envergure, multicentriques, confirment ces résultats et les intègrent aux données cliniques, les images de dépistage routinier pourraient un jour alimenter des outils non invasifs estimant le risque héréditaire et aidant à décider qui devrait se voir proposer un test génétique ou un suivi plus étroit, sans changer la manière dont la mammographie est réalisée.
Citation: Pecchi, A., Sessa, G., Nocetti, L. et al. Preliminary exploration of radiomic mammographic analysis in triple negative breast cancer related to BRCA profile. Sci Rep 16, 8765 (2026). https://doi.org/10.1038/s41598-026-35774-1
Mots-clés: cancer du sein triple négatif, mutation BRCA, mammographie, radiomique, radiogénomique