Clear Sky Science · fr
Le rôle du récepteur nicotinique α7 de l’acétylcholine dans la promotion de la polarisation des macrophages M2 sur les sites inflammatoires
Comment les nerfs contribuent à calmer une inflammation débridée
Quand on se coupe un doigt ou qu’une infection est combattue, notre organisme déclenche une inflammation pour nous protéger. Mais si cette réaction s’emballe et dure trop longtemps, elle peut endommager les tissus sains et favoriser des maladies chroniques. Cette étude examine comment un récepteur « apaisant » spécifique des cellules immunitaires, appelé récepteur nicotinique α7 de l’acétylcholine (α7nAChR), aide à orienter l’inflammation vers la réparation plutôt que vers les dégâts, offrant des pistes pour de nouveaux traitements de maladies comme la septicémie, les affections intestinales et l’arthrite.
Les deux visages des équipes de nettoyage immunitaires
Les macrophages sont des cellules immunitaires qui jouent le rôle d’équipes de nettoyage et de réparation. Ils peuvent basculer entre deux modes principaux. En mode « attaque », souvent appelé M1, ils sécrètent des molécules agressives pour tuer les microbes et déblayer les débris. En mode « réparation », dit M2, ils libèrent des signaux apaisants qui calment l’inflammation et favorisent la régénération tissulaire. Une réponse saine commence par une dominance de cellules M1 puis bascule progressivement vers M2 lorsque le danger diminue. Les auteurs ont voulu savoir si l’α7nAChR, un récepteur d’abord célèbre pour son rôle dans la communication nerveuse et les effets de la nicotine sur le cerveau, aide aussi à orienter les macrophages vers cet état réparateur M2 pendant l’inflammation.
Un commutateur lié aux nerfs favorisant la réparation
Pour étudier cela, les chercheurs ont utilisé des souris porteuses ou dépourvues de l’α7nAChR et ont déclenché une inflammation abdominale de deux manières : avec un composant bactérien (mimant une infection) et par une manipulation intestinale douce (mimant une lésion stérile chirurgicale). Ils ont mesuré des marqueurs moléculaires distinguant les comportements M1 et M2 et ont utilisé la cytométrie en flux pour compter les proportions de chaque type de macrophage. Chez les souris normales, la phase initiale de l’inflammation était dominée par des signaux M1, mais au cours des un à deux jours suivants, les marqueurs M2 augmentaient, reflétant une transition naturelle vers la réparation. Chez les souris dépourvues d’α7nAChR, en revanche, les marqueurs pro-inflammatoires étaient plus élevés, les marqueurs de réparation plus faibles, et la proportion de macrophages M2 dans la zone enflammée était systématiquement réduite, inclinant l’équilibre local vers un état riche en M1, plus dommageable.
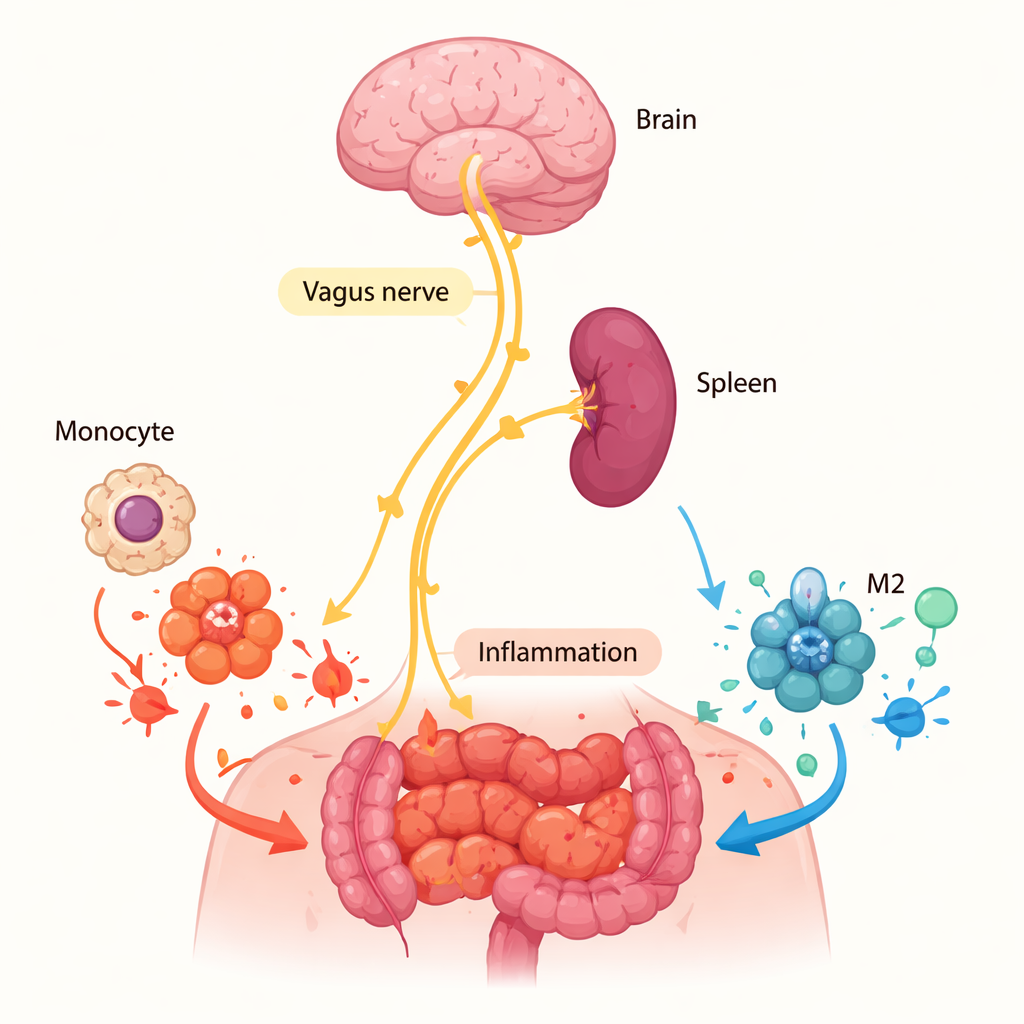
Pourquoi la rate compte plus que la plaie
L’équipe a ensuite cherché à savoir où l’α7nAChR exerçait son effet. Il aurait pu agir directement sur le site enflammé si les cellules locales libéraient de l’acétylcholine, le neurotransmetteur qui active le récepteur. Mais les mesures d’acétylcholine dans le liquide abdominal et dans les cultures cellulaires issues du tissu enflammé sont restées pratiquement nulles, ce qui plaide contre un signal local fort. L’attention s’est donc tournée vers la rate, un organe immunitaire clé déjà impliqué dans la « voie cholinergique anti-inflammatoire » contrôlée par le nerf vague. Lorsque les chercheurs ont retiré la rate chirurgicalement chez des souris normales, puis induit une inflammation abdominale, la proportion de macrophages M2 dans la cavité péritonéale a chuté et le nombre total de macrophages a diminué. Ce schéma reflétait ce qu’ils observaient chez les souris dépourvues d’α7nAChR, suggérant que des signaux pilotés par les nerfs dans la rate préparent les monocytes — précurseurs des macrophages — à devenir des cellules M2 avant même leur arrivée sur le site enflammé.
Tester le commutateur sur des cellules humaines
Pour vérifier si le même récepteur peut moduler des cellules humaines, les chercheurs ont utilisé des monocytes cultivés en laboratoire à partir d’une lignée leucémique (THP-1) et de sang humain donné. Ils ont orienté ces cellules vers un développement en macrophages M1 ou M2 en utilisant des signaux immunitaires standards, puis ont ajouté un médicament spécifique activant l’α7nAChR. Dans les deux sources cellulaires humaines, l’activation de l’α7nAChR n’a pas augmenté les marqueurs M1 mais a clairement augmenté des caractéristiques clés du phénotype M2, notamment la protéine de surface CD206 et la molécule anti-inflammatoire interleukine-10. Ces expériences soutiennent l’idée que l’α7nAChR agit comme un commutateur d’orientation, facilitant pour les macrophages en développement l’adoption d’une identité réparatrice sans pour autant éteindre entièrement la réponse immunitaire.
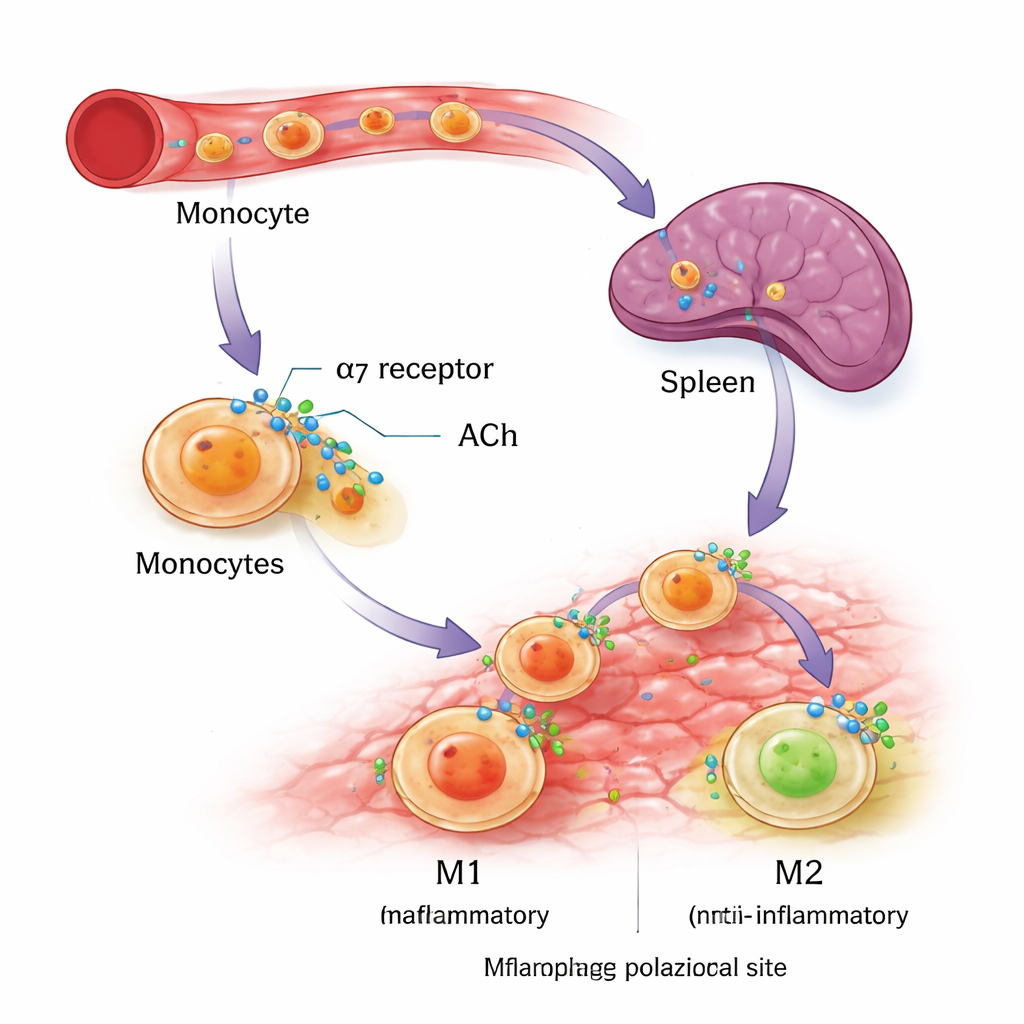
Des indices fournis par la nicotine vers de futures thérapies
Ces résultats aident à expliquer plusieurs observations intrigantes, comme pourquoi la stimulation du nerf vague peut améliorer des maladies inflammatoires et pourquoi les fumeurs, malgré de nombreux risques pour la santé, semblent présenter un risque légèrement réduit pour certaines affections intestinales — la nicotine peut activer l’α7nAChR. Plutôt que de se contenter de bloquer des molécules pro-inflammatoires, l’α7nAChR semble aider l’organisme à convertir ses équipes de nettoyage immunitaires en cellules M2 davantage orientées vers la réparation, en particulier via l’apprentissage des monocytes dans la rate. Pour le grand public, cela signifie que notre système nerveux fait plus que détecter la douleur ou contrôler les muscles : il oriente aussi discrètement les cellules immunitaires pour savoir quand combattre et quand réparer. Apprendre à actionner ce commutateur intégré en toute sécurité, par des médicaments ou une stimulation nerveuse ciblée, pourrait ouvrir de nouvelles voies pour calmer une inflammation nocive tout en préservant la capacité de défense de l’organisme.
Citation: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Mots-clés: polarisation des macrophages, inflammation, nerf vague, récepteur nicotinique de l’acétylcholine, régulation immunitaire