Clear Sky Science · fr
Formes physiologiquement pertinentes des traceurs radioactifs Tc‑ et Re‑pyrophosphate et base de leur sensibilité à l’amyloïde transthyretine
Pourquoi cette histoire d’imagerie cardiaque est importante
Beaucoup de personnes développent, en vieillissant, des dépôts silencieux de protéines mal repliées — appelés amyloïdes — dans le cœur. Certains de ces dépôts, notamment ceux formés à partir d’une protéine sanguine nommée transthyrétine, peuvent raidir le muscle cardiaque et entraîner des maladies graves. Les cliniciens s’appuient de plus en plus sur un traceur radioactif connu sous le nom de pyrophosphate de technétium‑99m (99mTc‑PYP) pour visualiser ces dépôts lors des scintigraphies. Pourtant, étonnamment, la forme exacte de ce traceur dans l’organisme et la raison pour laquelle il semble « préférer » certains types d’amyloïde restaient floues. Cet article combine théorie et expérience pour découvrir l’aspect réel du traceur en conditions proches de la physiologie et comment cette structure pourrait lui permettre de cibler les fibrilles de transthyrétine délétères.
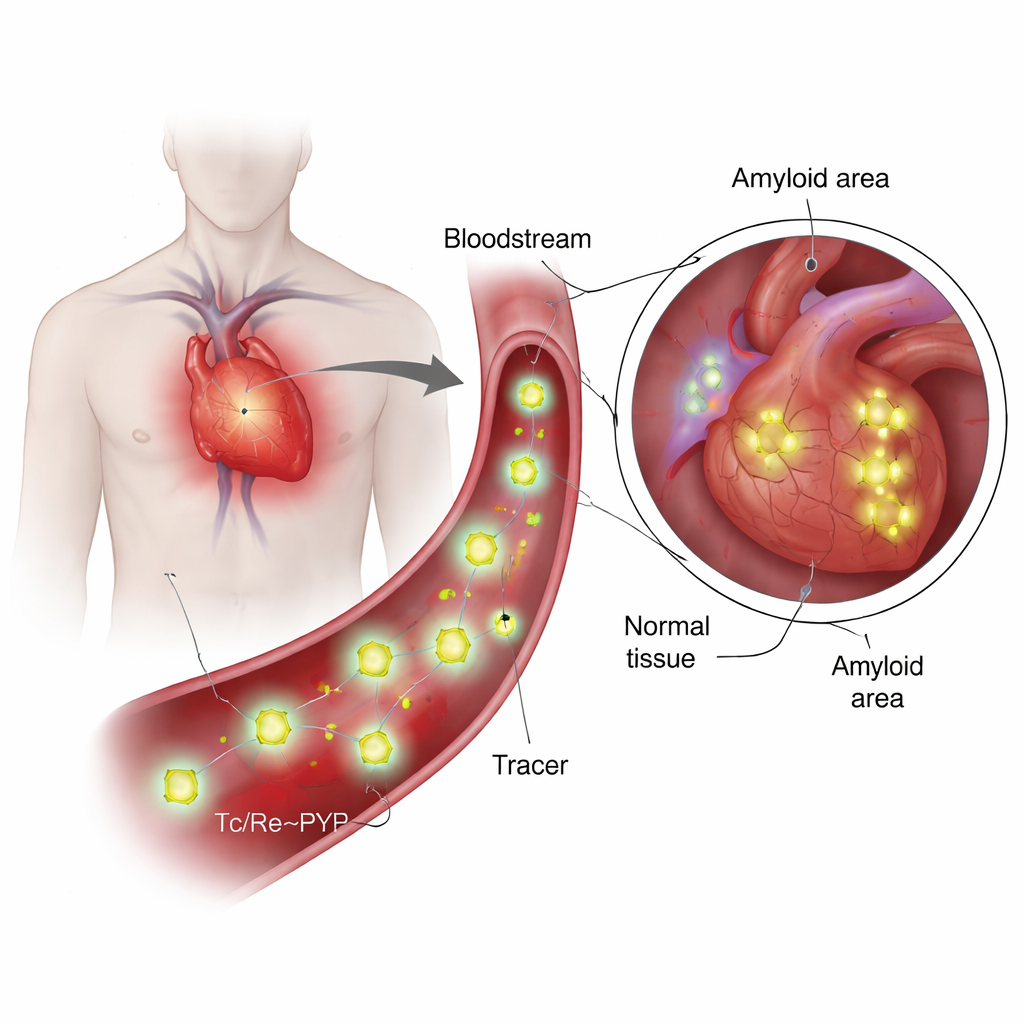
Que sont ces traceurs et qu’est‑ce qui les rend particuliers ?
Le 99mTc‑PYP est utilisé depuis des décennies pour imager l’os, car il a tendance à s’accumuler là où le calcium et le renouvellement minéral sont élevés. Plus récemment, on a découvert qu’il peut aussi différencier deux grandes formes d’amylose cardiaque : l’une constituée de chaînes légères d’anticorps (AL) et l’autre de transthyrétine (ATTR). Dans l’ATTR, le cœur s’allume souvent fortement sur les scans PYP, tandis que les cas AL restent généralement peu lumineux, même lorsque l’accumulation calcique paraît similaire. Ce décalage pose une question centrale : le traceur se fixe‑t‑il uniquement au calcium, ou interagit‑il directement avec la protéine amyloïde elle‑même ? Répondre à cela exige de connaître la véritable structure chimique du traceur dans des conditions proches de celles du sang, ce que les travaux antérieurs n’avaient qu’esquissé.
Utiliser un substitut plus sûr pour voir l’invisible
Étant donné que le technétium est radioactif et présent en très faibles quantités dans les préparations médicales, il est difficile à étudier directement avec de nombreuses techniques de laboratoire. Les auteurs ont donc utilisé le rhénium, un élément étroitement apparenté de taille et de préférences de liaison presque identiques mais présentant une chimie plus commode, comme substitut. Ils ont préparé des mélanges rhénium‑pyrophosphate dans des conditions imitant les kits cliniques PYP, puis les ont sondés avec un ensemble d’outils : calculs quantiques de haut niveau, spectroscopie d’absorption UV‑visible, diverses spectroscopies vibrationnelles (infrarouge et Raman), résonance magnétique nucléaire, spectrométrie de masse et spectroscopie Mössbauer de l’étain. Ensemble, ces méthodes leur ont permis de tester de nombreuses structures candidates et de restreindre les espèces susceptibles d’exister à pH neutre, comparable à celui du sang.
Une forme moléculaire flexible mais reconnaissable
Les éléments de preuve convergent vers une « noyau » commun : un complexe octaédrique dans lequel un atome de technétium ou de rhénium à l’état d’oxydation +4 est lié à deux groupes pyrophosphate et à deux molécules d’eau. En termes simples, le métal se trouve au centre d’une cage presque octaédrique formée par des atomes d’oxygène, les pyrophosphates jouant le rôle d’ancrages multitronchus et les molécules d’eau occupant les positions restantes. Cette unité basique diaqua dipyrophosphate n’est pas rigide. Comme les bras pyrophosphate peuvent pivoter et former des liaisons hydrogène internes avec les eaux liées, la molécule explore de nombreuses conformations légèrement différentes en solution. Les calculs et les spectres suggèrent que ces variations décalent ses empreintes d’absorption lumineuse et vibrationnelle, expliquant pourquoi les bandes expérimentales sont larges et pourquoi les études antérieures ont eu du mal à identifier une structure nette et unique.
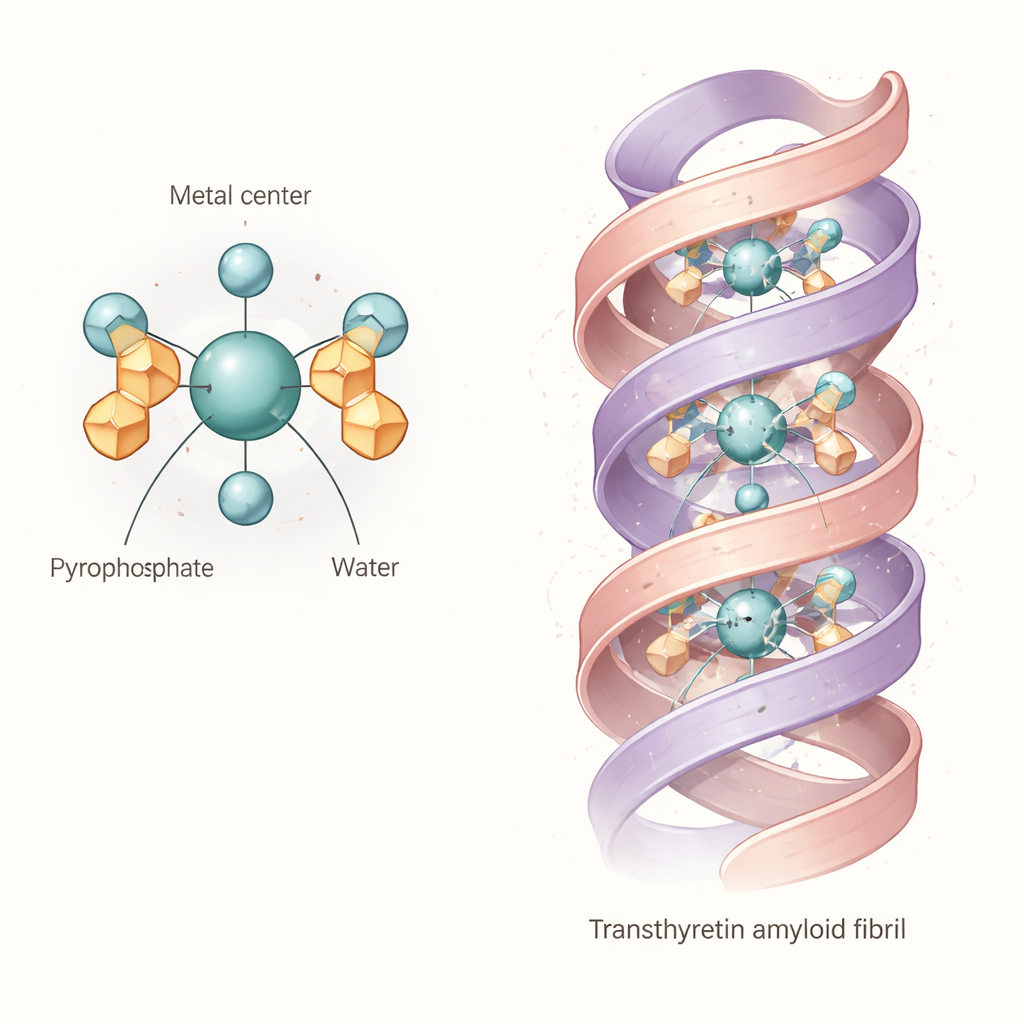
Ce que cela implique pour la fixation à l’amyloïde cardiaque
Les auteurs ont ensuite testé si ce complexe flexible pouvait plausiblement se loger directement dans les fibrilles d’amyloïde de transthyrétine. En utilisant une structure cryo‑microscopique électronique détaillée d’une fibrille humaine de transthyrétine, ils ont réalisé des recherches de dockings informatiques avec le complexe modélisé de technétium‑pyrophosphate. Les résultats montrent que l’unité diaqua dipyrophosphate peut s’insérer dans un canal central qui parcourt la fibrille, établissant de multiples liaisons hydrogène et ponts salins avec des chaînes latérales chargées bordant la cavité. Cela suggère que, du moins pour certaines conformations de fibrilles de transthyrétine, le traceur ne se contente pas de marquer des dépôts minéraux voisins ; il peut être directement enlacé par l’architecture protéique elle‑même. La « souplesse » structurelle du traceur l’aide probablement à s’adapter à des poches et des distributions de charge légèrement différentes rencontrées dans les fibrilles de patients réels.
Conséquences pour le diagnostic et les traceurs futurs
Pour un lecteur non spécialiste, la leçon est que le balayage cardiaque PYP largement utilisé repose sur un traceur plus subtil et plus conscient des protéines qu’on ne le pensait. En conditions physiologiques, il faut le considérer comme une petite cage métal‑pyrophosphate porteuse d’eau, capable de fléchir et de former de multiples points de contact avec les canaux amyloïdes de transthyrétine. Cette compréhension aide à expliquer pourquoi le traceur donne des signaux forts dans certaines maladies amyloïdes mais pas dans d’autres, et pourquoi de petites modifications de la protéine ou de son environnement peuvent provoquer des pertes de sensibilité apparemment inexplicables. En clarifiant la forme active et la répartition de charge du traceur, l’étude jette les bases de la conception d’agents d’imagerie ou thérapeutiques de nouvelle génération qui reconnaîtraient plus sélectivement les fibrilles pathogènes dans le cœur et au‑delà.
Citation: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Mots-clés: amylose cardiaque, transthyrétine, pyrophosphate de technétium, imagerie moléculaire, chimie des radiotraceurs