Clear Sky Science · fr
Activités synergiques anti-persister, inhibitrices d’efflux et antibiofilm des postbiotiques dérivés de Lactobacillus vaginal contre UPEC : vers une nouvelle thérapie pour les ITU
Pourquoi les infections urinaires tenaces comptent
Les infections urinaires (IU) sont parmi les infections bactériennes les plus fréquentes, en particulier chez les femmes, et de nombreuses personnes en souffrent de façon récurrente malgré la prise d’antibiotiques. Cette étude explore une nouvelle approche épargnant les antibiotiques pour lutter contre ces infections récalcitrantes et récidivantes : exploiter des bactéries vaginales bénéfiques et leurs produits chimiques sécrétés pour empêcher les E. coli problématiques de s’installer, de se cacher et de réapparaître.
Les survivants cachés derrière les infections répétées
Les antibiotiques classiques peuvent éliminer la plupart des bactéries, mais une petite sous-population dite « cellules persister » survit en entrant dans un état dormant à faible activité. Ces dormeurs ne sont pas résistants génétiquement, mais tolèrent des doses très élevées d’antibiotiques et peuvent se réveiller plus tard, provoquant des IU chroniques et récurrentes. Les chercheurs ont travaillé avec une souche courante responsable d’IU, E. coli UTI89, et ont montré que des antibiotiques puissants comme la colistine et le méropénem favorisent l’apparition de ces persisters. Dans des tests en laboratoire reproduisant l’urine, de faibles fractions d’E. coli ont survécu à une exposition antibiotique extrême, confirmant la facilité d’apparition des persisters et pourquoi les traitements standard échouent souvent à offrir un soulagement durable.
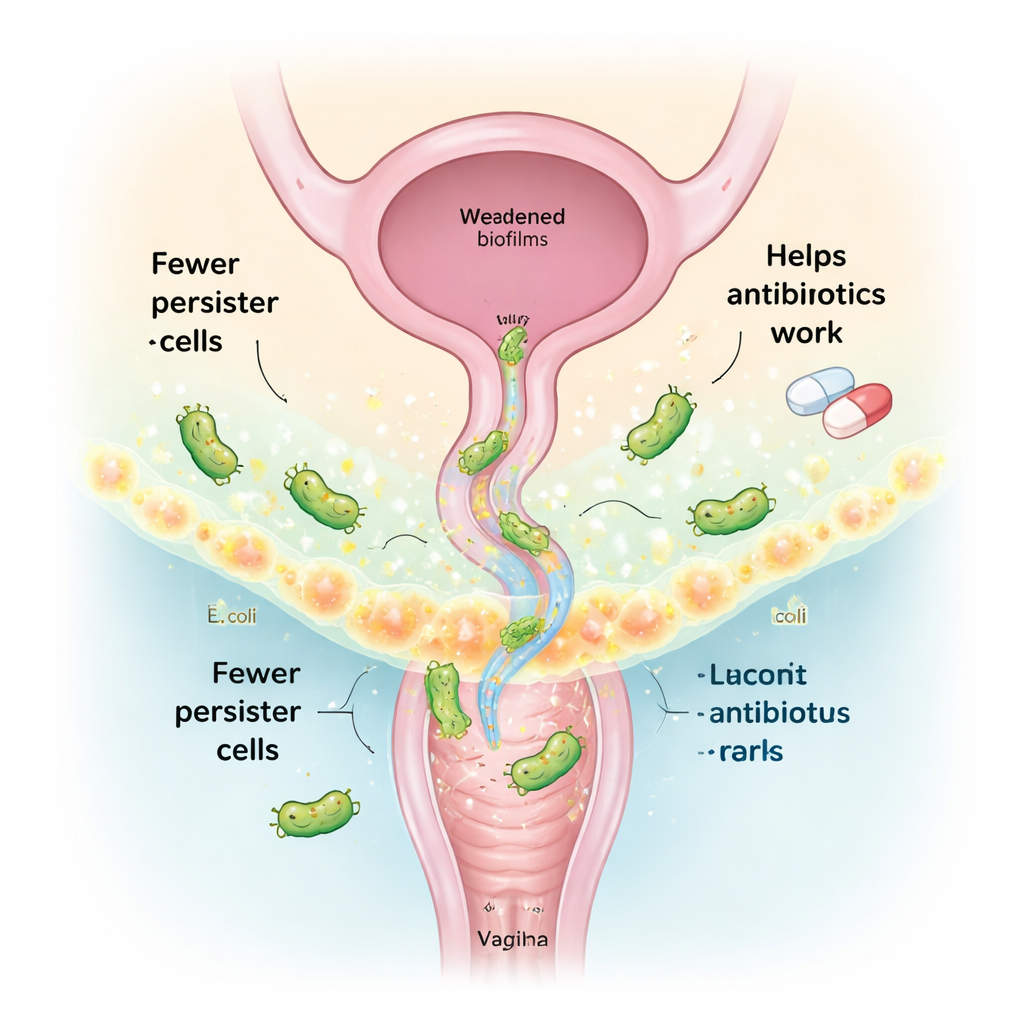
Transformer des bactéries vaginales amies en traitement
Un vagin sain est généralement dominé par des espèces de Lactobacillus, qui contribuent à contrôler les microbes nuisibles. Plutôt que d’utiliser des bactéries vivantes « probiotiques », cette étude s’est concentrée sur leur surnageant cellulaire—essentiellement le mélange de molécules qu’elles sécrètent, appelées postbiotiques. À partir de souches de Lactobacillus vaginales prélevées chez des femmes en bonne santé, l’équipe a séparé et analysé ces composés sécrétés. Deux métabolites clés, l’anhydride itaconique et le (−)-terpinen-4-ol, se sont distingués par leur capacité à agir en synergie et à réduire fortement le nombre de cellules persister d’E. coli lorsqu’ils sont combinés aux antibiotiques. Un troisième composé, la tryptamine, déjà montré comme capable de dégrader la matrice visqueuse du biofilm bactérien, a été ajouté pour renforcer l’action antibiofilm.
Comment le nouveau mélange affaiblit les bactéries difficiles à tuer
Les scientifiques ont constaté que ces molécules dérivées de Lactobacillus attaquent les persisters d’E. coli sur plusieurs fronts simultanément. Premièrement, elles augmentent la production d’espèces réactives de l’oxygène—formes d’oxygène chimiquement réactives qui endommagent les composants bactériens—rendant les antibiotiques beaucoup plus létaux pour les cellules dormantes. Lorsque des antioxydants ont été ajoutés, cet effet létal a diminué, soulignant le rôle du stress oxydatif. Deuxièmement, les composés rendent la membrane externe bactérienne plus « perméable », comme le montrent des colorants fluorescents qui pénètrent plus facilement dans les cellules après traitement. Troisièmement, ils inhibent les « pompes d’efflux » cellulaires, ces minuscules machines qui expulsent normalement les antibiotiques hors de la cellule. Avec les pompes bloquées, davantage de médicament reste à l’intérieur des bactéries, et moins de persisters survivent. Ensemble, ces changements ont réduit des biofilms d’E. coli préformés jusqu’à dix ordres de grandeur dans des tests en laboratoire, sans nuire aux cellules immunitaires de mammifères aux doses testées.
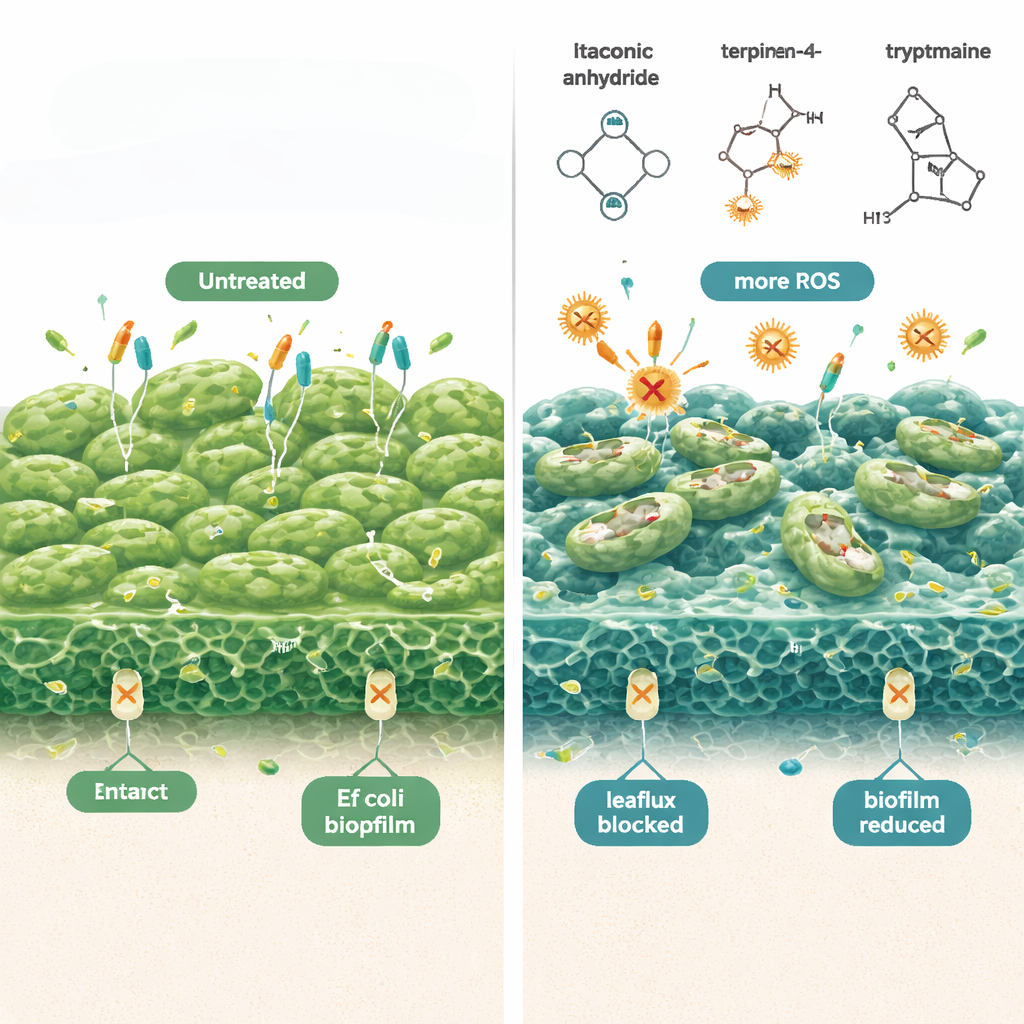
Du banc de laboratoire à un lavage vaginal pratique
Pour transformer ces résultats en un produit utilisable au quotidien, l’équipe a conçu un lavage vaginal personnalisé utilisant une base gélifiée thermosensible appelée poloxamère 407. À température ambiante, il se comporte comme un fluide pour une application facile, puis il épaissit doucement à la température corporelle afin d’améliorer le contact avec les parois vaginales. Le gel contient une combinaison définie et sûre d’anhydride itaconique, de (−)-terpinen-4-ol et de tryptamine. En plaque, cette formulation a fonctionné sur une plage de pH similaire aux conditions vaginales, supprimant fortement la formation de biofilm d’E. coli et réduisant d’environ neuf ordres de grandeur le nombre de bactéries vivantes. Elle est restée stable et biologiquement active pendant au moins trois mois en stockage froid et a également montré une activité large contre d’autres bactéries problématiques telles que Klebsiella, MRSA et Pseudomonas.
Évaluer la sécurité et la protection chez la souris
Ensuite, les chercheurs ont évalué le lavage dans un modèle murin d’infection vaginale par E. coli. Des souris ont été inoculées avec des E. coli marqués fluorescents (GFP) puis traitées soit avec le nouveau lavage aux métabolites, soit avec un lavage probiotique contenant des Lactobacillus vivants, soit avec un lavage vaginal commercial, soit avec la base placebo. Les animaux recevant le lavage métabolite personnalisé ont présenté beaucoup moins d’inflammation vaginale, ont maintenu leur poids corporel et ont eu des charges bactériennes nettement plus faibles dans les sécrétions vaginales par rapport aux autres groupes. Plus remarquable encore, les souris traitées n’avaient pas d’E. coli détectable dans l’urine, la vessie, les reins ou le tissu vaginal et ont conservé une fonction rénale normale, indiquant que la formulation a non seulement réduit l’infection locale mais a aussi empêché la propagation vers le haut des voies urinaires.
Ce que cela pourrait signifier pour les personnes souffrant d’IU récurrentes
L’étude conclut qu’un lavage vaginal composé de métabolites précis produits par des espèces de Lactobacillus naturellement protectrices peut affaiblir E. coli responsables d’IU de multiples façons : en réduisant les populations de persisters, en perturbant les biofilms et en rendant les antibiotiques standards plus efficaces. Comme cette approche repose sur des molécules non vivantes plutôt que sur des bactéries vivantes ou de longues prises de médicaments systémiques, elle pourrait être plus sûre, plus stable et plus facile à réglementer. Bien que des essais cliniques chez l’humain soient encore nécessaires, ce lavage à base de métabolites ouvre la voie vers un avenir où les IU récurrentes sont prévenues non seulement par des antibiotiques plus puissants, mais en renforçant intelligemment les défenses microbiennes naturelles du corps à la source.
Citation: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Mots-clés: infection urinaire, microbiome vaginal, postbiotiques de Lactobacillus, tolérance aux antibiotiques, biofilms bactériens