Clear Sky Science · fr
Modèles d’organoïdes cérébraux de la maladie liée à SZT2 révèlent une surproduction de cellules gliales radiales externes via l’activation de mTORC1
Quand la croissance cérébrale s’emballe
Pourquoi certains enfants développent-ils une tête anormalement grande, des crises d’épilepsie et de lourds retards du développement ? Cette étude aborde la question en explorant une maladie génétique rare liée au gène SZT2. À l’aide de « mini‑cerveaux » cultivés en laboratoire à partir de cellules souches, les chercheurs montrent comment un interrupteur défectueux du contrôle de la croissance peut conduire certaines cellules souches cérébrales à se surproduire, ce qui pourrait expliquer la surcroissance cérébrale et les perturbations du câblage observées chez les enfants touchés.
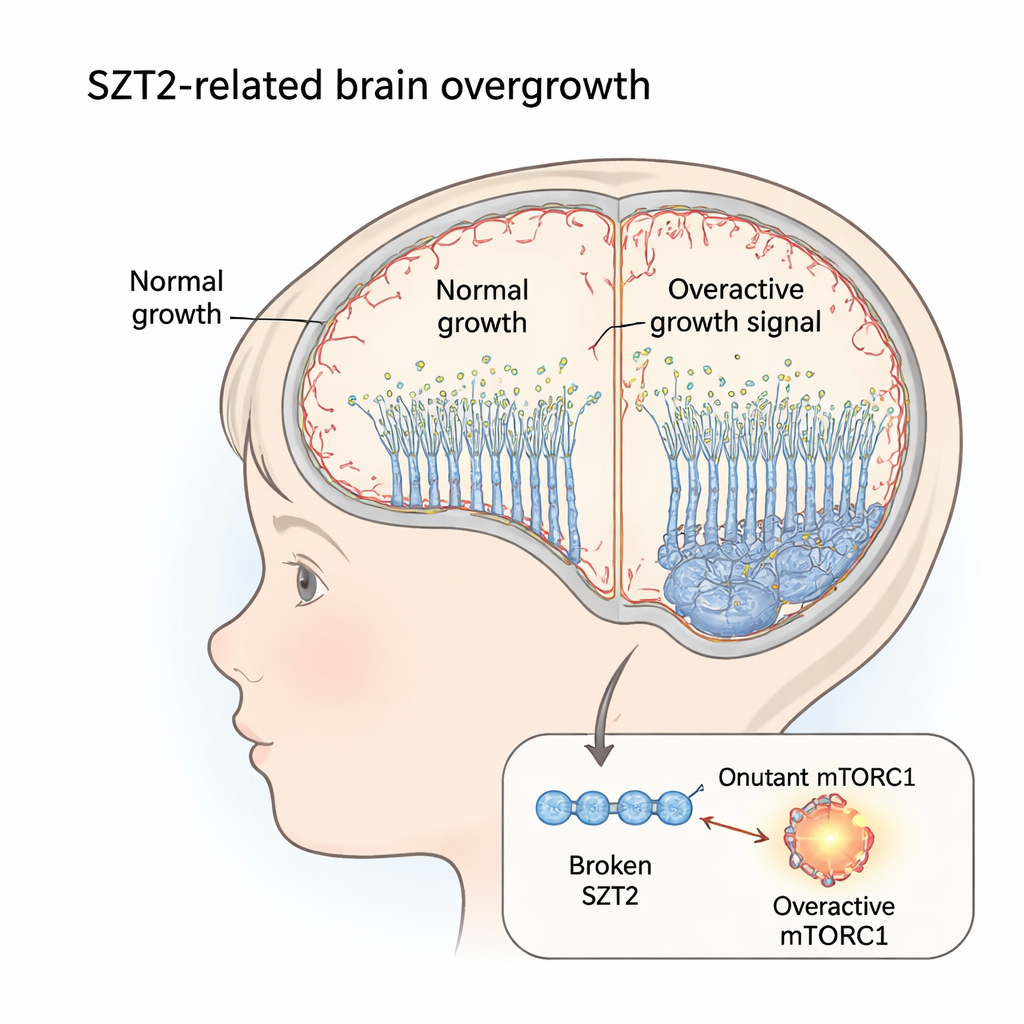
Un frein de croissance cassé dans le cerveau
Le gène SZT2 aide normalement à maintenir sous contrôle une voie de croissance puissante, connue sous le nom de mTORC1. Lorsque les deux copies de SZT2 sont altérées, les enfants peuvent développer de l’épilepsie, une déficience intellectuelle et une macrocéphalie — une tête anormalement volumineuse. Des travaux antérieurs avaient montré que mTORC1 restait « activé » dans les cellules de ces patients. Mais il n’était pas clair comment cela se manifeste pendant le développement cérébral humain précoce, période où se définissent la structure de base et la taille du cortex.
Construire des mini‑cerveaux pour modéliser la maladie
Pour étudier cela directement dans du tissu humain, l’équipe a utilisé des cellules souches pluripotentes induites, capables de se différencier en presque tous les types cellulaires. Ils ont modifié le gène SZT2 dans ces cellules avec CRISPR/Cas9, créant une version mutante dépourvue d’un petit mais crucial segment de la protéine. Ces cellules éditées et des cellules témoins non éditées ont ensuite été cultivées en organoïdes cérébraux tridimensionnels — des structures sphériques qui reproduisent des étapes clés du développement cérébral précoce, y compris la formation de zones en couches et la production neuronale. Les organoïdes des deux groupes ont évolué de façon globalement similaire et affichaient la même identité de base que le cerveau antérieur humain en développement.
Des cellules souches en excès dans la zone de croissance cérébrale
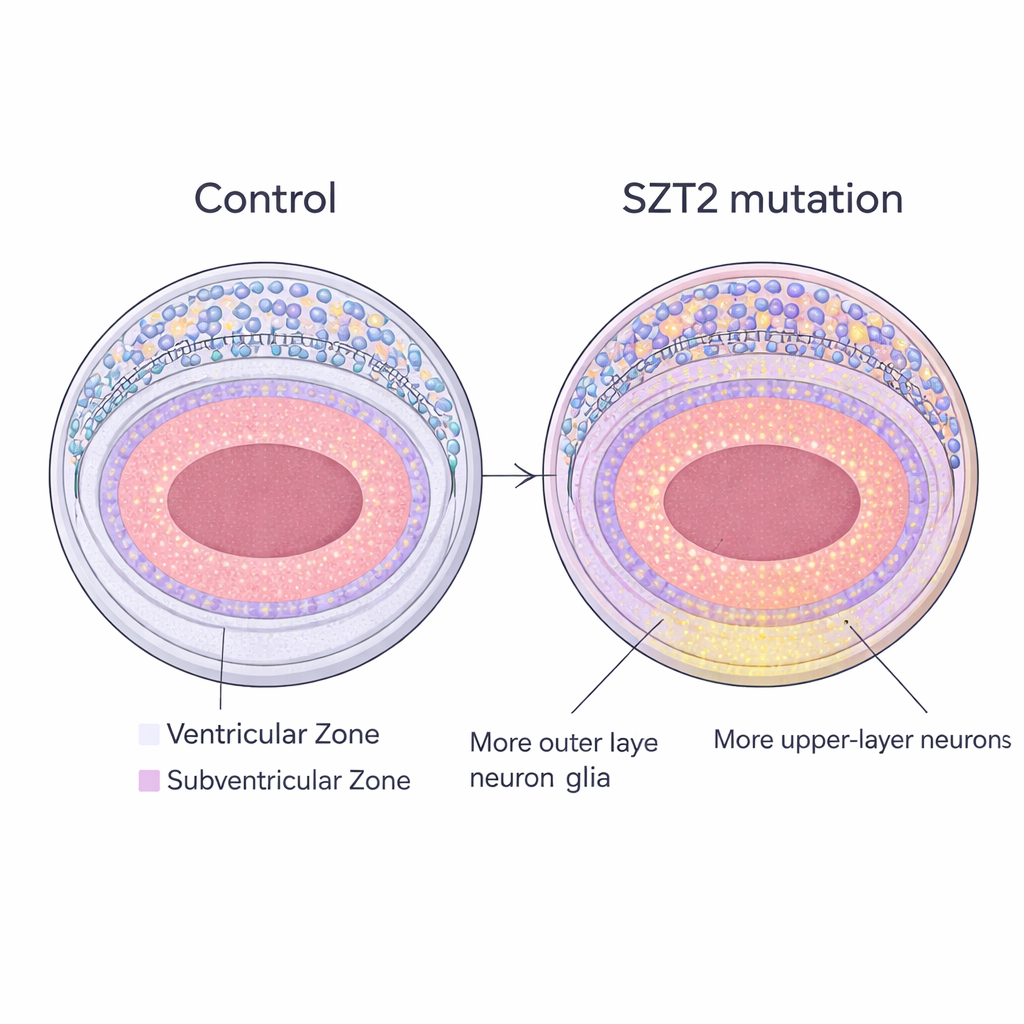
À l’intérieur de chaque mini‑cerveau, les chercheurs se sont concentrés sur deux régions clés : la zone ventriculaire interne, riche en cellules souches tapissant une cavité remplie de liquide, et la zone sous‑ventriculaire externe (SVZ), où se trouvent un type particulier de cellules souches appelées glies radiales externes. Ces glies radiales externes sont particulièrement abondantes chez l’humain et seraient à l’origine de l’expansion et du plissement de notre grand cerveau. Dans les organoïdes mutants pour SZT2, la SVZ était relativement élargie comparée à la zone interne, et elle contenait significativement plus de glies radiales externes que les témoins. Fait important, un autre type de cellules progénitrices dans la même région n’augmentait pas, ce qui suggère une amplification spécifique de cette population de cellules souches propre à l’humain.
D’un excès de cellules souches à un excès de neurones
L’équipe a ensuite examiné la couche ressemblant à la plaque corticale où les neurones prennent place. Là, ils ont compté deux types majeurs de neurones : les neurones des couches profondes et les neurones des couches supérieures, produits plus tard et essentiels aux communications longue distance entre régions cérébrales. Dans les organoïdes mutants SZT2, le nombre de neurones des couches supérieures était clairement augmenté, tandis que les neurones des couches profondes restaient à peu près inchangés. Ce schéma concorde avec les modèles actuels selon lesquels les glies radiales externes donnent principalement naissance aux neurones des couches supérieures. Fait intéressant, les chercheurs n’ont pas observé une augmentation générale des cellules en division, ce qui suggère que la modification provient davantage des choix de destinée et de la progression des cellules souches dans le développement que d’une simple accélération de la division.
Un signal hyperactif potentiellement traitable
Pour relier ces changements structurels à la voie de contrôle de la croissance, les scientifiques ont mesuré un marqueur de l’activité de mTORC1. Ils ont trouvé une signalisation mTORC1 renforcée non seulement dans la SVZ, où résident les glies radiales externes, mais aussi dans la zone interne et la couche externe riche en neurones des organoïdes mutants SZT2. Cela soutient l’idée que SZT2 agit comme un frein sur mTORC1 pendant le développement cérébral précoce ; lorsque ce frein défaillit, les glies radiales externes s’étendent, plus de neurones des couches supérieures sont produits et le cortex peut devenir anormalement volumineux et mal câblé. Les auteurs notent que cette même voie peut être atténuée par des médicaments existants bloquant mTOR, soulevant la possibilité — à tester — que des traitements administrés au bon moment pourraient un jour aider à gérer les troubles liés à SZT2.
Ce que cela signifie pour les patients et les familles
En termes simples, cette étude suggère qu’un gène SZT2 défectueux laisse un signal de croissance clé s’emballer dans le cerveau en développement. Ce signal surchauffé semble pousser un réservoir spécifique de cellules souches humaines à surproduire, conduisant à un cortex surdimensionné et potentiellement mal connecté qui pourrait sous‑tendre une grosse tête, des anomalies du corps calleux et des crises. Bien que le travail ait été réalisé dans des mini‑cerveaux cultivés en laboratoire à partir d’une seule lignée cellulaire et ne puisse pas encore prédire les résultats pour des enfants individuels, il fournit la première preuve directe sur modèle humain liant le dysfonctionnement de SZT2 à une surcroissance cérébrale précoce. Il oriente également vers les médicaments bloquant mTOR comme piste logique à explorer pour de futurs traitements.
Citation: Sato, E., Nakamura, Y., Fujimoto, M. et al. Brain organoid models of SZT2-related disease reveal an overproduction of outer radial glial cells through mTORC1 activation. Sci Rep 16, 5193 (2026). https://doi.org/10.1038/s41598-026-35733-w
Mots-clés: organoïdes cérébraux, mTORC1, SZT2, macrocéphalie, glie radiale externe