Clear Sky Science · fr
Impact pronostique des niches spatiales dans le cancer de la prostate
Pourquoi les « quartiers » de la tumeur comptent
Le cancer de la prostate est fréquent, mais toutes les tumeurs ne se comportent pas de la même manière. Certaines évoluent lentement, tandis que d’autres progressent rapidement et mettent la vie des patients en péril. Les médecins s’appuient aujourd’hui sur des marqueurs comme le taux de PSA et le grade histologique pour estimer quelles tumeurs sont dangereuses. Cette étude pose une question nouvelle : l’endroit précis où les cellules cancéreuses se trouvent dans la tumeur — la bordure active versus le noyau plus profond — peut-il aider à prédire l’évolution chez un patient ?
Voir la tumeur comme un petit écosystème
Les recherches récentes montrent qu’une tumeur n’est pas une masse uniforme de cellules identiques. Elle ressemble plutôt à un petit écosystème avec des « quartiers » distincts, ou niches spatiales. Dans le cancer de la prostate, le cœur interne de la tumeur et le bord externe où le cancer côtoie le tissu sain peuvent abriter des mélanges différents de cellules tumorales, de cellules immunitaires et de structures de soutien. Les auteurs ont utilisé une technologie nommée profilage spatial numérique, qui permet de mesurer des dizaines de protéines directement sur des coupes minces de tissu tumoral conservé, tout en conservant l’information sur l’emplacement exact de chaque mesure dans la tumeur.
Mesurer les protéines au centre et en périphérie de la tumeur
L’équipe a analysé des échantillons tumoraux provenant de 49 hommes atteints d’un cancer de la prostate à haut risque ayant subi une chirurgie. Pour chaque tumeur, ils ont sélectionné des régions au centre et à la périphérie et mesuré les niveaux de 46 protéines différentes liées aux cellules immunitaires, à la mort cellulaire et aux signaux de croissance. Cela a généré des dizaines de milliers de points de données. En examinant séparément le centre et la périphérie de la tumeur, ils ont confirmé que ces zones se comportent différemment : de nombreuses protéines, en particulier celles liées à l’activité immunitaire, étaient plus abondantes à la bordure externe de la tumeur, tandis que certains régulateurs de la mort cellulaire étaient plus élevés au centre.
Quand les vues séparées sont insuffisantes
Les chercheurs ont ensuite cherché à savoir si les profils protéiques du seul centre ou de la seule périphérie pouvaient prédire la durée pendant laquelle les patients resteraient exempts de progression après la chirurgie. En regroupant statistiquement les patients selon les profils protéiques de chaque compartiment pris isolément, ils ont identifié deux grands clusters pour le centre et deux pour la périphérie. Cependant, aucun de ces ensembles de clusters ne correspondait à l’évolution réelle des patients au fil du temps, et ils ne corrélaient pas clairement avec des facteurs de risque classiques tels que le score de Gleason ou des mutations connues comme BRCA1/2 et TP53. En d’autres termes, l’observation de chaque « quartier » isolément n’a pas fourni de nouveau marqueur pronostique utile.
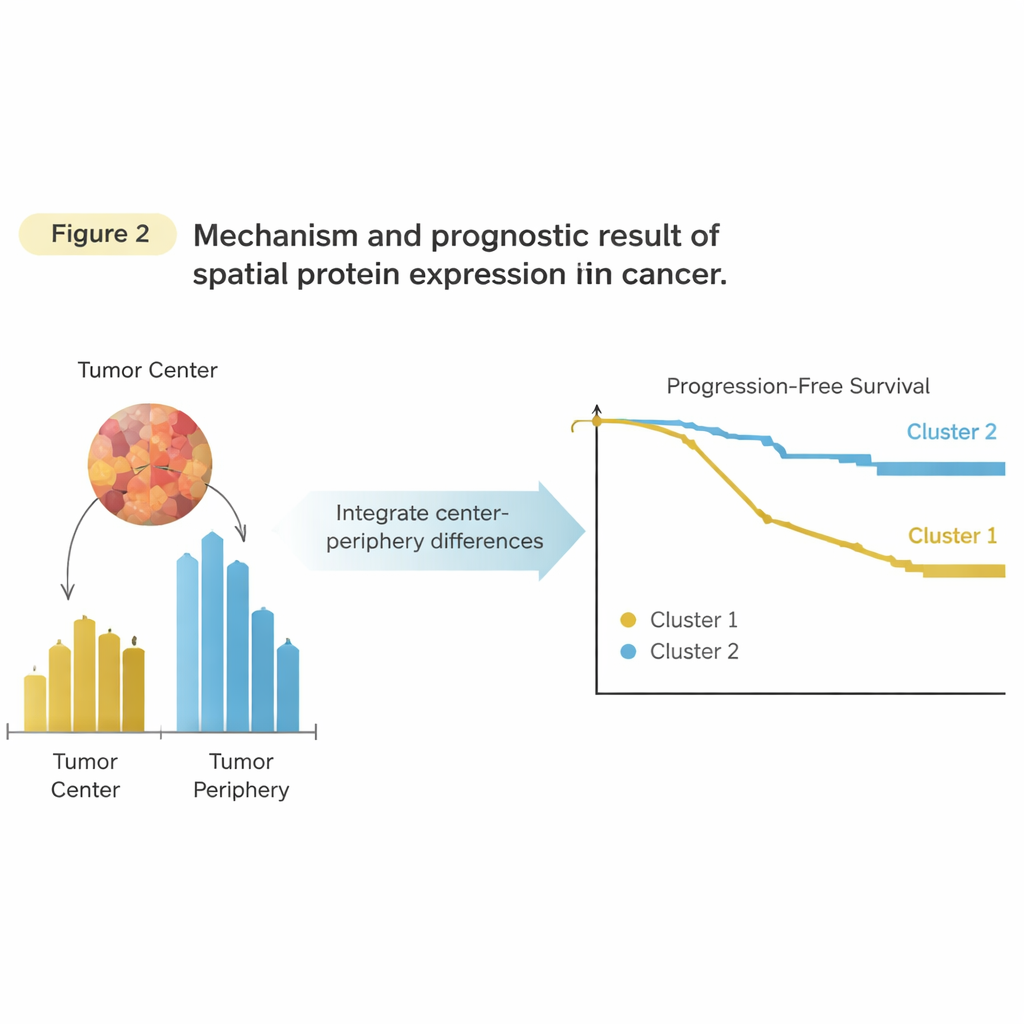
Combiner les deux quartiers révèle un signal
La démarche clé a été de combiner les informations du centre et de la périphérie plutôt que de les traiter séparément. Pour chaque protéine et chaque patient, les chercheurs ont calculé dans quelle mesure cette protéine était plus (ou moins) exprimée en périphérie par rapport au centre. Cela a produit une « valeur d’équilibre » unique par protéine qui conservait l’information spatiale sur son enrichissement dans la tumeur. En regroupant les patients sur la base de ces équilibres spatiaux, deux nouveaux clusters sont apparus. Cette fois, les clusters importaient : un groupe présentait un délai beaucoup plus court avant progression du cancer que l’autre. Fait important, la puissance de cette approche ne provenait pas d’une protéine isolée mais du motif spatial global à travers de nombreuses protéines, en particulier celles liées aux cellules immunitaires et au remodelage tissulaire à la bordure tumorale.
Ce que cela pourrait signifier pour les patients
Pour les personnes confrontées au cancer de la prostate, ces résultats suggèrent que l’emplacement d’expression des protéines dans la tumeur — pas seulement leur quantité totale — peut contenir des indices précieux sur le comportement futur de la maladie. Bien que l’étude soit limitée en taille et repose sur une technologie spécialisée et coûteuse, elle apporte une preuve de concept que des mesures protéiques tenant compte de la spatialisation peuvent révéler des informations pronostiques que les tests standard manquent. Avec des validations ultérieures et des méthodes de laboratoire plus simples, ce type de biomarqueur spatial pourrait un jour aider les médecins à mieux distinguer quels cancers de la prostate à haut risque sont susceptibles de progresser rapidement et lesquels pourraient suivre une trajectoire plus contrôlable, guidant ainsi des décisions de traitement plus personnalisées.
Citation: Schneider, F., Böning, S.H., Antunes, B.C. et al. Prognostic impact of spatial niches in prostate cancer. Sci Rep 16, 2598 (2026). https://doi.org/10.1038/s41598-026-35720-1
Mots-clés: cancer de la prostate, profilage spatial, microenvironnement tumoral, biomarqueur pronostique, hétérogénéité intratumorale