Clear Sky Science · fr
Le Vpr du VIH induit la déméthylation du promoteur antisens de SNCA, conduisant à un déclin neurocognitif
Pourquoi le VIH peut encore affecter le cerveau
Les personnes vivant avec le VIH bénéficient aujourd’hui d’une espérance de vie et d’un état de santé améliorés grâce aux antirétroviraux modernes. Pourtant, nombre d’entre elles continuent de présenter des troubles de la mémoire, de la concentration et des mouvements, même lorsque la charge virale sanguine est bien contrôlée. Cette étude examine les causes possibles en se focalisant sur une petite protéine virale, appelée Vpr, et sur une protéine cérébrale, l’alpha‑synucléine, qui joue également un rôle central dans la maladie de Parkinson. Comprendre comment ces deux molécules interagissent pourrait expliquer pourquoi le VIH accélère le vieillissement cérébral et suggérer de nouvelles façons de protéger le cerveau.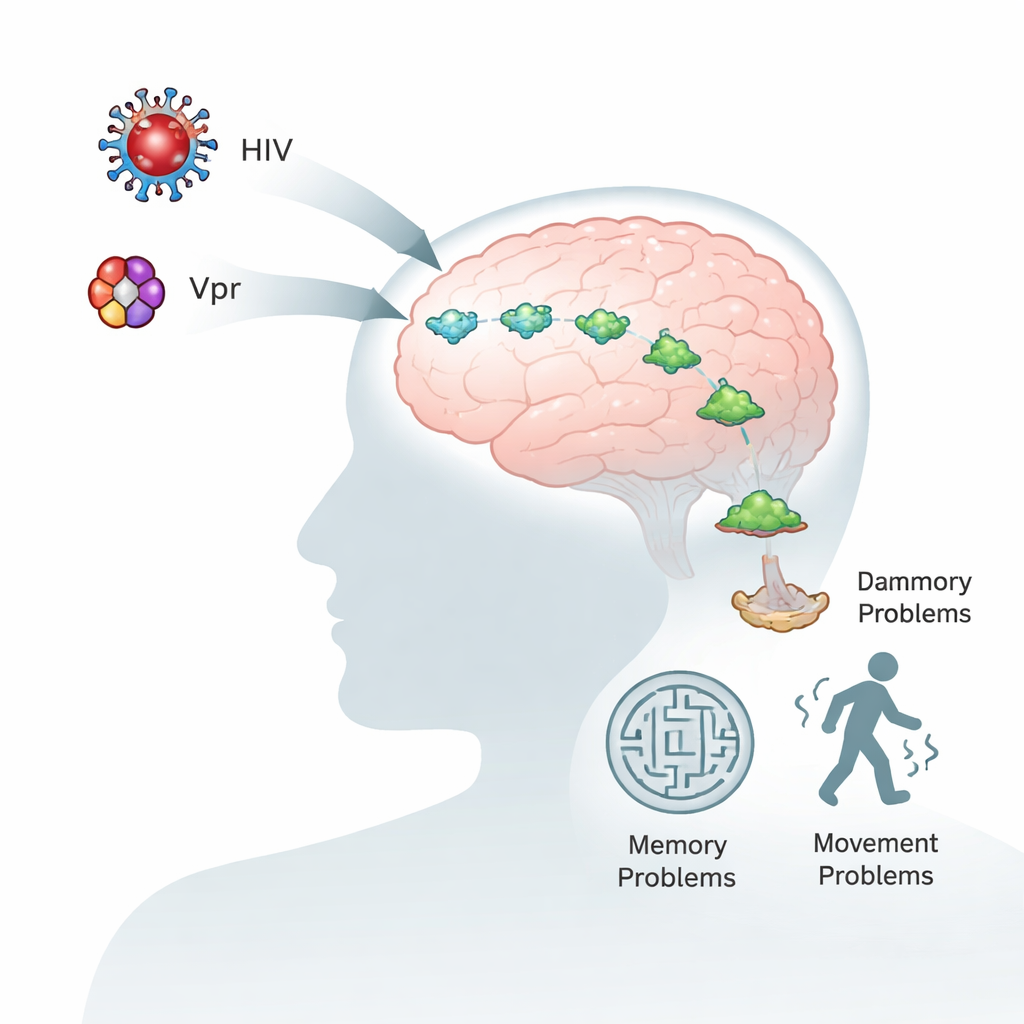
Une protéine cérébrale au carrefour du VIH et de Parkinson
L’alpha‑synucléine est une protéine qui aide les neurones à communiquer, en particulier dans les régions cérébrales qui contrôlent le mouvement et la mémoire. Lorsqu’un excès d’alpha‑synucléine s’accumule, elle forme des agrégats qui endommagent les synapses, sollicitent les mitochondries productrices d’énergie et alimentent l’inflammation. Ces agrégats sont une caractéristique de la maladie de Parkinson. Les auteurs montrent que l’alpha‑synucléine s’accumule aussi avec le vieillissement normal chez la souris, et que la protéine Vpr du VIH augmente encore davantage ses niveaux dans des cellules de type nerveux. Cela place l’alpha‑synucléine au carrefour entre les troubles cognitifs liés au VIH et les troubles moteurs classiques.
Comment une protéine virale réécrit la « ponctuation » cellulaire
Chaque cellule utilise des marques chimiques sur l’ADN — souvent décrites comme des signes de ponctuation moléculaire — pour activer ou réprimer des gènes. Dans ce travail, l’équipe s’est intéressée à un interrupteur de régulation peu connu situé à l’intérieur du gène de l’alpha‑synucléine, appelé promoteur antisens. Dans les cellules saines, cet interrupteur est fortement marqué par des groupes méthyle, ce qui le maintient relativement silencieux. Les chercheurs ont découvert que Vpr enlève ces marques à des sites spécifiques de cette région, un processus connu sous le nom de déméthylation. Une fois ces marques retirées, le promoteur antisens devient plus actif et stimule la production supplémentaire d’alpha‑synucléine, préparant le terrain à une agrégation nuisible.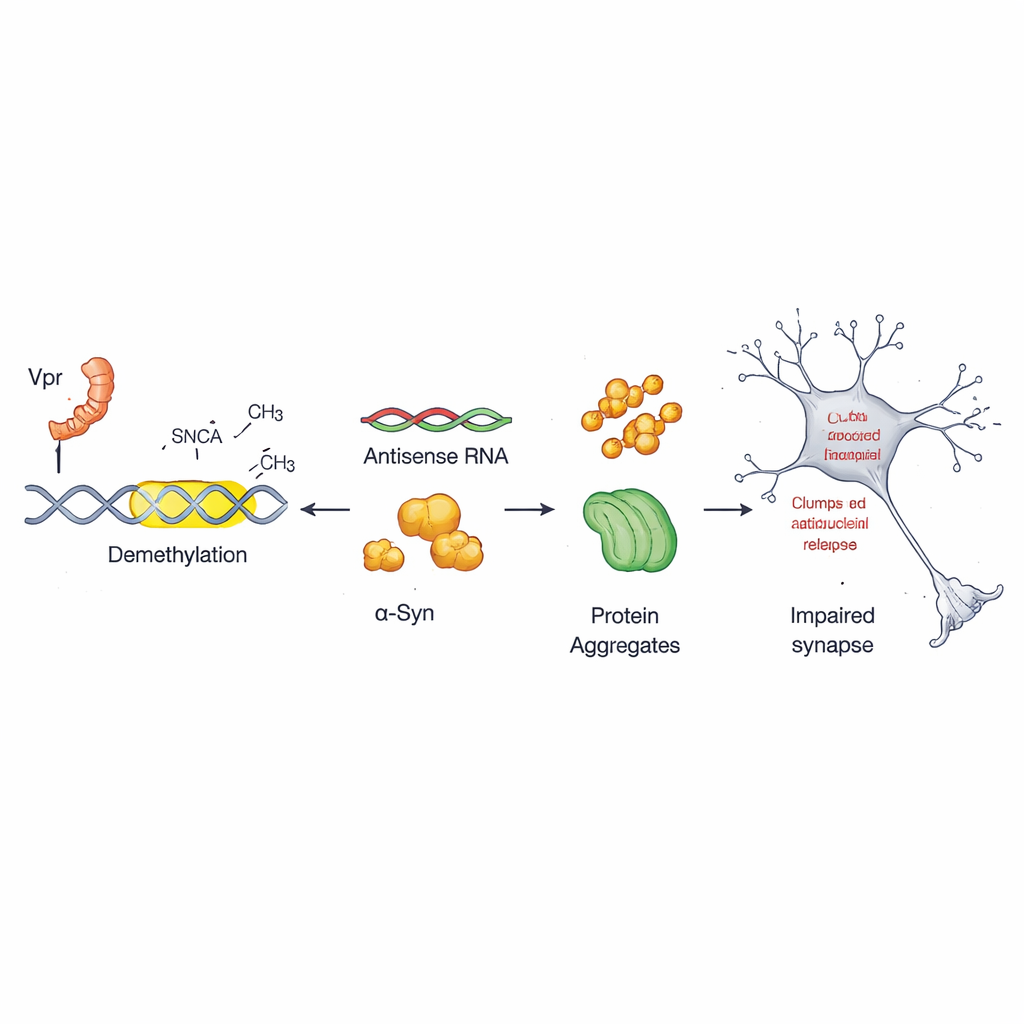
Des preuves issues de cellules, de souris et de cerveaux humains
En utilisant des cellules humaines cultivées de type nerveux et des neurones primaires de souris, les auteurs ont montré que l’ajout de Vpr augmente au fil du temps les niveaux d’ARN messager et de protéine d’alpha‑synucléine. Un médicament qui favorise globalement la déméthylation de l’ADN a reproduit certains de ces effets, soulignant le rôle du contrôle épigénétique. À l’inverse, un composé appelé DMOG, qui bloque les enzymes déméthylantes, a empêché Vpr d’activer pleinement le promoteur antisens. L’équipe s’est ensuite tournée vers des échantillons cérébraux humains provenant de personnes avec ou sans VIH. Les cerveaux de donneurs séropositifs — avant comme après traitement antirétroviral — présentaient moins de marques méthyle dans la même région d’ADN et des niveaux plus élevés d’alpha‑synucléine et de son transcrit antisens, en particulier chez les donneurs atteints de démence liée au VIH. Cela suggère que le virus laisse une cicatrice épigénétique durable dans le cerveau.
Des changements moléculaires aux troubles de la mémoire
Pour relier ces modifications moléculaires au comportement, les chercheurs ont examiné comment Vpr affecte les circuits cérébraux chez la souris. Lorsqu’ils ont appliqué Vpr à des coupes d’hippocampe de souris, une région essentielle pour la mémoire, la force synaptique de base entre les neurones n’était pas modifiée, mais la capacité à renforcer les connexions — un processus appelé potentialisation à long terme — était réduite. Chez des souris vivantes, des injections ciblées de Vpr dans l’hippocampe ont entraîné une performance moindre à une tâche de mémoire spatiale où les animaux doivent se souvenir de l’emplacement d’objets. Ensemble, ces expériences suggèrent que les modifications de l’alpha‑synucléine induites par Vpr ne sont pas de simples curiosités biochimiques ; elles se traduisent par un affaiblissement des synapses et des déficits mnésiques mesurables.
Ce que cela signifie pour les personnes vivant avec le VIH
Cette étude propose une chaîne d’événements plausible : le VIH libère Vpr, Vpr reprogramme un interrupteur clé de l’ADN contrôlant l’alpha‑synucléine, la protéine s’accumule et s’agrège, et les neurones perdent progressivement leur capacité à communiquer et à soutenir la mémoire. Comme des problèmes similaires d’alpha‑synucléine sous‑tendent la maladie de Parkinson, ce travail suggère que le VIH et les maladies neurodégénératives classiques partagent des mécanismes chevauchants. Surtout, les résultats mettent en lumière des stratégies potentielles — par exemple des médicaments qui stabilisent la méthylation de l’ADN au niveau du promoteur antisens ou qui limitent l’accumulation d’alpha‑synucléine — pour ralentir ou prévenir le déclin cognitif et les troubles moteurs liés au VIH.
Citation: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Mots-clés: troubles neurocognitifs associés au VIH, alpha-synucléine, épigénétique, méthylation de l’ADN, symptômes de type Parkinson