Clear Sky Science · fr
Refonte rationnelle d'une ADNzyme G-quadruplex à haute activité par modification des bases de contour et des boucles
Petites machines à ADN au grand potentiel
Imaginez remplacer des enzymes protéiques fragiles par de courts brins d'ADN capables de résister à la chaleur, aux produits chimiques et aux manipulations brusques, tout en accomplissant des réactions chimiques utiles. Cette étude explore précisément cette idée. Les chercheurs modifient des structures d'ADN particulières pour qu'elles se comportent comme de minuscules enzymes nettoyants, capables d'utiliser le peroxyde d'hydrogène pour générer un signal fort. Ces « machines » en ADN, plus robustes et plus rapides, pourraient rendre les tests médicaux, les capteurs environnementaux et les diagnostics portables futurs moins coûteux, plus fiables et plus faciles à utiliser hors du laboratoire.
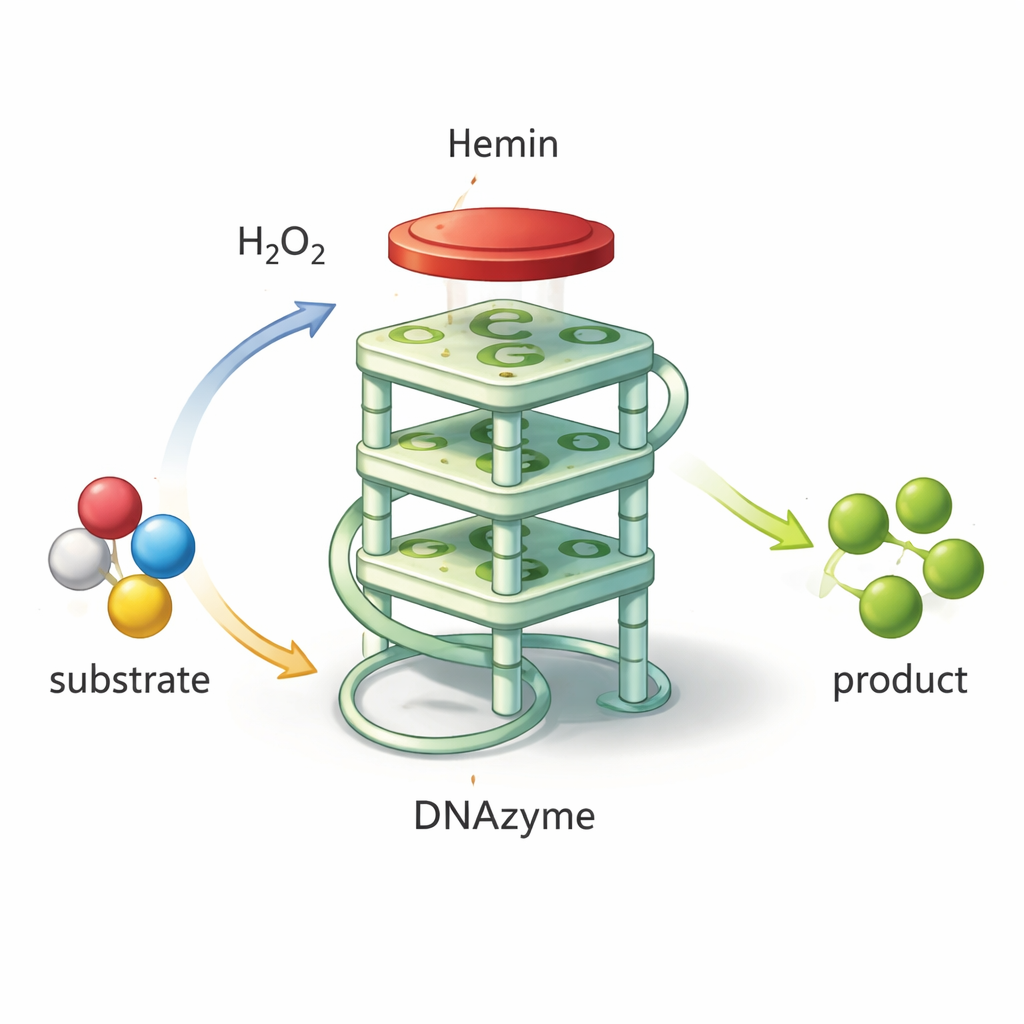
Transformer l'ADN en un petit outil chimique
Toute l'ADN n'est pas simplement un support passif d'information génétique. Certaines courtes séquences peuvent se replier en formes inhabituelles qui captent des molécules spécifiques ou accélèrent même des réactions chimiques. L'une de ces formes est le G‑quadruplex, dans lequel de l'ADN riche en guanines se replie en un empilement compact en quatre couches. Lorsqu'une petite molécule contenant du fer, appelée hémin, se pose sur cet empilement, l'ensemble agit comme une « ADNzyme » : un catalyseur à base d'ADN qui imite les peroxydases naturelles. Il peut utiliser le peroxyde d'hydrogène pour oxyder un colorant, produisant un signal vert intense facile à mesurer. Comme ces ADNzymes sont peu coûteux à produire, très stables et aisés à reconfigurer, ils constituent des éléments prometteurs pour des biosenseurs détectant pathogènes, toxines ou marqueurs de maladie.
Pourquoi les ADNzymes actuels doivent être améliorés
Malgré leurs atouts, la plupart des ADNzymes restent plus lentes et moins efficaces que les enzymes protéiques présentes dans la nature. Les biosenseurs existants doivent souvent amplifier la cible par des techniques comme la PCR ou ajouter des composants auxiliaires, ce qui augmente le coût et la complexité. Les tentatives précédentes pour améliorer les ADNzymes ont inclus l'association de deux unités d'ADN, la fixation permanente de l'hémin ou l'entourage du site réactif par des groupes chimiques supplémentaires. Ces astuces aident parfois, mais elles peuvent aussi introduire du volume gênant ou exiger une chimie sophistiquée. Une question clé est de savoir comment de simples modifications des bases d'ADN avoisinantes — en particulier celles qui ne rompent pas la structure centrale du G‑quadruplex — pourraient régler l'activité de façon prévisible et « concevable ».
Refonte d'une ADNzyme à haute performance
L'équipe s'est intéressée à une ADNzyme particulièrement active connue sous le nom de B730, qui figure déjà parmi les meilleurs catalyseurs G‑quadruplex non modifiés. Ils ont systématiquement modifié l'ADN juste à l'extérieur de son cœur en ajoutant ou en repositionnant des bases courantes comme l'adénine, la thymine et la cytosine dans les régions de boucle et de queue. Une version reconfigurée, appelée B730‑1.2, combinait des adénines ajoutées dans les boucles avec une courte paire thymine–cytosine à une extrémité du brin. Dans des conditions modérées de peroxyde d'hydrogène, cette variante a triplé la vitesse initiale de réaction et multiplié par environ quatre la quantité totale de produit coloré par rapport au B730 d'origine. Elle a également surpassé nettement deux autres ADNzymes bien connus, AS1411 et CatG4, lors de tests comparatifs.
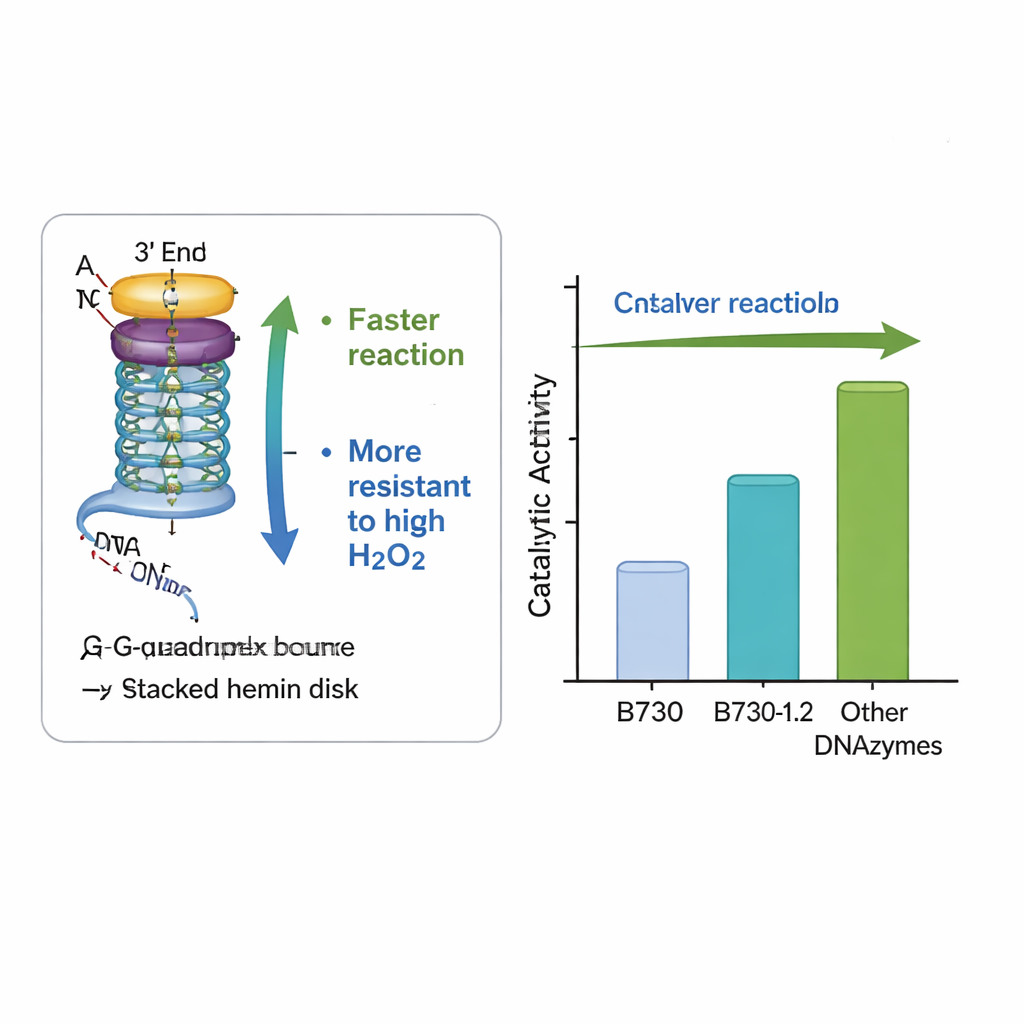
Conçue pour résister à des conditions difficiles
Un obstacle pratique important pour les peroxydases naturelles comme artificielles est que des niveaux élevés de peroxyde d'hydrogène — l'agent qui alimente la réaction — peuvent détruire l'enzyme et arrêter le processus. L'ADNzyme remaniée B730‑1.2 a montré une résilience remarquable : elle a maintenu et même accru son activité à des concentrations de peroxyde qui inactivent généralement des systèmes similaires. Des mesures d'absorption de lumière ont confirmé que l'ADN modifié favorisait la formation plus rapide de l'intermédiaire réactif clé — le fameux Compound I — sans perturber la conformation globale du G‑quadruplex. Autrement dit, des changements subtils des bases environnantes ont créé un environnement local plus favorable à la chimie, accélérant les étapes utiles tout en protégeant le centre catalytique de l'auto‑destruction.
Ce que cela signifie pour les capteurs de demain
Pour un non‑spécialiste, le message est simple : en ajustant soigneusement quelques « lettres » de part et d'autre d'une ADNzyme déjà performante, les auteurs ont produit une version qui fonctionne plus vite et résiste mieux à des conditions plus rudes. Leur stratégie de modifier les bases de contour et des boucles offre une recette simple et peu coûteuse pour fabriquer des catalyseurs à base d'ADN plus puissants sans recourir à des modifications chimiques complexes. De tels ADNzymes robustes et efficaces pourraient constituer le cœur de bandes-tests et d'appareils portables de nouvelle génération, transformant rapidement des signaux biologiques invisibles — comme des traces de virus ou de polluants — en changements de couleur faciles à lire.
Citation: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Mots-clés: ADNzyme G-quadruplex, mimétique de peroxydase, biosurveillance, ingénierie d'aptamères, catalyse du peroxyde d'hydrogène