Clear Sky Science · fr
Étude des liquides ioniques à base d’Acoramidis comme stabilisants potentiels de la transthyrétine via des calculs DFT, le docking moléculaire et des études ADMET
Pourquoi il est si difficile de développer un comprimé pour une maladie cardiaque rare
L’amylose à transthyrétine (ATTR) est une maladie grave dans laquelle une protéine sanguine s’accumule dans le cœur et les nerfs, les endommageant progressivement. Un nouveau médicament, l’Acoramidis, peut aider à stopper cette accumulation, mais un obstacle pratique subsiste : le médicament se dissout mal dans l’eau, ce qui complique son absorption par l’organisme lorsqu’il est pris sous forme de comprimé. Cette étude explore une manière ingénieuse de repenser l’Acoramidis en nouvelles formes de type sel, appelées liquides ioniques, susceptibles de rendre le médicament plus facile à administrer et plus efficace.
Transformer un médicament prometteur en forme buvable
Pour qu’un comprimé soit efficace, il doit d’abord se dissoudre dans les fluides aqueux de l’estomac et de l’intestin, puis traverser la paroi intestinale pour atteindre la circulation sanguine. L’Acoramidis est efficace pour stabiliser la protéine transthyrétine (TTR), ce qui aide à prévenir la formation d’amas protéiques nocifs associés à l’ATTR, mais il présente une faible solubilité et une mauvaise biodisponibilité orale. Les chercheurs ont cherché à résoudre ce problème en associant chimiquement l’Acoramidis à différents contre‑ions chargés, créant trois nouvelles versions de liquides ioniques (IL1, IL2 et IL3). Ces versions sont conçues pour se comporter davantage comme des sels fluides que comme des cristaux rigides, ce qui pourrait améliorer la dissolution et la distribution du médicament dans l’organisme. 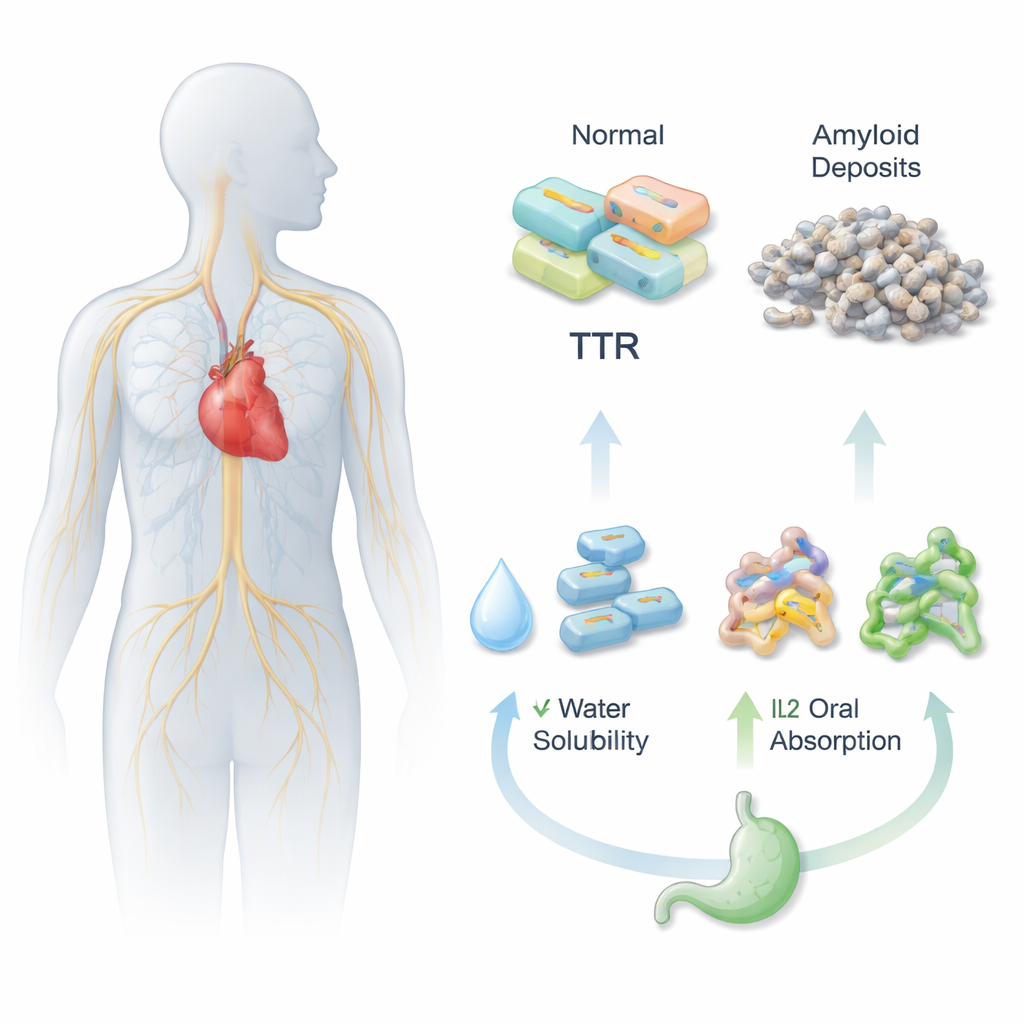
Examiner les nouvelles molécules par calcul
Plutôt que d’aller directement aux essais sur animaux ou humains, l’équipe a utilisé des méthodes informatiques avancées pour prédire le comportement de ces nouvelles formes. Des calculs de chimie quantique ont estimé la polarité de chaque molécule — un indicateur clé de la solubilité dans l’eau — et la facilité de polarisation électronique, liée à la manière dont elles pourraient interagir avec des protéines. IL1 se distingue par le moment dipolaire le plus élevé et la plus grande réactivité électronique, ce qui suggère une meilleure solubilité aqueuse et la capacité d’établir des contacts plus forts et plus flexibles avec ses cibles. Les calculs énergétiques indiquent également qu’IL1 est plus stable thermiquement que le médicament d’origine et les deux autres liquides ioniques, ce qui signifie qu’il serait moins susceptible de se décomposer avant d’atteindre sa cible.
Quelle force de liaison avec la cible
Ensuite, les chercheurs ont utilisé le docking moléculaire, un test virtuel de « serrure et clé », pour évaluer l’affinité de l’Acoramidis et de ses trois formes ioniques pour le canal de liaison de la protéine TTR. Les quatre composés se sont enfilés dans la région correcte de la TTR, mais IL1 a formé la liaison la plus solide, avec l’énergie de liaison la plus favorable et plusieurs contacts stabilisants — en particulier des liaisons hydrogène — avec des acides aminés clés de la protéine. Cette liaison plus forte suggère qu’IL1 pourrait être encore meilleur que la molécule parentale pour maintenir la TTR dans sa structure tétramérique sûre, aidant ainsi à prévenir la désagrégation et le mauvais repliement qui conduisent aux dépôts amyloïdes.
Le corps va‑t‑il absorber et éliminer ces nouvelles formes ?
Enfin, l’équipe a utilisé des outils pharmacologiques en ligne pour explorer la façon dont l’organisme pourrait traiter ces composés — leur solubilité, leur capacité à traverser la paroi intestinale, leur circulation dans le sang et leur élimination finale. Les trois liquides ioniques ont été prédits comme plus solubles dans l’eau que l’Acoramidis, IL3 présentant la plus grande solubilité brute. Les mesures de perméabilité intestinale et d’absorption orale globale se sont améliorées pour les trois liquides ioniques, IL1 et IL2 offrant le meilleur compromis entre pénétration intestinale et biodisponibilité prédite. La liaison aux protéines sanguines, les taux d’élimination et les demi‑vies ont également évolué de manière à suggérer que les formes en liquide ionique pourraient fournir une exposition plus fiable après administration orale, IL1 présentant de nouveau un profil particulièrement favorable. 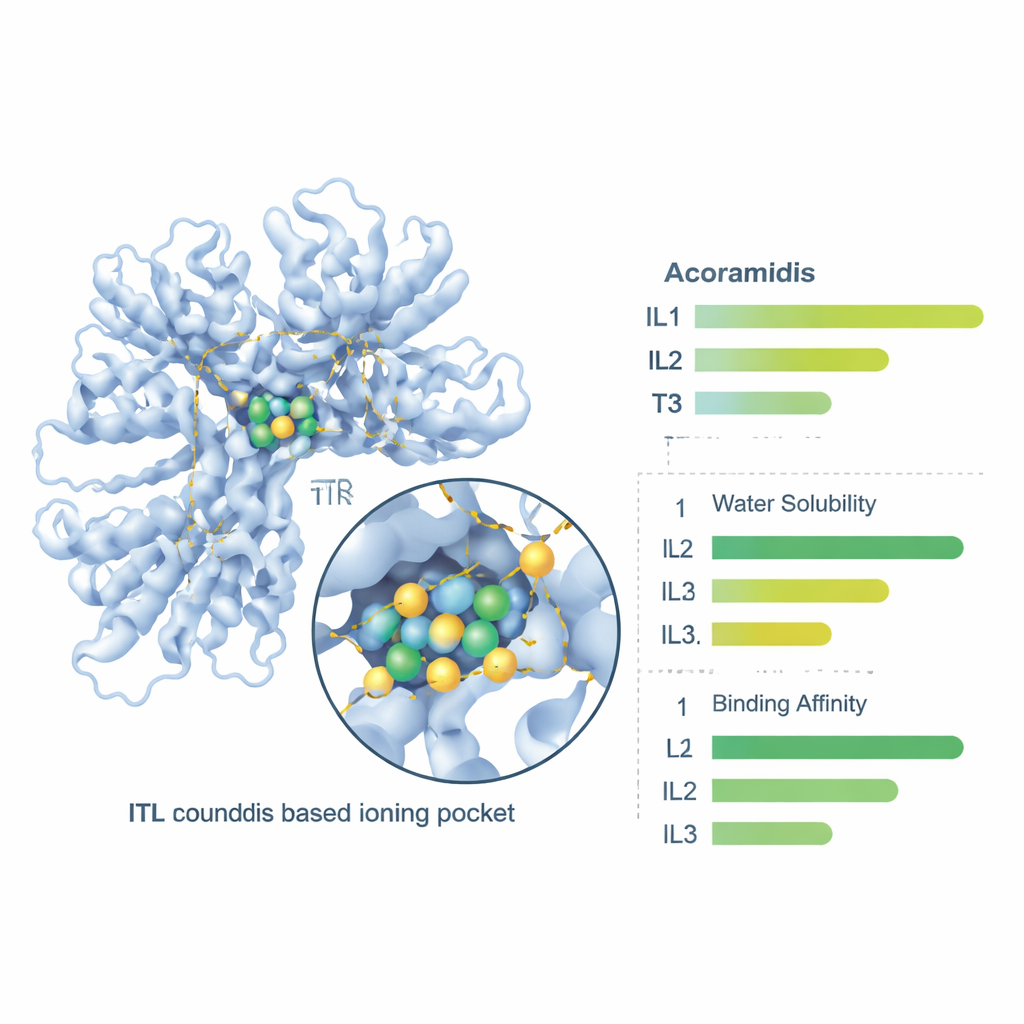
Ce que cela pourrait signifier pour les futurs traitements de l’ATTR
Pour un non‑spécialiste, le message principal est que l’Acoramidis apparaît déjà prometteur pour une maladie cardiaque et nerveuse rare mais grave, mais que sa faible solubilité limite son efficacité par voie orale. En transformant l’Acoramidis en liquides ioniques spécialement conçus, cette étude montre — entièrement par des tests informatiques — qu’il pourrait être possible de créer des versions qui se dissolvent mieux, se lient plus fortement à leur cible protéique et sont absorbées plus efficacement. Parmi les trois candidats, IL1 semble offrir le meilleur compromis en termes de stabilité, d’affinité de liaison, de solubilité et d’absorption orale prédite, en faisant un candidat solide pour des développements expérimentaux et cliniques futurs visant à proposer des traitements plus efficaces et faciles à prendre pour l’ATTR.
Citation: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Mots-clés: amylose à transthyrétine, Acoramidis, liquides ioniques, mauvais repliement des protéines, administration orale de médicaments