Clear Sky Science · fr
Conception in silico d’un vaccin multi-épitope ciblant DENV-1 et DENV-3
Pourquoi les vaccins contre la dengue restent essentiels
La dengue n’est plus une maladie tropicale rare ; elle menace désormais des milliards de personnes dans plus de 100 pays et submerge régulièrement les hôpitaux dans certaines régions d’Asie, d’Amérique latine et ailleurs. Pourtant, même avec deux vaccins homologués disponibles, la protection reste inégale, en particulier chez les personnes n’ayant jamais eu la dengue et dans les régions où plusieurs sérotypes viraux circulent simultanément. Cette étude pose une question d’actualité : la conception assistée par ordinateur peut-elle nous aider à élaborer un vaccin plus sûr et plus précis, visant spécifiquement les co-infections dangereuses associant deux sérotypes de dengue qui frappent souvent ensemble ?
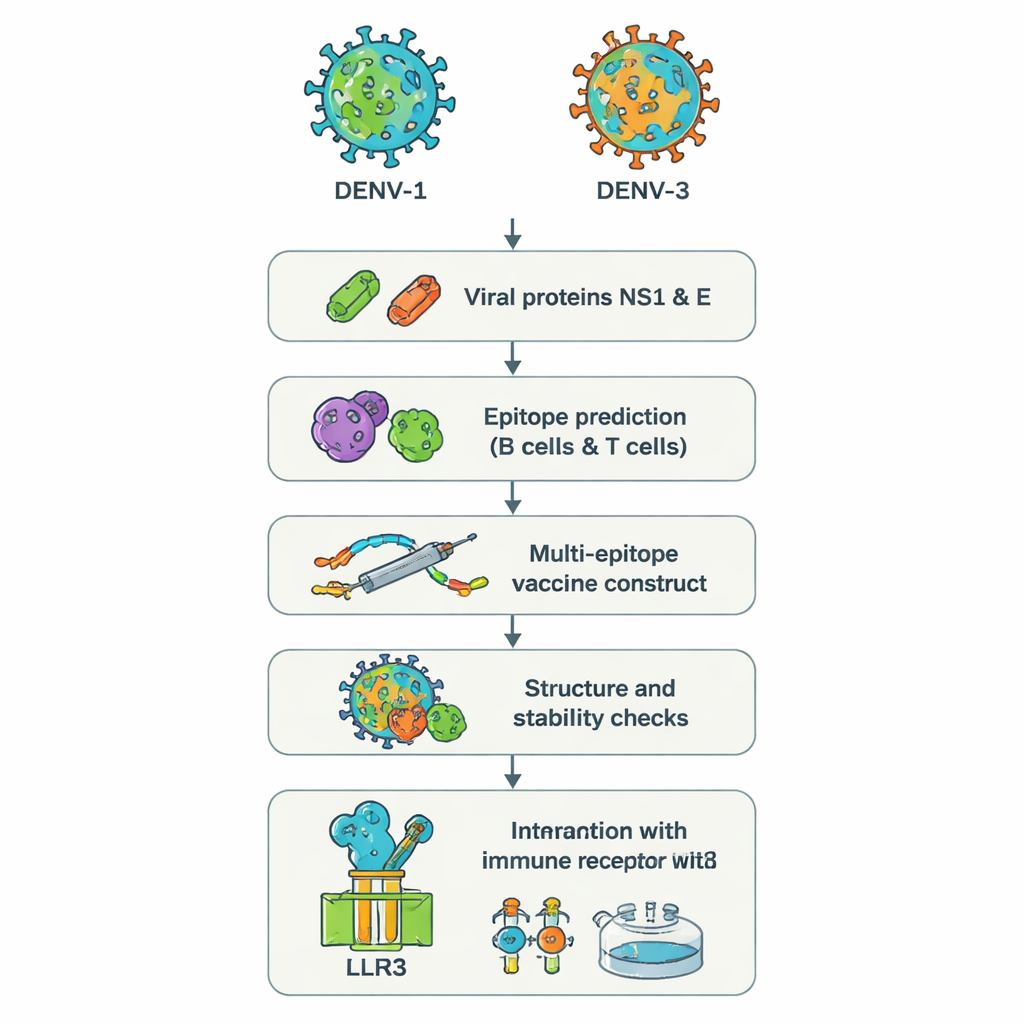
Deux sérotypes sournois et pourquoi ils posent problème
Le virus de la dengue existe en quatre variantes, appelées sérotypes DENV‑1 à DENV‑4. L’infection par l’un d’eux peut provoquer une forte fièvre, des douleurs intenses et, dans certains cas, des hémorragies potentiellement mortelles ou un choc. Fait préoccupant, retomber malade une seconde fois avec un sérotype différent peut parfois aggraver la maladie plutôt que la protéger, car des anticorps existants peuvent faciliter l’entrée du nouveau virus dans les cellules, un mécanisme appelé amélioration dépendante des anticorps. Lors des récentes flambées, des cliniciens ont signalé des patients infectés simultanément par DENV‑1 et DENV‑3, une combinaison associée à des formes plus sévères et à des résultats de tests trompeurs. Les vaccins actuels ne protègent pas de manière fiable tous les groupes d’âge et tous les sérotypes, en particulier chez les personnes sans exposition antérieure, laissant une lacune dangereuse dans les défenses.
Concevoir un vaccin à partir des molécules
Plutôt que de cultiver des virus entiers en laboratoire, les chercheurs ont utilisé une approche parfois appelée « vaccinologie inversée ». Ils sont partis des séquences génétiques de deux protéines de la dengue, NS1 et E, issues de DENV‑1 et DENV‑3. Ces protéines sont essentielles à l’entrée du virus dans les cellules et à la manière dont le système immunitaire le reconnaît. Des outils web puissants ont analysé les séquences protéiques pour repérer de courts segments — des épitopes — les plus susceptibles d’être reconnus par les cellules B humaines (qui fabriquent des anticorps) et les cellules T (qui tuent les cellules infectées et coordonnent les réponses). À partir de centaines de candidats, l’équipe a sélectionné un petit ensemble d’épitope prédits comme fortement visibles par le système immunitaire, partagés entre les deux sérotypes et capables de déclencher des signaux antiviraux utiles tels que l’interféron‑gamma.
Assembler une seule molécule vaccinale multifonction
Les épitopes choisis ont ensuite été assemblés numériquement en une longue protéine artificielle, un vaccin « multi‑épitope ». De courts liens d’acides aminés servent d’espacers flexibles pour que chaque épitope conserve sa conformation et reste accessible aux cellules immunitaires. Un fragment supplémentaire, fondé sur un peptide antimicrobien humain naturel appelé bêta‑défébine, a été ajouté comme adjuvant pour renforcer la réponse globale. L’analyse informatique a prédit que la construction finale, contenant 575 acides aminés, serait stable, hydrophile (donc plus facile à solubiliser) et peu susceptible d’agir comme allergène. D’autres outils de prédiction structurale ont généré un modèle tridimensionnel et vérifié que la plupart des éléments constitutifs occupaient des positions réalistes, semblables à celles observées dans des structures protéiques connues.
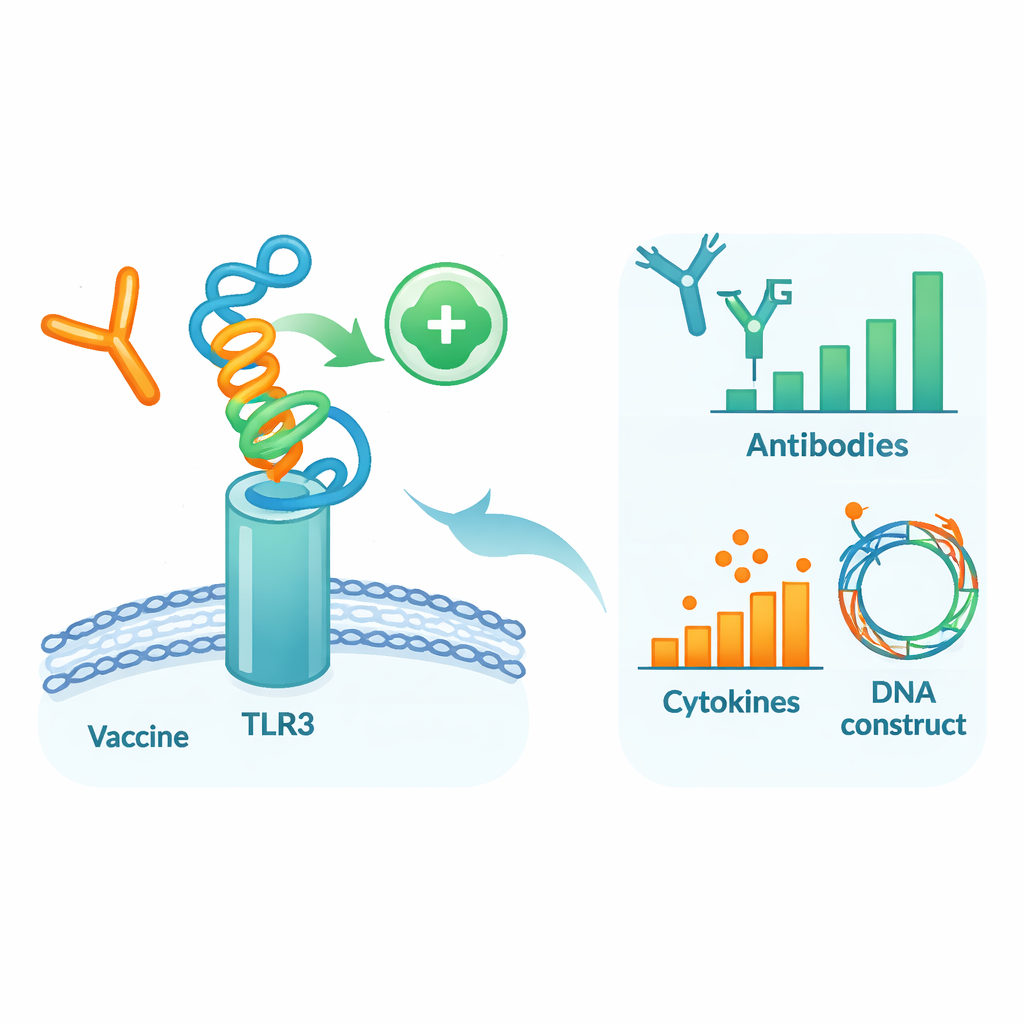
Tester le candidat dans un corps virtuel
Pour évaluer le comportement potentiel de cette protéine conçue dans un contexte proche de l’humain, les auteurs ont réalisé une série de simulations informatiques détaillées. Ils ont d’abord docké le modèle vaccinal sur TLR3, une protéine détectrice des cellules immunitaires qui repère le matériel viral et contribue à déclencher les défenses précoces. Des simulations de dynamique moléculaire — des « films » virtuels des atomes en mouvement — ont suggéré que le vaccin et TLR3 forment un complexe stable, soutenu par des énergies d’interaction favorables et de nombreux liaisons hydrogène. Des analyses complémentaires du mouvement et de l’énergie ont mis en évidence des régions spécifiques des deux molécules qui constituent des « points chauds » de contact. Ensuite, un simulateur du système immunitaire a été utilisé pour imiter trois doses du vaccin sur plusieurs mois. Le système immunitaire virtuel a produit de fortes vagues d’anticorps protecteurs IgG, des mémoires B et T durables, et des molécules de signalisation cohérentes avec une réponse antivirale robuste.
Du modèle informatique à un plan prêt pour le laboratoire
Enfin, les chercheurs ont adapté le code génétique du vaccin pour une production efficace dans des microbes de laboratoire courants et ont inséré avec succès cette séquence d’ADN optimisée dans un plasmide d’expression standard, prêt pour des tests expérimentaux futurs. En termes simples, leur travail fournit un plan détaillé pour un nouveau vaccin contre la dengue ciblant des fragments soigneusement choisis de DENV‑1 et DENV‑3, prédicté comme stable et sûr, et supposé mobiliser fortement les deux bras du système immunitaire. Bien que ces résultats soient purement computationnels et doivent être confirmés dans des cellules, des animaux, puis des humains, ils illustrent comment la bioinformatique moderne peut générer rapidement des candidats vaccinaux adaptés à des problèmes complexes comme la co‑infection par la dengue.
Citation: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Mots-clés: vaccin contre la dengue, multi-épitope, DENV-1, DENV-3, immunoinformatique