Clear Sky Science · fr
Analyse intégrative de la protéomique et de la métabolomique révèle un désordre du métabolisme des acides aminés dans des cellules de leucémie myéloïde aiguë résistantes à l’adriamycine
Pourquoi certains médicaments contre la leucémie cessent de fonctionner
La chimiothérapie a transformé le traitement de la leucémie myéloïde aiguë (LMA), un cancer du sang à croissance rapide. Pourtant, de nombreux patients voient leur maladie réapparaître parce que les cellules cancéreuses apprennent à survivre aux mêmes médicaments conçus pour les tuer. Cette étude pose une question simple mais essentielle : que change à l’intérieur des cellules leucémiques lorsqu’elles deviennent résistantes à l’adriamycine, l’un des médicaments de chimiothérapie standard, et ces modifications pourraient‑elles indiquer de nouvelles voies pour restaurer l’efficacité du médicament ?
Regarder à l’intérieur des cellules leucémiques
Pour explorer cela, les chercheurs ont comparé une lignée cellulaire humaine courante de LMA, appelée HL60, avec une lignée sœur rendue résistante à l’adriamycine (HL60/R). Plutôt que d’examiner un seul gène ou une seule protéine à la fois, ils ont utilisé deux approches larges et complémentaires. La protéomique a mesuré des milliers de protéines différentes — les molécules effectrices qui accomplissent la plupart des tâches dans une cellule. La métabolomique a mesuré des centaines de petites molécules constituant le métabolisme cellulaire, notamment lipides, sucres et acides aminés. En combinant ces couches « omiques », l’équipe a construit un tableau détaillé des différences entre les cellules résistantes et leurs homologues encore sensibles.
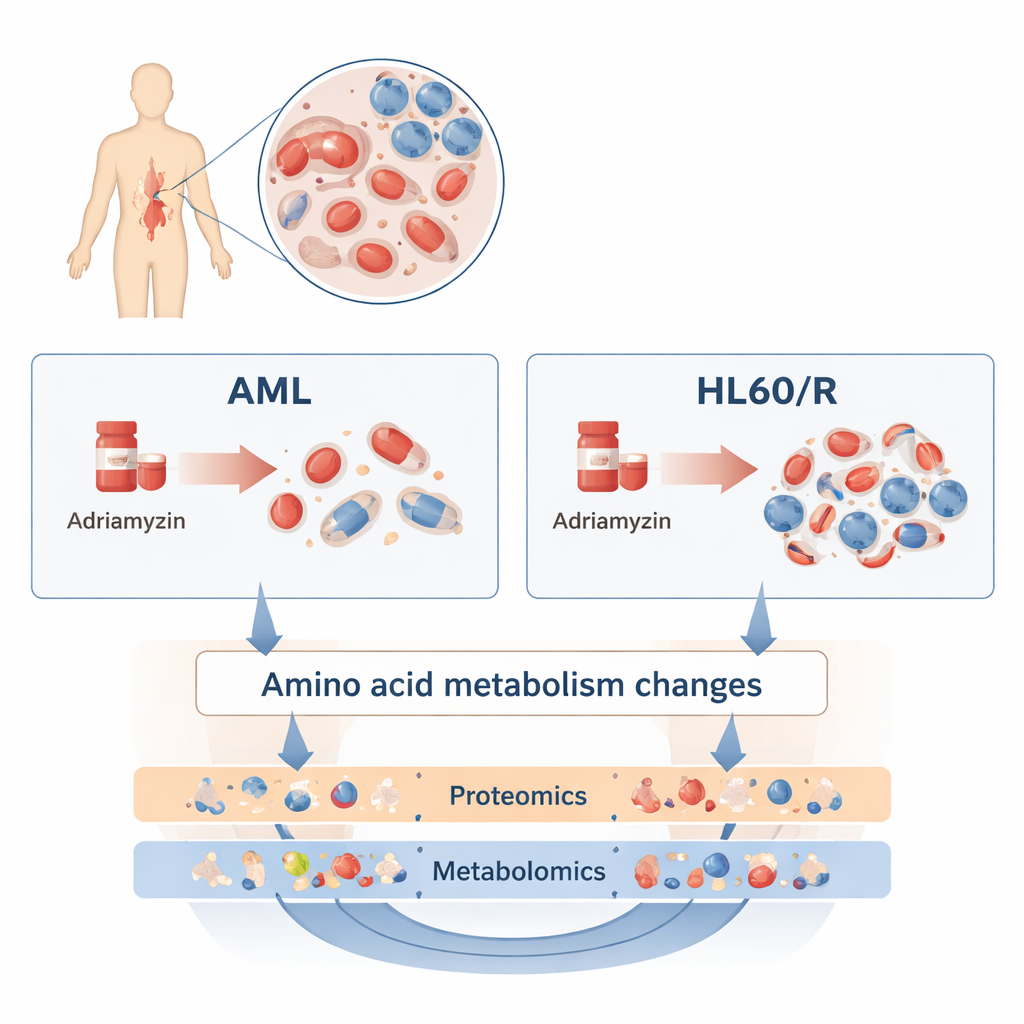
Réorganisation massive des machines cellulaires
Le relevé protéomique a révélé des changements considérables : plus de 3 200 protéines présentaient des niveaux supérieurs ou inférieurs dans les cellules résistantes à l’adriamycine comparées aux cellules HL60 normales. Beaucoup de ces protéines se regroupaient dans des voies contrôlant l’utilisation de l’énergie et la réponse au stress. En particulier, des protéines des voies de signalisation cAMP, de la voie HIF‑1 (qui aide les cellules à faire face à un faible apport en oxygène) et de la phosphorylation oxydative (un processus majeur de production d’énergie dans les mitochondries) étaient modifiées. Ces réorientations suggèrent que les cellules leucémiques résistantes reprogramment leur respiration, leur croissance et leur signalisation pour résister à la chimiothérapie.
Le métabolisme se tourne vers les acides aminés
L’analyse métabolomique a raconté une histoire complémentaire. Sur environ 1 400 métabolites détectés, 260 ont changé de manière significative dans les cellules résistantes. Des modèles statistiques ont clairement séparé les cellules résistantes des cellules non résistantes, indiquant une signature métabolique cohérente de la résistance. Lorsque les métabolites altérés ont été cartographiés sur les voies biochimiques connues, plusieurs itinéraires se sont distingués. Nombre des voies les plus fortement affectées étaient liées aux acides aminés, les éléments constitutifs des protéines — en particulier celles impliquant l’alanine, l’aspartate, le glutamate, la cystéine, la méthionine et le glutathion. D’autres réseaux, tels que le métabolisme des purines et des pyrimidines (importants pour l’ADN et l’ARN) et le métabolisme de certains lipides, étaient également perturbés, soulignant que la résistance s’accompagne d’un remaniement métabolique étendu.
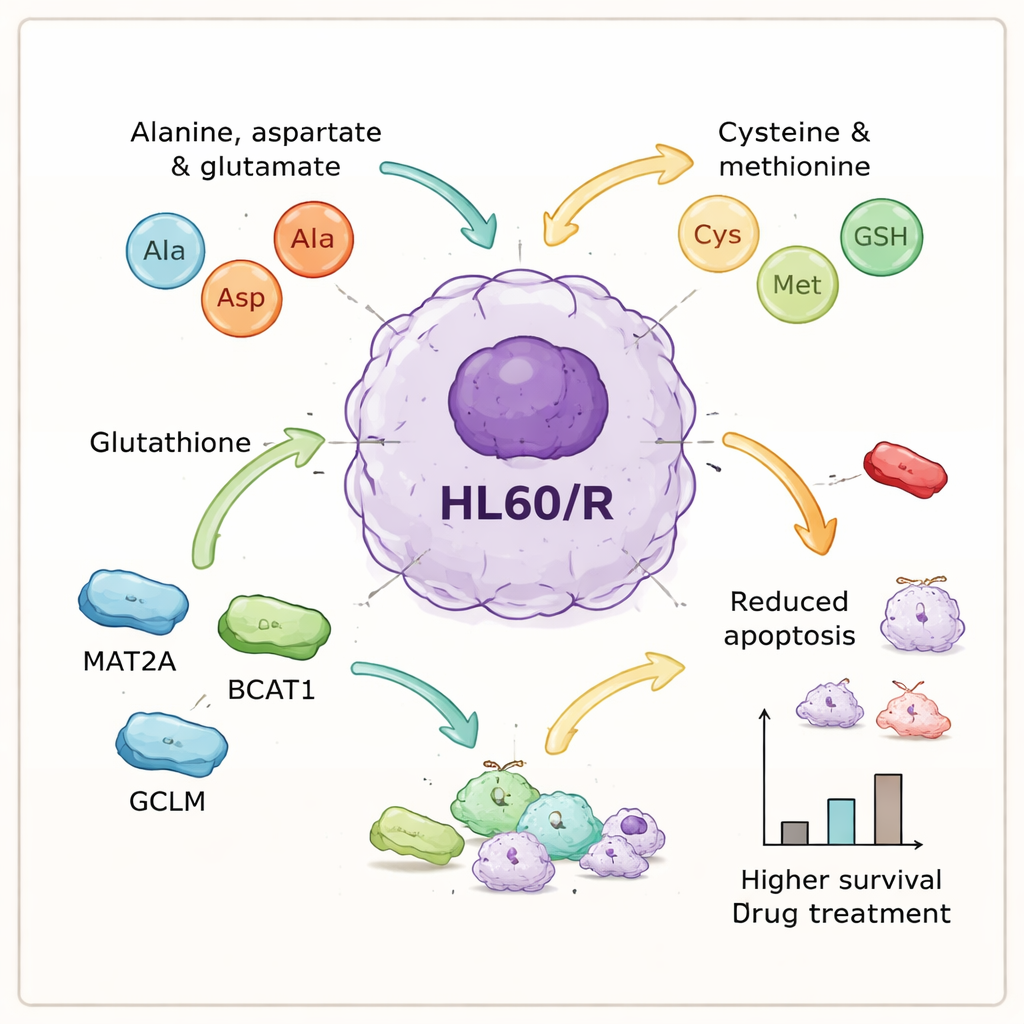
Acteurs moléculaires clés qui aident les cellules cancéreuses à durer
En intégrant les données protéiques et métabolites, les auteurs ont identifié un ensemble de processus liés aux acides aminés qui semblaient centraux pour la résistance. Ils ont retenu six protéines associées à ces voies — GOT1, GPX1, AHCY, MAT2A, BCAT1 et GCLM — pour une inspection plus approfondie. Des tests en laboratoire ont confirmé que cinq d’entre elles étaient plus abondantes dans les cellules résistantes, cohérent avec l’idée d’une augmentation du traitement des acides aminés, tandis qu’une enzyme antioxydante, GPX1, était réduite. Pour étudier la relation de cause à effet, l’équipe a utilisé de petits ARN interférents pour réduire l’expression de trois des protéines surexprimées — MAT2A, BCAT1 et GCLM — dans les cellules résistantes. Lorsque ces protéines ont été inhibées, les cellules ont subi beaucoup plus de mort cellulaire programmée après traitement, ce qui signifie qu’elles ont perdu une large partie de leur protection acquise contre l’adriamycine.
Ce que cela implique pour les traitements futurs
Pris ensemble, ces résultats suggèrent que les cellules de LMA résistantes à l’adriamycine survivent non seulement à cause de mutations isolées, mais parce qu’elles remodelent leur chimie interne, avec le métabolisme des acides aminés comme centre névralgique. En réorientant davantage de ressources vers certaines voies des acides aminés et du glutathion, les cellules semblent mieux capables de gérer le stress, réparer les dommages et éviter la mort lors de l’exposition à la chimiothérapie. Pour les non-spécialistes, le message clé est que la résistance n’est pas aléatoire : elle suit des schémas identifiables qui peuvent être mesurés et, potentiellement, ciblés. À terme, des médicaments qui interfèrent avec des protéines spécifiques du traitement des acides aminés telles que MAT2A, BCAT1 ou GCLM pourraient être associés à l’adriamycine ou à des agents similaires, offrant aux cliniciens de nouveaux outils pour prévenir ou surmonter la résistance chez les patients atteints de leucémie myéloïde aiguë.
Citation: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Mots-clés: leucémie myéloïde aiguë, résistance aux médicaments, adriamycine, métabolisme des acides aminés, multi-omique