Clear Sky Science · fr
Un modèle cellulaire fonctionnel et robuste pour le criblage à haut débit de modulateurs de Piezo1
Pourquoi de minuscules capteurs de pression dans nos cellules comptent
Chaque fois que le sang circule dans nos vaisseaux, ou que nous traversons une pièce, nos cellules ressentent de faibles forces mécaniques. Une protéine clé, véritable « capteur de pression » nommée Piezo1, aide les cellules à convertir ces forces en signaux électriques et chimiques qui maintiennent les tissus en bonne santé. Parce que Piezo1 intervient dans la croissance des vaisseaux sanguins, la résistance osseuse, l’immunité et certaines maladies génétiques rares, les développeurs de médicaments cherchent à identifier des molécules capables de moduler son activité. L’article décrit ici présente une méthode nouvelle et plus rapide pour rechercher ces molécules en utilisant des cellules génétiquement modifiées et des lectures optiques plutôt que des techniques lentes et gourmandes en main‑d’œuvre.
Transformer le toucher en signal lumineux
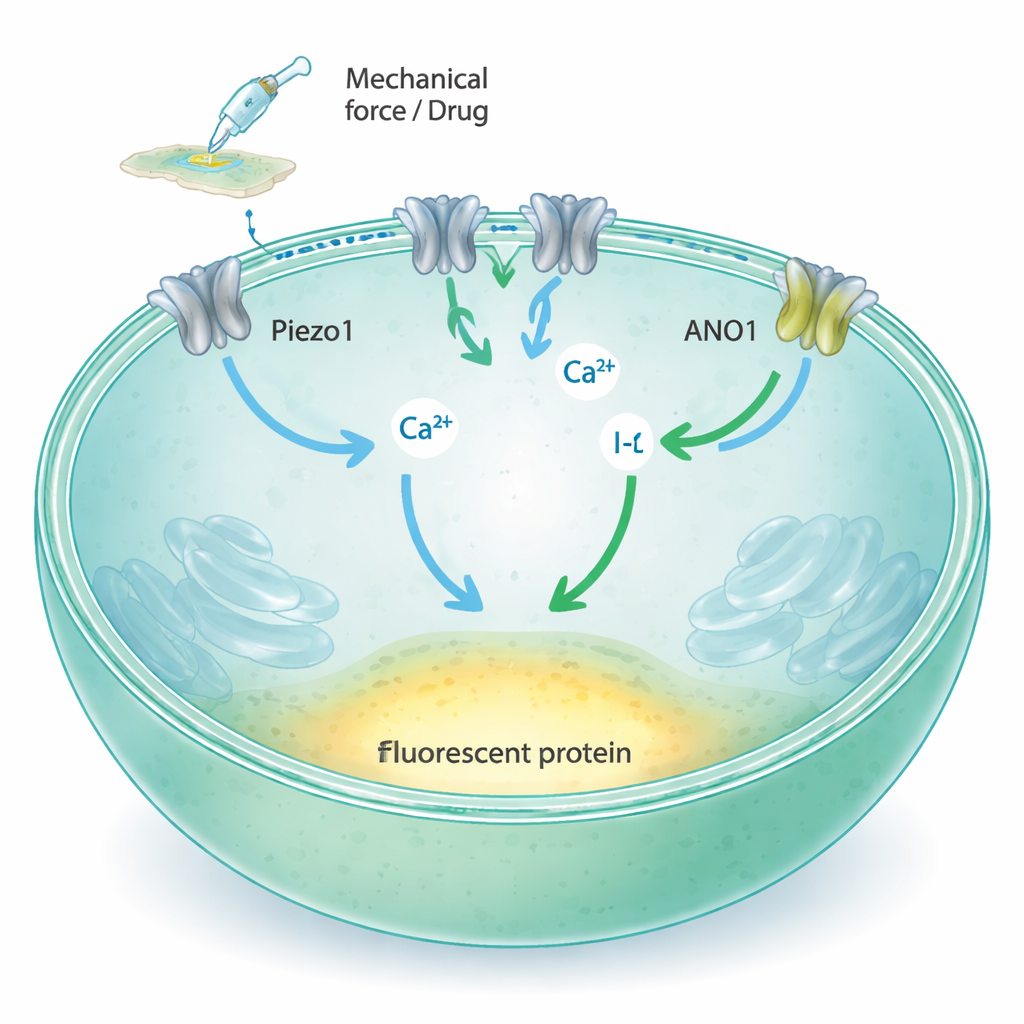
Piezo1 est un canal de la membrane cellulaire qui s’ouvre lorsque la membrane est étirée ou poussée, laissant entrer du calcium et d’autres ions chargés dans la cellule. Les méthodes classiques pour étudier ces canaux reposent sur des électrodes en verre fines ou des sondes fluorescentes spécialisées, puissantes mais difficiles à adapter aux dizaines de milliers de tests requis pour la découverte de médicaments moderne. Les auteurs ont cherché à convertir l’activité de Piezo1 en un simple changement de lumière qu’un lecteur de plaques peut mesurer rapidement sur de nombreux échantillons simultanément. Leur idée était de relier Piezo1 à deux composants supplémentaires : ANO1, un autre canal ionique sensible au calcium, et une protéine fluorescente jaune modifiée qui perd de l’intensité en présence d’ions iodure.
Construire une cellule-test réactive
Les chercheurs ont utilisé des cellules thyroïdiennes de rat Fischer (FRT), qui expriment naturellement Piezo1 et adhèrent bien aux plaques plastiques standard. Ils ont confirmé que ces cellules expriment Piezo1 mais pas son homologue proche Piezo2, et montré que Piezo1 dans ces cellules répond au flux de fluide et à la sonde mécanique en laissant entrer du calcium. Ensuite, ils ont introduit le canal ANO1 et la protéine fluorescente sensible à l’iodure (YFP‑H148Q/I152L) dans les cellules. Lorsque le calcium augmente à l’intérieur de la cellule, ANO1 s’ouvre et permet à l’iodure d’entrer ; la protéine fluorescente devient alors moins lumineuse au fur et à mesure que l’iodure s’accumule autour d’elle. La microscopie, la cytométrie en flux et les enregistrements électriques ont montré que l’ANO1 et le capteur fluorescent étaient présents en grande quantité et fonctionnaient comme prévu.
De l’action d’un médicament à un signal lumineux mesurable
Avec ce système en trois parties, l’équipe a établi une chaîne de cause à effet simple : si une molécule test active Piezo1, le calcium entre, ANO1 s’ouvre, l’iodure afflue et le signal de fluorescence diminue ; si une molécule bloque Piezo1, le signal reste lumineux. Ils ont validé cette logique en utilisant des activateurs bien connus de Piezo1 (Yoda1, Jedi1, Jedi2) et des bloqueurs (Ruthenium Red, GsMTx4). Les activateurs ont provoqué des diminutions de fluorescence dépendantes de la dose, avec des valeurs de sensibilité cohérentes avec les données publiées. Les bloqueurs ont produit le schéma inverse, réduisant la réponse à mesure que leur concentration augmentait. L’essai ne fonctionnait que lorsque le calcium et l’iodure étaient présents, ce qui souligne que le signal dépendait bien de l’entrée de calcium induite par Piezo1 et de l’afflux d’iodure médié par ANO1. Des mesures statistiques telles que le facteur Z et le rapport signal/bruit ont indiqué que la méthode est suffisamment stable et fiable pour un criblage à l’échelle industrielle.
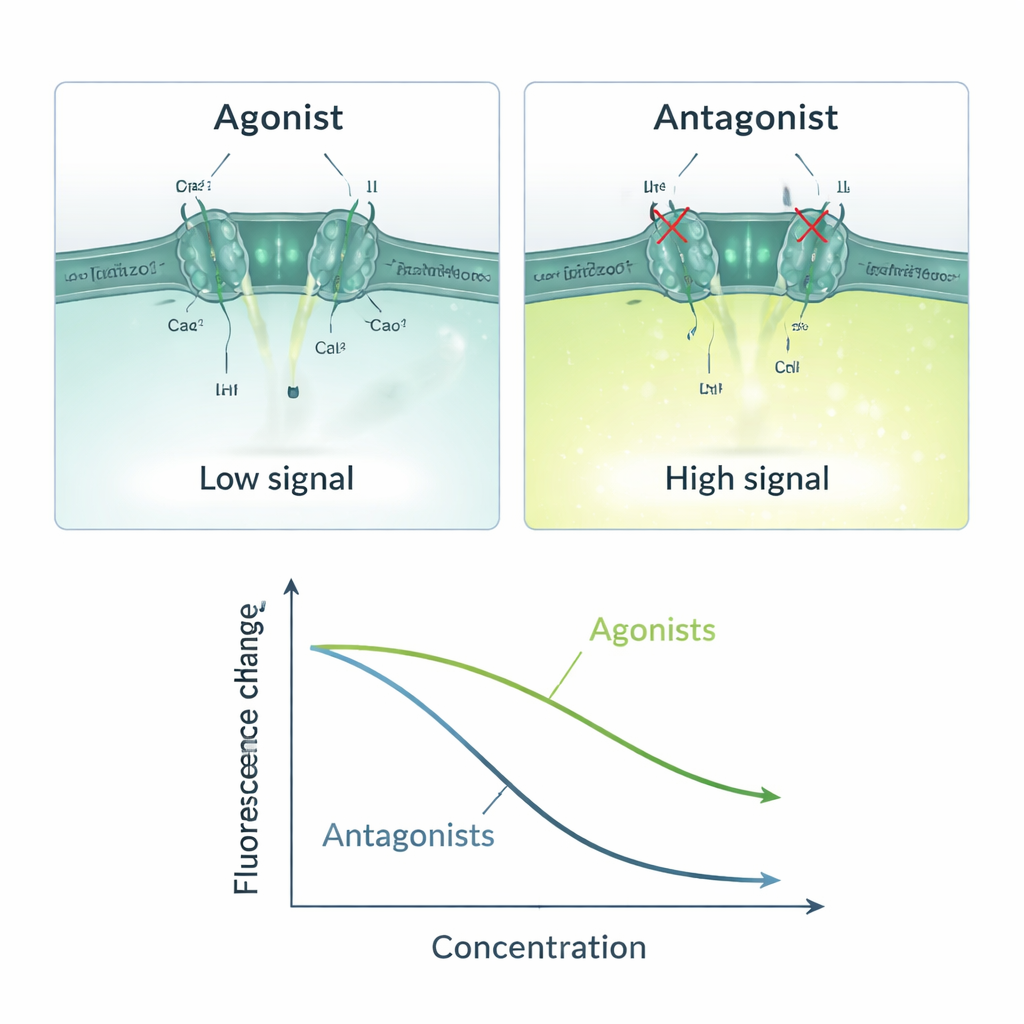
Tests rapides et évolutifs, avec quelques réserves
Le nouveau modèle cellulaire peut réaliser une mesure d’un puits en environ 14 secondes et scanner une plaque de 96 puits en près de 22 minutes, et il peut être adapté à des instruments lisant des centaines de puits simultanément. Les cellules modifiées restent stables pendant de nombreuses générations sous sélection antibiotique, ce qui permet de répéter les expériences dans le temps. Parce que la lecture est optique et utilise du matériel de microplaque standard, l’approche est relativement peu coûteuse et accessible. Cependant, les auteurs soulignent que leur test est indirect : toute molécule agissant sur des étapes en amont ou en aval de Piezo1 dans la chaîne de signalisation — comme ANO1 lui‑même ou d’autres protéines gérant le calcium — peut produire un faux positif. Pour cette raison, les « hits » issus de ce criblage doivent encore être confirmés par des méthodes plus directes comme l’électrophysiologie.
Ce que cela signifie pour les traitements futurs
Concrètement, les chercheurs ont construit une sorte de « détecteur de fumée » de laboratoire qui s’assombrit chaque fois qu’un composé pousse Piezo1 à s’ouvrir, et reste lumineux quand Piezo1 est bloqué. Cet avertisseur est sensible, rapide et facile à déployer à grande échelle, ce qui le rend bien adapté pour un premier passage dans la recherche de médicaments visant à moduler les capteurs mécaniques du corps. Bien qu’il ne remplace pas les tests de suivi plus détaillés, ce modèle cellulaire constitue un point de départ puissant pour découvrir des molécules qui pourraient un jour aider à traiter des troubles vasculaires, des maladies osseuses, des problèmes immunitaires et d’autres affections liées à la manière dont nos cellules ressentent et répondent aux forces physiques.
Citation: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Mots-clés: Canal Piezo1, canaux ioniques mécanosensibles, criblage à haut débit, essai cellulaire, découverte de médicaments