Clear Sky Science · fr
Effets radiosensibilisants des nanoparticules d’argent ciblant l’angiogenèse et la signalisation des métalloprotéinases matricielles dans des lignées cellulaires de cancer du sein triple négatif
Rendre les cancers du sein les plus difficiles plus vulnérables
Le cancer du sein triple négatif est l’une des formes de cancer du sein les plus difficiles à traiter. Il a tendance à croître rapidement, à se propager tôt et il manque des « poignées » moléculaires habituelles auxquelles s’accrochent de nombreux médicaments modernes. La radiothérapie fait souvent partie du traitement, mais ces tumeurs peuvent rester tenacement résistantes. Cette étude pose une question simple et intrigante : de minuscules particules d’argent peuvent-elles améliorer l’efficacité de la radiation tout en ralentissant la capacité de la tumeur à former de nouveaux vaisseaux sanguins et à se disséminer ?
Petits alliés argentés pour la radiothérapie
Les chercheurs se sont concentrés sur des nanoparticules d’argent — des sphères d’argent ultra petites mesurées en milliardièmes de mètre. Parce que l’argent est dense et interagit fortement avec les rayons X, ces particules peuvent concentrer les effets de la radiation là où elles s’accumulent. L’équipe a travaillé avec deux modèles de laboratoire largement utilisés du cancer du sein triple négatif, en les comparant à une lignée cellulaire mammaire non cancéreuse. Ils ont d’abord testé la toxicité des nanoparticules d’argent seules et ont constaté que les cellules cancéreuses étaient tuées à des doses bien plus faibles que les cellules normales, ce qui suggère une fenêtre thérapeutique utile. En utilisant des méthodes mathématiques pour analyser l’interaction entre les particules et la radiation, ils ont montré que la combinaison des deux produisait un effet anticancéreux clairement plus puissant que chaque traitement pris isolément.
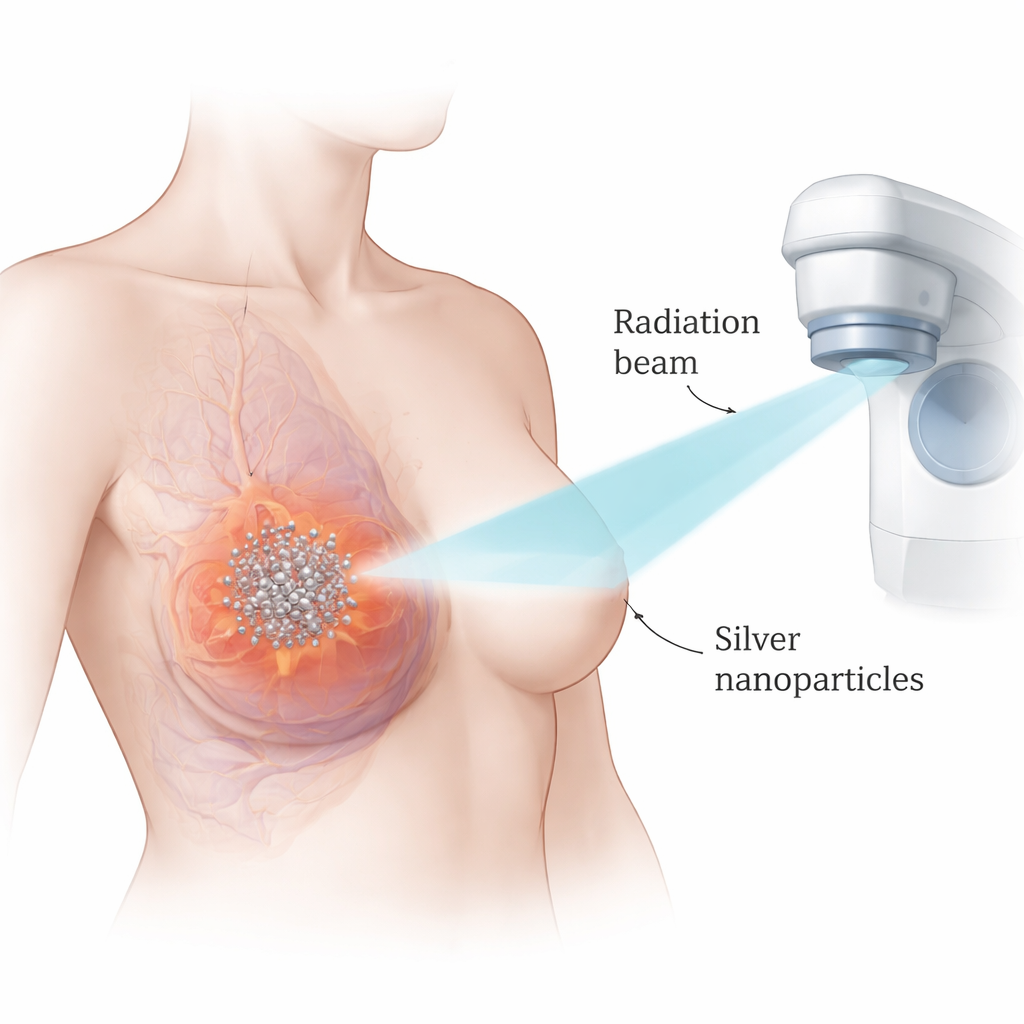
Forcer les cellules cancéreuses à s’autodétruire
Puis, les scientifiques ont examiné comment le traitement combiné tuait les cellules. Ils ont mesuré l’apoptose, une forme de suicide cellulaire programmé, et suivi l’accumulation de molécules hautement réactives connues sous le nom d’espèces réactives de l’oxygène (ROS). On sait déjà que la radiation agit en partie en générant des ROS qui endommagent l’ADN. Dans les deux lignées de cancer du sein triple négatif, les nanoparticules d’argent seules augmentaient l’apoptose et les niveaux de ROS, et la radiation seule produisait un effet similaire — mais leur utilisation conjointe faisait grimper ces deux mesures de façon spectaculaire. Cela signifie qu’un plus grand nombre de cellules cancéreuses étaient poussées vers un mode d’autodestruction ordonné, plutôt que de rester dans un état endommagé qui peut parfois favoriser la rechute ou la résistance.
Couper l’apport sanguin et ralentir la dissémination
Les tumeurs dépendent des vaisseaux sanguins pour apporter oxygène et nutriments, et les cancers agressifs peuvent même imiter des vaisseaux sanguins eux-mêmes. L’équipe a examiné deux interrupteurs moléculaires clés impliqués dans la construction et la stabilisation des vaisseaux tumoraux, appelés VEGFR2 et Tie2. Dans les deux lignées, les nanoparticules d’argent ont réduit l’activité de ces gènes, et la combinaison avec la radiation les a encore plus inhibés. Ils ont aussi étudié deux enzymes, MMP-2 et MMP-9, qui aident les cellules cancéreuses à dégrader les tissus environnants et à migrer. Dans un des modèles cellulaires, la radiation et les nanoparticules d’argent diminuaient ces enzymes, tandis que le traitement combiné produisait l’effet le plus marqué. Lorsque les chercheurs ont observé le déplacement des cellules cancéreuses pour combler une « égratignure » artificielle dans une boîte de culture, et lorsqu’ils ont testé la formation de tubes de type vasculaire dans un système de coculture, le traitement combiné a le plus clairement ralenti la migration et la formation de tubes.
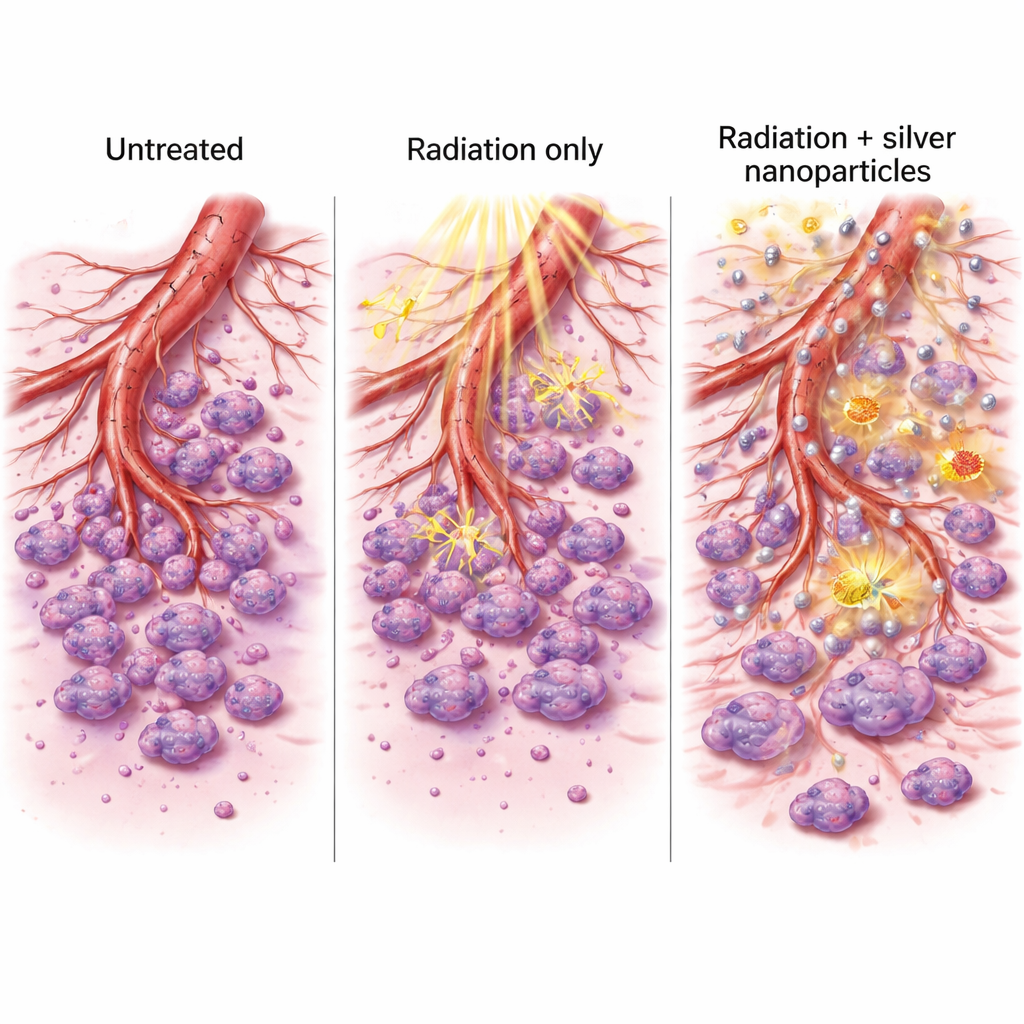
Pourquoi ces changements sont importants
En réduisant l’expression des gènes qui favorisent la néovascularisation et des enzymes qui facilitent l’invasion cellulaire, l’association argent-plus-radiation a fait plus que tuer des cellules cancéreuses. Elle a aussi perturbé les systèmes de soutien que les tumeurs utilisent pour s’étendre et se disséminer. Les cellules traitées étaient moins capables de refermer des plaies dans des boîtes de culture et moins aptes à s’organiser en réseaux ramifiés ressemblant à de premiers vaisseaux sanguins. Associés à l’augmentation marquée de la mort cellulaire et de la production de ROS, ces effets suggèrent un double avantage : une attaque directe plus puissante contre la tumeur et un affaiblissement des outils nécessaires à une croissance et des métastases futures.
Ce que cela pourrait signifier pour les patients
Pour l’instant, ces résultats proviennent de cellules cancéreuses cultivées en laboratoire, pas de patients. Néanmoins, ils dressent un tableau encourageant. Les nanoparticules d’argent ont agi comme radiosensibilisants, rendant la radiothérapie standard plus efficace contre les cellules de cancer du sein triple négatif. En parallèle, elles semblaient étouffer la capacité de la tumeur à construire des réseaux d’irrigation sanguine et à envahir les tissus voisins. Si des études animales et cliniques futures confirment que ces particules peuvent être délivrées de manière sûre et sélective aux tumeurs, elles pourraient permettre aux médecins d’utiliser des doses de radiation plus faibles tout en obtenant de meilleurs résultats, offrant une nouvelle voie pour combattre l’une des formes de cancer du sein les plus difficiles.»
Citation: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Mots-clés: cancer du sein triple négatif, nanoparticules d’argent, radiothérapie, angiogenèse, métastase