Clear Sky Science · fr
Des bis-4-hydroxycoumarines chlorées suppriment la réplication des flavivirus en inhibant la traduction et la réplication du virus de la dengue de type 2
Nouveaux espoirs contre les virus transmis par les moustiques
Les virus de la dengue et du Zika infectent des centaines de millions de personnes chaque année, souvent dans des régions aux ressources médicales limitées. Les vaccins n’offrent qu’une protection partielle et il n’existe toujours pas de médicament antiviral largement utilisé que les médecins puissent prescrire dès les premiers symptômes. Cette étude examine une famille de composés synthétiques inspirés de molécules végétales, en posant une question simple mais urgente : l’un d’eux peut‑il ralentir de manière fiable ces virus à l’intérieur de cellules humaines sans nuire aux cellules elles‑mêmes ?
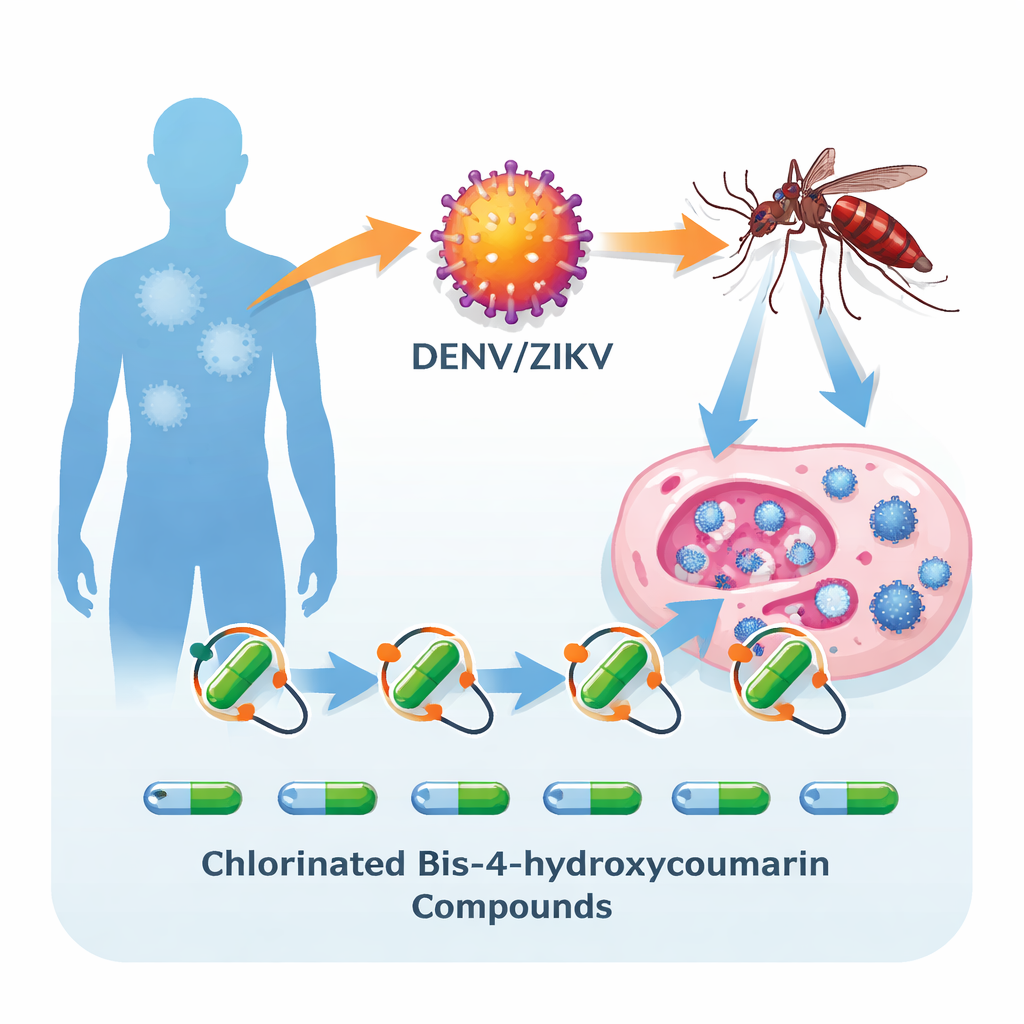
Des molécules inspirées des plantes comme bloqueurs viraux
Les chercheurs se sont concentrés sur les coumarines, une classe de composés naturels présents dans de nombreuses plantes et connues depuis longtemps pour leur potentiel antimicrobien et antiviral. Ils ont testé douze dérivés de « biscoumarines » — deux unités de coumarine liées entre elles — contre le virus de la dengue de type 2 et le virus Zika dans des cellules en culture. En mesurant le nombre de particules virales infectieuses produites et l’état de santé des cellules, ils ont découvert que deux variantes chlorées, nommées composé 3 et composé 4, étaient particulièrement prometteuses. À de faibles concentrations micromolaires, ces bis‑4‑hydroxycoumarines chlorées réduisaient la production virale de plus de 90 % tout en préservant la viabilité et le fonctionnement de la plupart des cellules.
Ajuster la chimie pour une protection renforcée
Toutes les modifications chimiques n’ont pas eu le même effet. En modifiant systématiquement les atomes autour d’une partie annulée des molécules, l’équipe a constaté que l’ajout de chlore à des positions spécifiques conférait la meilleure activité antivirale. Remplacer le chlore par d’autres halogènes comme le fluor ou le brome — ou ajouter d’autres groupements chimiques — affaiblissait généralement l’effet sur la dengue et le Zika. À l’aide de modèles informatiques, ils ont corrélé la puissance antivirale à des caractéristiques moléculaires simples, comme la répartition des charges et la surface exposée. Des méthodes d’apprentissage automatique ont capturé ces relations bien mieux que des outils statistiques plus anciens, suggérant que l’intelligence artificielle peut aider à orienter la conception de candidats‑médicaments anti‑dengue améliorés.
Comment les composés perturbent le cycle viral
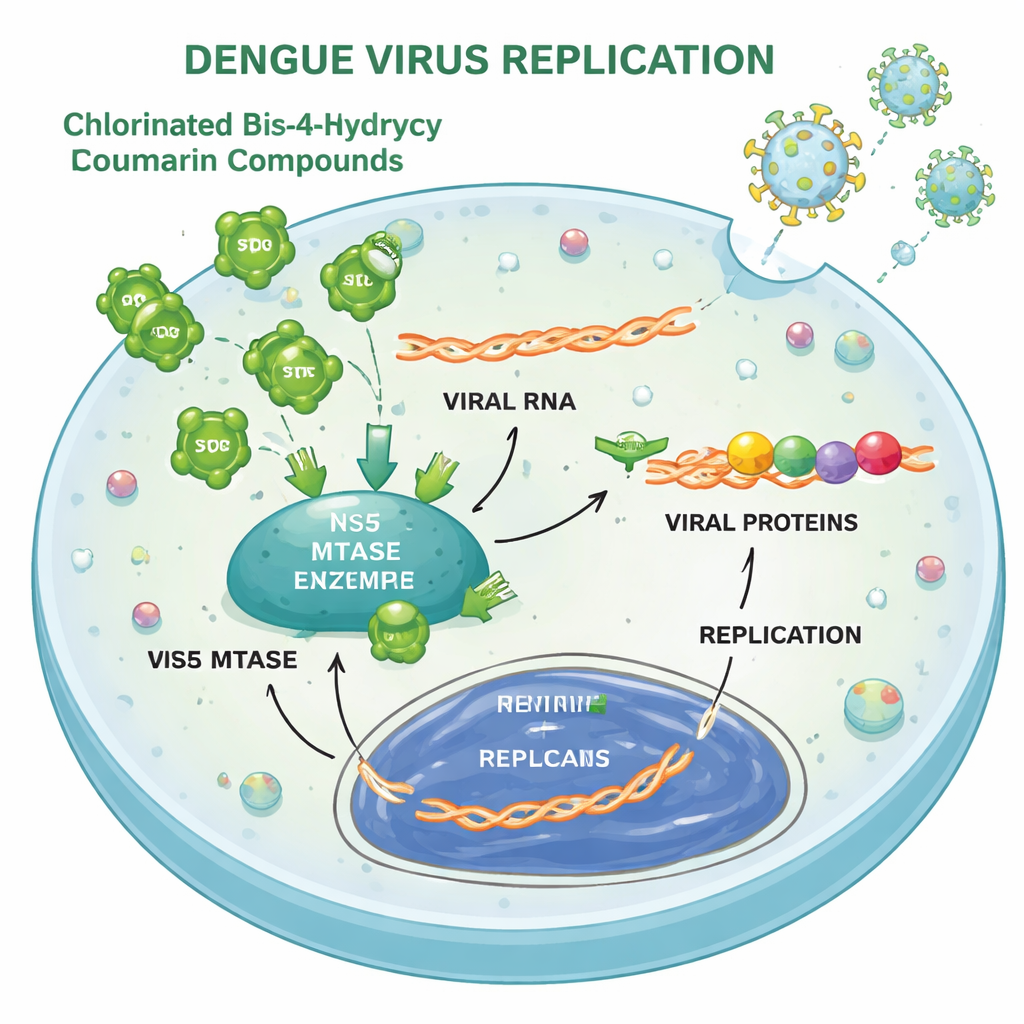
Une fois à l’intérieur d’une cellule, le virus de la dengue utilise son génome ARN comme plan pour fabriquer une longue polyprotéine qui est découpée en éléments fonctionnels, puis copie son ARN pour engendrer de nouveaux virus. L’étude montre que les composés 3 et 4 perturbent principalement ces étapes de traduction et de réplication. Dans les cellules infectées, la quantité d’une protéine de capside virale clé chutait nettement en présence des composés, et un système rapporteur suivant la réplication de l’ARN viral montrait également une diminution dépendante de la dose. Des tests biochimiques et des docks informatiques ont identifié une enzyme virale, la méthyltransférase NS5, comme une cible directe mais relativement faible : les composés pouvaient inhiber sa fonction de « capping » de l’ARN, bien moins efficacement qu’un inhibiteur de référence connu. Ils ralentissaient aussi modestement la protéase virale, une autre enzyme impliquée dans la découpe de la polyprotéine.
Les virus peinent à s’adapter à l’attaque
Les virus échappent souvent aux médicaments par mutation. Pour savoir si cela pouvait se produire ici, l’équipe a cultivé à plusieurs reprises le virus de la dengue dans des cellules exposées aux nouveaux composés sur de nombreux cycles d’infection. Plusieurs changements sont apparus dans une autre protéine virale, NS4B, qui participe à la courbure des membranes cellulaires pour former de petites poches où la réplication a lieu. De façon surprenante, ces virus mutés n’étaient pas moins sensibles aux composés que la souche originale. Des structures prédites par ordinateur suggéraient que la conformation globale de NS4B restait largement inchangée. Ce schéma laisse entendre que les mutations constituaient des ajustements généraux face au stress plutôt qu’une résistance vraie et spécifique. Il soutient aussi l’idée que les composés agissent sur plusieurs éléments de la machinerie de réplication ou sur des facteurs cellulaires de l’hôte que le virus ne peut pas facilement reprogrammer.
Pourquoi ces résultats comptent pour les traitements futurs
Pour le grand public, le message principal est que les chercheurs ont mis au jour un nouveau « échafaudage » chimique capable de ralentir les virus de la dengue et du Zika à plusieurs étapes de leur cycle de vie, notamment lors de la traduction des gènes viraux et de la copie de l’ARN à l’intérieur des cellules. La molécule la plus prometteuse, le composé 3, agit à faibles doses, nuit relativement peu aux cellules, cible les quatre principaux sérotypes de la dengue ainsi que le Zika, et ne pousse pas rapidement le virus à évoluer une résistance en laboratoire. Bien que ces bis‑4‑hydroxycoumarines chlorées soient encore loin d’être des médicaments, elles offrent un point de départ solide pour que chimistes et virologues affinent ces composés, les testent chez l’animal et, éventuellement, les associent à d’autres médicaments — des étapes qui pourraient nous rapprocher d’un comprimé antiviral très attendu contre les infections transmises par les moustiques.
Citation: Loeanurit, N., Phan, THT., Hengphasatporn, K. et al. Chlorinated bis-4-hydroxycoumarins suppress flavivirus replication by inhibiting dengue virus type 2 translation and replication. Sci Rep 16, 5300 (2026). https://doi.org/10.1038/s41598-026-35654-8
Mots-clés: virus de la dengue, virus Zika, composés antiviraux, dérivés de coumarine, réplication virale