Clear Sky Science · fr
Réponse chémosensorielle aux chimiothérapies à base de platine via les récepteurs du goût amer in vitro révèle un nouveau mécanisme des troubles du goût amer
Pourquoi les médicaments contre le cancer peuvent soudain rendre tout amer
Les patients atteints de cancer signalent souvent que les aliments prennent un goût étrangement amer ou métallique peu de temps après le début de la chimiothérapie. Cela va au‑delà du simple déplaisir : cela peut réduire l’appétit, favoriser la perte de poids et diminuer la qualité de vie alors même que les patients ont le plus besoin de force. Cette étude pose une question apparemment simple mais aux conséquences pratiques importantes : comment les médicaments chimiothérapeutiques courants à base de platine perturbent‑ils exactement notre sens du goût, et peut‑on atténuer cet effet en toute sécurité sans affaiblir le traitement ?
Le rôle caché des « capteurs d’amer » dans la bouche et l’intestin
Notre langue et notre tractus digestif sont ponctués de récepteurs du goût amer, conçus pour nous avertir de substances potentiellement nuisibles. Ces capteurs, appelés TAS2R, ne se limitent pas aux papilles gustatives ; on les trouve également dans les cellules de l’estomac. Les chercheurs ont utilisé une lignée cellulaire gastrique humaine (HGT‑1) qui se comporte comme un détecteur d’amertume in vitro : lorsque les récepteurs amers sont activés, les cellules expulsent davantage de protons (acide), ce qui se mesure par un indice intracellulaire de protons. En exposant ces cellules à deux médicaments anticancéreux à base de platine très utilisés — le carboplatine et le cisplatine — l’équipe a pu examiner en toute sécurité à quel point ces médicaments paraissent « amers » aux cellules humaines sans jamais demander à une personne de goûter un composé toxique. 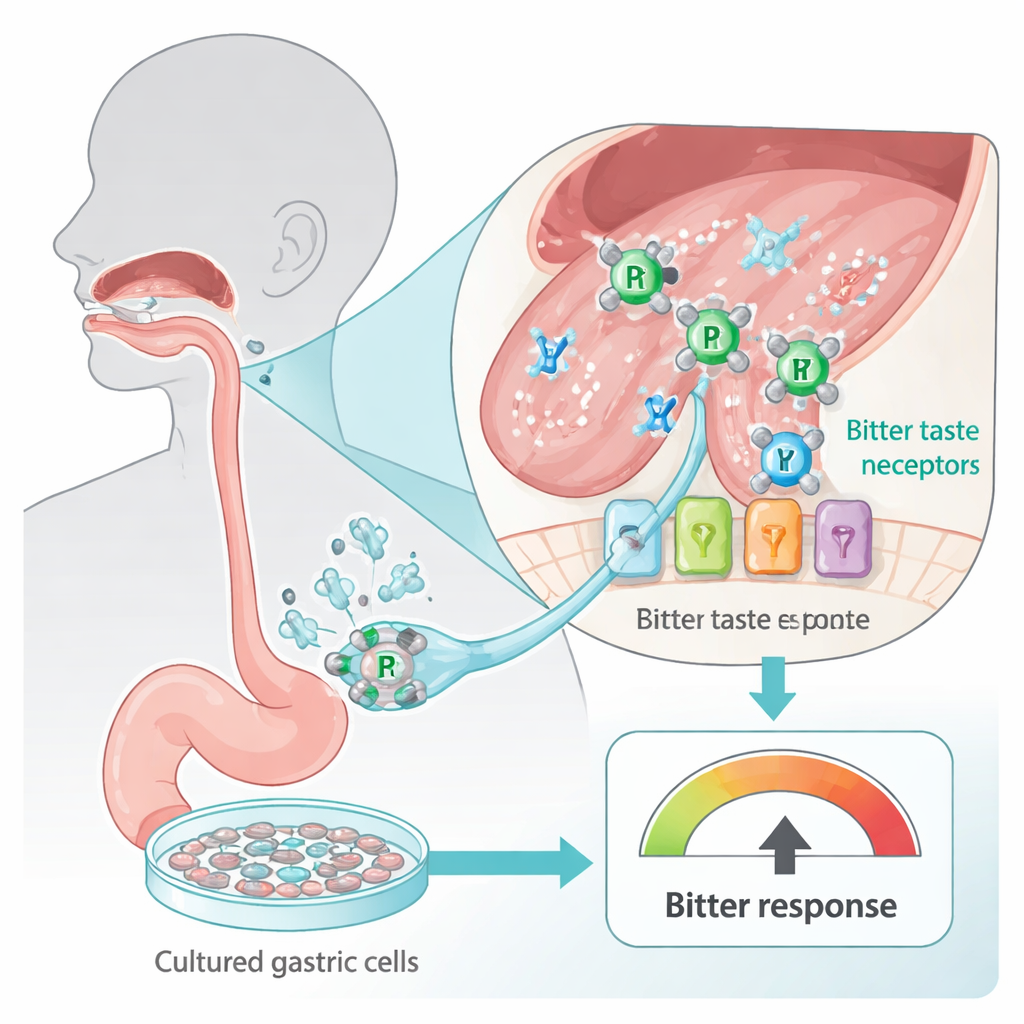
Des médicaments de chimiothérapie qui ont un goût amer pour les cellules
Lorsque les cellules gastriques ont été traitées à des concentrations cliniquement pertinentes de carboplatine et de cisplatine, les deux médicaments ont déclenché une réponse de type amer nette et dépendante de la dose : plus la dose était élevée, plus la réaction cellulaire était forte. Le cisplatine, toutefois, a produit une réponse plus intense que le carboplatine si l’on tient compte de leur ratio posologique thérapeutique habituel (environ 1:4), ce qui suggère qu’il peut contribuer davantage aux problèmes de goût amer chez les patients. Au niveau génétique, l’exposition à ces médicaments a modifié l’activité de plusieurs gènes codant des récepteurs amers dans les cellules, indiquant que les agents à base de platine n’agissent pas sur un seul « interrupteur de l’amer » mais remodelent largement le système de détection de l’amer. Parmi ces récepteurs, TAS2R4 et TAS2R5 se sont distingués comme étant à la fois très actifs et fortement affectés par le traitement.
Désactiver les signaux amers et tester un bloqueur d’amer naturel
Pour identifier les récepteurs les plus importants, l’équipe a désactivé sélectivement certains récepteurs amers. L’élimination de TAS2R4 ou la réduction de l’expression de TAS2R5 ont chacune réduit la réponse de type amer au carboplatine et au cisplatine, confirmant que ces récepteurs contribuent à la détection des médicaments. Les scientifiques ont ensuite testé une contre‑mesure prometteuse : le sel sodique de l’homoeriodictyol (Na‑HED), une flavanone isolée à l’origine de la plante nord‑américaine Herba Santa et déjà connue pour masquer l’amertume d’autres composés. Lorsqu’on a ajouté Na‑HED conjointement aux médicaments à base de platine, il a nettement atténué la réponse cellulaire amère — d’environ trois quarts pour le carboplatine et le cisplatine — sans nuire aux cellules lorsqu’il était utilisé seul. Cela montre que Na‑HED peut agir directement sur les récepteurs amers pour atténuer le signal déclenché par les chimiothérapies.
Quand la détection de l’amer et l’absorption du médicament se croisent
Au‑delà d’expliquer pourquoi la chimiothérapie au platine peut être perçue comme amère, l’étude révèle une tournure inattendue : ces mêmes récepteurs amers semblent aussi influencer la quantité de ces médicaments qui pénètre dans les cellules. À l’aide d’une spectrométrie de masse très sensible, les chercheurs ont mesuré la teneur en platine à l’intérieur des cellules après traitement. Les cellules dépourvues de certains récepteurs, tels que TAS2R4 ou TAS2R43, ont accumulé plus de platine que les cellules normales, ce qui suggère que des récepteurs intacts aident à limiter l’entrée ou la rétention de ces agents toxiques. Na‑HED n’a pas modifié l’absorption du carboplatine, mais il a réduit la quantité de cisplatine entrant dans les cellules et a montré une interaction moléculaire directe avec le cisplatine en solution. Cela laisse entendre qu’un composé masquant l’amer pourrait, dans certains cas, aussi moduler l’impact local d’un médicament sur les tissus, comme les cellules gustatives ou les glandes salivaires. 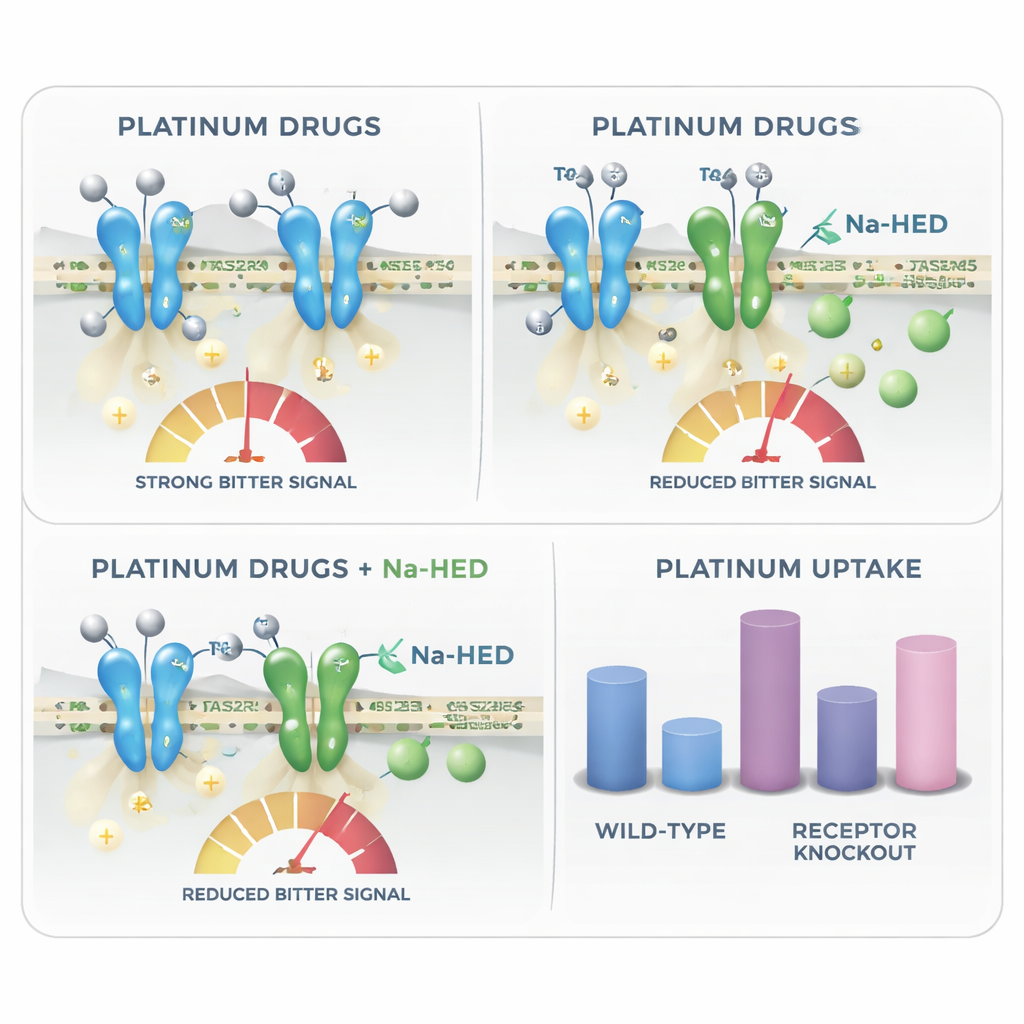
Vers des expériences gustatives plus douces pendant la chimiothérapie
Pour les patients, l’enseignement principal est porteur d’espoir : la chimiothérapie à base de platine semble provoquer des troubles du goût amer en activant directement des récepteurs amers présents non seulement sur la langue mais aussi dans des cellules de type intestinal. Le cisplatine paraît particulièrement puissant à cet égard. L’étude montre que Na‑HED peut considérablement atténuer ce signal amer dans un système cellulaire contrôlé et peut aussi limiter l’absorption locale du cisplatine. Si ces résultats doivent être confirmés chez l’homme, ils ouvrent la voie à de futurs bains de bouche « rincer et recracher » contenant du Na‑HED qui pourraient adoucir les sensations âpres et métalliques sans interférer avec l’action anticancéreuse des médicaments à l’échelle de l’organisme.
Citation: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Mots-clés: altérations du goût liées à la chimiothérapie, récepteurs du goût amer, cisplatine et carboplatine, composés masquant l'amer, nutrition des patients atteints de cancer