Clear Sky Science · fr
Calculs DFT de la complexation de Ac3+ et Bi3+ par le chélateur hybride 3p-C-DEPA pour la radiothérapie alpha ciblée
Pourquoi cette recherche compte pour le traitement du cancer
La médecine oncologique moderne s’appuie de plus en plus sur des médicaments radioactifs capables de traquer les tumeurs cellule par cellule. Une approche puissante, appelée thérapie alpha ciblée, utilise des particules très énergétiques qui peuvent tuer des cellules cancéreuses individuelles avec une précision remarquable. Mais pour délivrer ces particules en toute sécurité, le métal radioactif doit être enfermé dans une « cage » moléculaire afin qu’il ne migre pas vers les tissus sains. Cette étude explore une nouvelle molécule‑cage, 3p‑C‑DEPA, conçue pour accueillir des métaux particulièrement difficiles comme l’actinium‑225 et le bismuth‑213, et pose la question : peut‑elle les lier plus solidement que le chélateur de référence actuel, DOTA ?
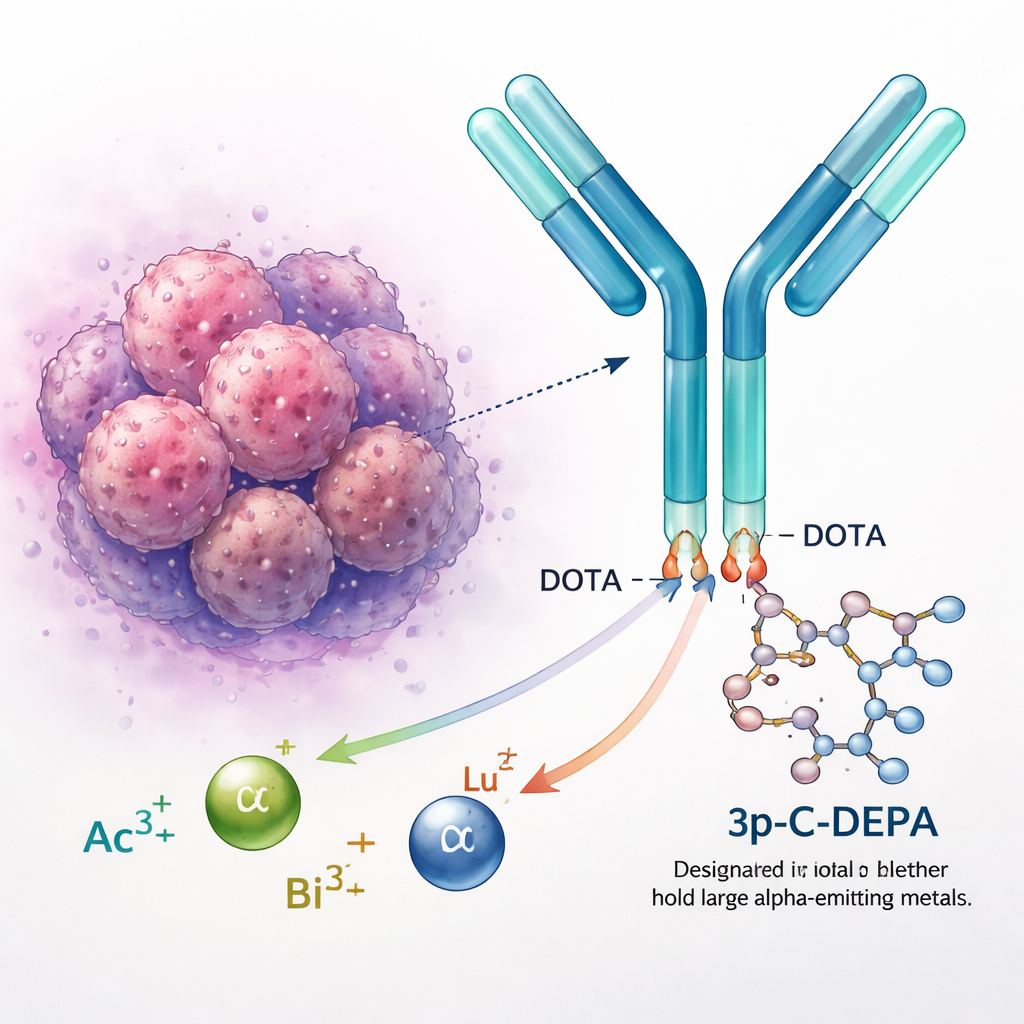
Verrouiller les métaux radioactifs en toute sécurité
Des métaux radioactifs tels que l’actinium, le bismuth et le lutécium sont utilisés pour diagnostiquer et traiter le cancer. Pris isolément, cependant, ces ions métalliques chargés positivement interagiraient librement avec l’organisme, risquant d’endommager des organes sains. Les chimistes les attachent donc à des « chélateurs », des molécules en forme d’anneau qui entourent le métal et le maintiennent en place. Le chélateur de référence DOTA est employé dans plusieurs médicaments approuvés, mais il peine avec des ions plus volumineux et plus diffus comme l’actinium‑225. Ces métaux peuvent s’échapper avec le temps, soulevant des inquiétudes sur la sécurité à long terme et limitant l’usage de la thérapie alpha ciblée.
Une cage hybride conçue pour les atomes plus gros
Le nouveau chélateur, 3p‑C‑DEPA, combine des caractéristiques de deux architectures établies : le cadre rigide et annulaire de DOTA et la structure plus flexible et ouverte d’un autre chélateur, le DTPA. Cette architecture hybride confère à 3p‑C‑DEPA dix « mains » de liaison fortes (atomes d’azote et d’oxygène) contre huit pour DOTA, et une cavité plus spacieuse qui peut mieux accueillir de gros ions métalliques. Des travaux expérimentaux antérieurs suggéraient que 3p‑C‑DEPA peut marquer rapidement des anticorps à des températures douces et maintenir des radionucléides à base de bismuth stables dans le sérum sanguin. L’étude actuelle franchit l’étape suivante en utilisant des calculs au niveau quantique pour comparer systématiquement la capacité de 3p‑C‑DEPA et de DOTA à lier le lutécium‑177, le bismuth‑213 et l’actinium‑225.
Regarder la poignée moléculaire
Parce qu’il est difficile de travailler directement avec des émetteurs alpha à courte durée de vie, les chercheurs ont eu recours à la théorie de la fonctionnelle de la densité (DFT), une méthode computationnelle puissante qui estime la répartition des électrons dans les molécules et la force des attractions entre atomes. Ils ont modélisé chaque ion métallique en milieu aqueux, puis son complexe avec DOTA ou 3p‑C‑DEPA, et calculé la variation d’énergie libre lorsque le métal passe de l’eau à la cage du chélateur. Cette variation d’énergie est traduite en « constante de stabilité » : plus la valeur est élevée, plus le chélateur retient fermement le métal. Deux approches DFT différentes et deux modèles de solvatation ont été utilisés pour reproduire des conditions de solution réalistes et vérifier que les tendances observées sont robustes et non des artefacts d’un seul protocole numérique.
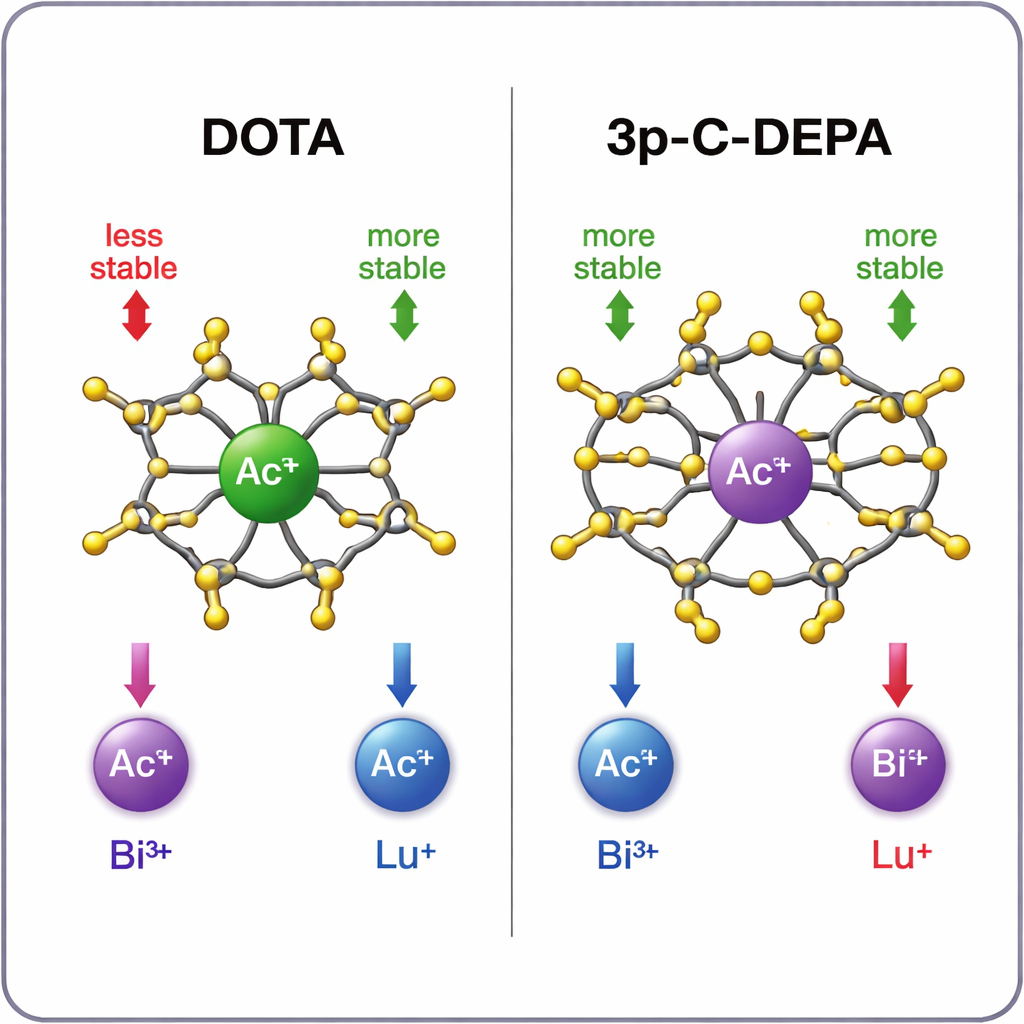
Quelle cage retient le mieux quel métal ?
Les simulations montrent un schéma clair. Pour le grand ion actinium, 3p‑C‑DEPA forme un complexe sensiblement plus stable que DOTA, grâce à sa cavité plus vaste et à son plus grand nombre de donneurs oxygène capables d’agripper le métal. Le bismuth‑213 est également bien accueilli par 3p‑C‑DEPA, profitant à la fois de sa taille et de son caractère accepteur d’électrons, qui s’accorde avec les groupes donneurs d’électrons du chélateur. En revanche, le plus petit lutécium‑177 s’adapte plus confortablement dans l’environnement plus serré et huit‑bras de DOTA. Dans 3p‑C‑DEPA, l’excès de groupes donneurs s’entasse autour du petit ion, générant des interactions répulsives qui semblent ralentir la marque et affaiblir légèrement le complexe final. Les tendances de stabilité calculées concordent bien avec les données expérimentales disponibles et les rendements de radio‑marquage, ce qui renforce la crédibilité des prédictions théoriques.
Ce que cela signifie pour les thérapies anticancéreuses à venir
Concrètement, l’étude suggère que DOTA n’est pas une cage universelle : elle fonctionne très bien pour des métaux plus petits comme le lutécium, mais est sous‑optimale pour des émetteurs alpha plus volumineux tels que l’actinium‑225. 3p‑C‑DEPA, en revanche, se comporte comme un support sur mesure pour ces ions plus gros, les tenant plus fermement et dans des conditions plus douces qui conviennent aux molécules de ciblage délicates comme les anticorps. Bien que des travaux expérimentaux et cliniques supplémentaires soient nécessaires, les calculs désignent 3p‑C‑DEPA comme une base prometteuse pour des thérapies alpha ciblées plus sûres et plus efficaces — élargissant potentiellement l’accès à des traitements anticancéreux très puissants capables d’éradiquer des tumeurs tout en épargnant les tissus sains environnants.
Citation: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Mots-clés: thérapie alpha ciblée, radiopharmaceutiques, conception de chélateurs, actinium-225, théorie de la fonctionnelle de la densité