Clear Sky Science · fr
Investigation expérimentale et corrélation thermodynamique de la solubilité de la chlordiazepoxide dans le CO₂ supercritique
Pourquoi dissoudre un médicament connu d’une manière nouvelle importe
Beaucoup de médicaments modernes sont efficaces mais difficiles à formuler de façon efficiente : ils peuvent mal se dissoudre, se dégrader lors de la fabrication ou nécessiter d’importantes quantités de solvants organiques. Cette étude porte sur la chlordiazepoxide, un anxiolytique utilisé depuis longtemps, et pose une question pratique aux implications larges : dans quelle mesure se dissout‑elle dans le dioxyde de carbone supercritique, un solvant plus propre et réglable qui pourrait aider à produire des particules médicamenteuses plus sûres et plus efficaces ?
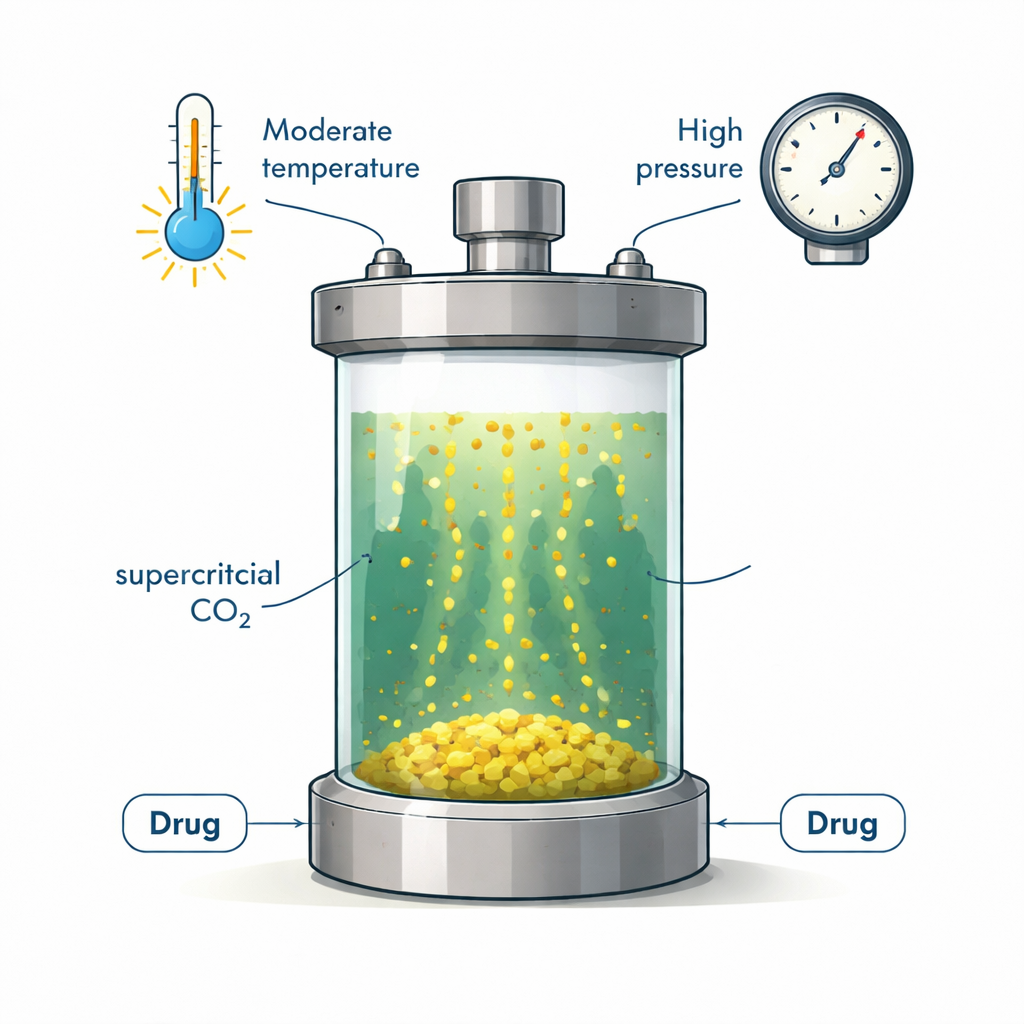
Un fluide « vert » qui se comporte à la fois comme un gaz et comme un liquide
Le dioxyde de carbone supercritique est du CO₂ porté au‑delà d’une certaine pression et température, jusqu’à ce qu’il ne soit plus ni un gaz ordinaire ni un liquide classique. Dans cet état, il s’écoule comme un gaz tout en ayant une densité proche de celle d’un liquide, ce qui lui permet de dissoudre de nombreuses substances. L’industrie l’utilise déjà pour décaféiner le café et extraire arômes et huiles. Pour la pharmacie, le CO₂ supercritique est attractif parce qu’il est non toxique, approuvé par les autorités, peu coûteux et facile à recycler. Il peut aider à produire de petites particules médicamenteuses uniformes et réduire le recours à des solvants organiques agressifs—à condition, bien sûr, que le médicament se dissolve suffisamment dans ce fluide.
Mesurer le comportement d’un anxiolytique sous pression
Les auteurs ont cherché à mesurer, pour la première fois, combien de chlordiazepoxide se dissout dans du CO₂ supercritique pur sur une plage de conditions pertinentes pour le traitement. Ils ont placé une poudre solide du médicament dans une cellule haute pression et fait circuler du CO₂ entre 12 et 30 mégapascals et entre 308 et 338 kelvins (environ 35–65 °C). Après avoir laissé le système atteindre l’équilibre, ils ont prélevé la phase CO₂, l’ont rapidement détendue dans un solvant, puis ont utilisé l’absorption ultraviolet‑visible pour déterminer la quantité de médicament dissoute. La solubilité globale variait d’environ 20 à 576 parties par million, correspondant à des fractions molaires comprises entre 0,0198×10⁻³ et 0,576×10⁻³, des valeurs comparables à celles d’autres médicaments modérément solubles dans le CO₂ supercritique.
Comment la pression et la température influent sur la solubilité
Les mesures ont révélé des tendances claires et intuitives. À température fixe, l’augmentation de la pression a toujours accru la solubilité. Une pression plus élevée rapproche les molécules de CO₂, rendant la phase supercritique plus dense et meilleure pour entourer et transporter les molécules du médicament. La température a un effet plus subtil. À faibles pressions, le réchauffement tend à diminuer la solubilité parce qu’il raréfie le CO₂ et réduit sa capacité de dissolution. Au‑delà d’une pression de croisement d’environ 19 mégapascals, la tendance s’inverse : une température plus élevée augmente la solubilité parce qu’elle favorise la libération du médicament de l’état solide vers le fluide. Cet équilibre entre la densité du fluide et la volatilité intrinsèque du médicament est caractéristique des systèmes supercritiques et est important pour choisir des conditions opératoires pratiques.
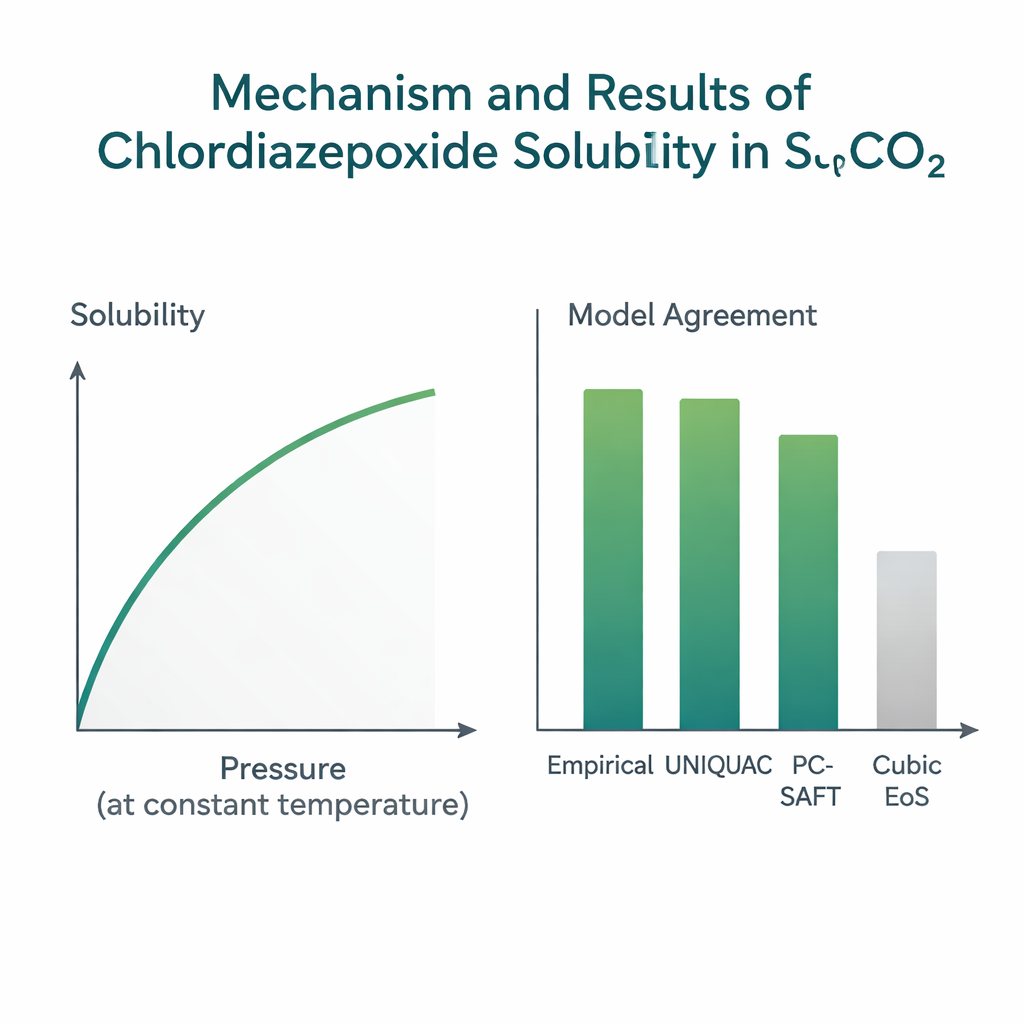
Apprendre aux modèles à prédire ce que voit le laboratoire
Parce que réaliser des expériences haute pression est lent et coûteux, les ingénieurs s’appuient sur des modèles mathématiques pour prédire la solubilité dans de nouvelles conditions ou pour des molécules apparentées. L’équipe a testé plusieurs familles de modèles avec leur nouvel ensemble de données. De simples formules empiriques « basées sur la densité », qui relient la solubilité directement à la densité du CO₂ et à la température en n’utilisant que quelques constantes d’ajustement, ont donné les meilleurs résultats. En particulier, la corrélation bien établie de Chrastil a ajusté les données avec un écart moyen d’environ 5 %, et d’autres formules similaires ont également bien performé. Une approche plus physiquement détaillée dite « liquide élargi », appelée UNIQUAC, qui tient compte de la taille et de la forme moléculaires ainsi que des énergies d’interaction, a obtenu une précision comparable, autour de 6 % d’écart. En revanche, les équations d’état cubiques couramment utilisées—formules généralistes pour le comportement des fluides—ont montré des écarts proches de 20 %, manquant des détails fins de l’interaction spécifique entre ce médicament et le CO₂.
Ce que cela signifie pour la fabrication pharmaceutique future
Concrètement, l’étude montre que la chlordiazepoxide se dissout dans le CO₂ supercritique à des conditions pertinentes technologiquement, et que son comportement peut être très bien rendu par des modèles relativement simples et bien choisis. Cela fournit une carte fiable pour concevoir des procédés plus verts visant à produire de nouvelles formes solides ou des nanoparticules du médicament, ce qui peut améliorer la stabilité ou l’absorption dans l’organisme. Plus largement, le travail apporte un jeu de données rare et soigneusement mesuré pour un médicament largement utilisé et montre quels outils de modélisation sont les plus fiables lors de la planification de procédés au CO₂ supercritique—des informations utiles pour orienter des fabrications plus propres et plus efficaces d’un grand nombre d’autres médicaments.
Citation: Saadati Ardestani, N., Noubigh, A., Esfandiari, N. et al. Experimental investigation and thermodynamic correlation of chlordiazepoxide solubility in supercritical CO₂. Sci Rep 16, 6552 (2026). https://doi.org/10.1038/s41598-026-35623-1
Mots-clés: dioxyde de carbone supercritique, solubilité des médicaments, chlordiazepoxide, procédés pharmaceutiques verts, modélisation thermodynamique