Clear Sky Science · fr
Une approche protéomique et protéomique redox pour comprendre l’hétérogénéité du SDRA
Pourquoi cela compte pour les patients en réanimation
Le syndrome de détresse respiratoire aiguë (SDRA) est une forme mortelle d’insuffisance pulmonaire qui peut affecter des personnes atteintes d’infections sévères, de traumatismes ou d’autres maladies critiques. Beaucoup de patients atteints de SDRA se ressemblent cliniquement, mais certains récupèrent tandis que d’autres non, et aucun médicament n’a été prouvé pour inverser spécifiquement le syndrome. Cette étude pose une question simple mais importante : si l’on examine de près les protéines et les réactions chimiques à l’intérieur des poumons et du sang des patients atteints de SDRA, peut-on révéler des « types » biologiques cachés de la maladie qui expliqueraient pourquoi l’évolution est si différente selon les patients ?
Regarder à l’intérieur des poumons, pas seulement dans le sang
Pour explorer cela, les chercheurs ont suivi 16 adultes en unité de soins intensifs atteints de SDRA et sous ventilation mécanique. Dans les trois premiers jours après le diagnostic, ils ont prélevé du sang et un échantillon spécifique appelé liquide de lavage bronchoalvéolaire (LBA), qui correspond à un lavage délicat des alvéoles pulmonaires. Ils ont répété ces prélèvements sur plusieurs jours lorsque cela était possible. À l’aide de spectrométrie de masse de pointe, ils ont mesuré des centaines de protéines dans chaque échantillon (protéomique) et, surtout, ont aussi évalué dans quelle mesure certaines de ces protéines étaient oxydées (protéomique redox), ce qui reflète leur dommage ou leur régulation par les espèces réactives de l’oxygène, sous-produits chimiquement agressifs de l’inflammation.
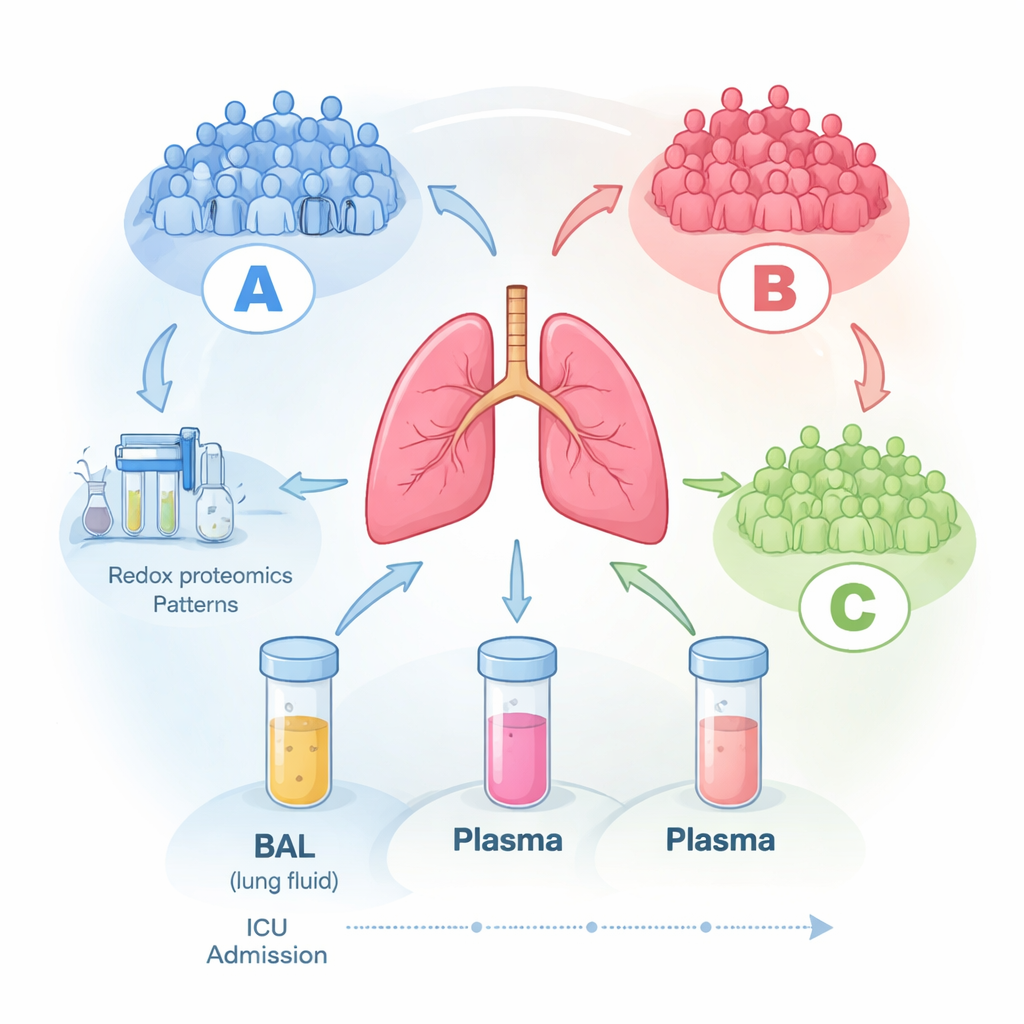
Trois groupes de patients cachés émergent
Lorsque l’équipe a laissé les données se regrouper d’elles-mêmes sans fournir d’informations cliniques au calcul, un schéma net est apparu dans les échantillons de liquide pulmonaire : trois groupes moléculaires distincts, étiquetés A, B et C. Les patients du groupe A avaient tendance à être plus gravement malades à l’inclusion, tandis que les groupes B et C présentaient une maladie plus bénigne. Fait frappant, ces signatures moléculaires sont restées largement stables pendant jusqu’à six jours en réanimation, ce qui suggère que chaque patient appartient à un profil biologique relativement constant plutôt qu’à des fluctuations aléatoires jour après jour. Les mesures cliniques habituelles au lit du malade — niveaux d’oxygène, durée de séjour ou scores généraux de gravité — ne suivaient pas bien ces regroupements moléculaires, laissant entendre que les outils cliniques classiques manquent des processus biologiques clés se déroulant dans les poumons.
Stress oxydatif et défenses de l’organisme
Un thème majeur ressortant des données est l’équilibre entre les espèces réactives de l’oxygène, dommageables, et les défenses antioxydantes de l’organisme. Dans le groupe A, le plus sévère, de nombreuses protéines pulmonaires impliquées dans la production d’énergie et l’entretien cellulaire étaient présentes à des niveaux plus faibles. Encore plus révélateur, des enzymes antioxydantes importantes telles que les péroxiredoxines, des protéines liées au glutathion, la thioredoxine et la catalase étaient significativement réduites. En revanche, les groupes B et en particulier C présentaient des niveaux plus élevés de ces protéines protectrices, suggérant que leurs poumons étaient mieux équipés pour détoxifier les oxydants nocifs et limiter les dégâts collatéraux de l’inflammation. Les schémas de l’état d’oxydation des protéines apportent une couche supplémentaire, montrant des sous-ensembles distincts de protéines oxydées enrichis chez les groupes les plus et les moins sévères.
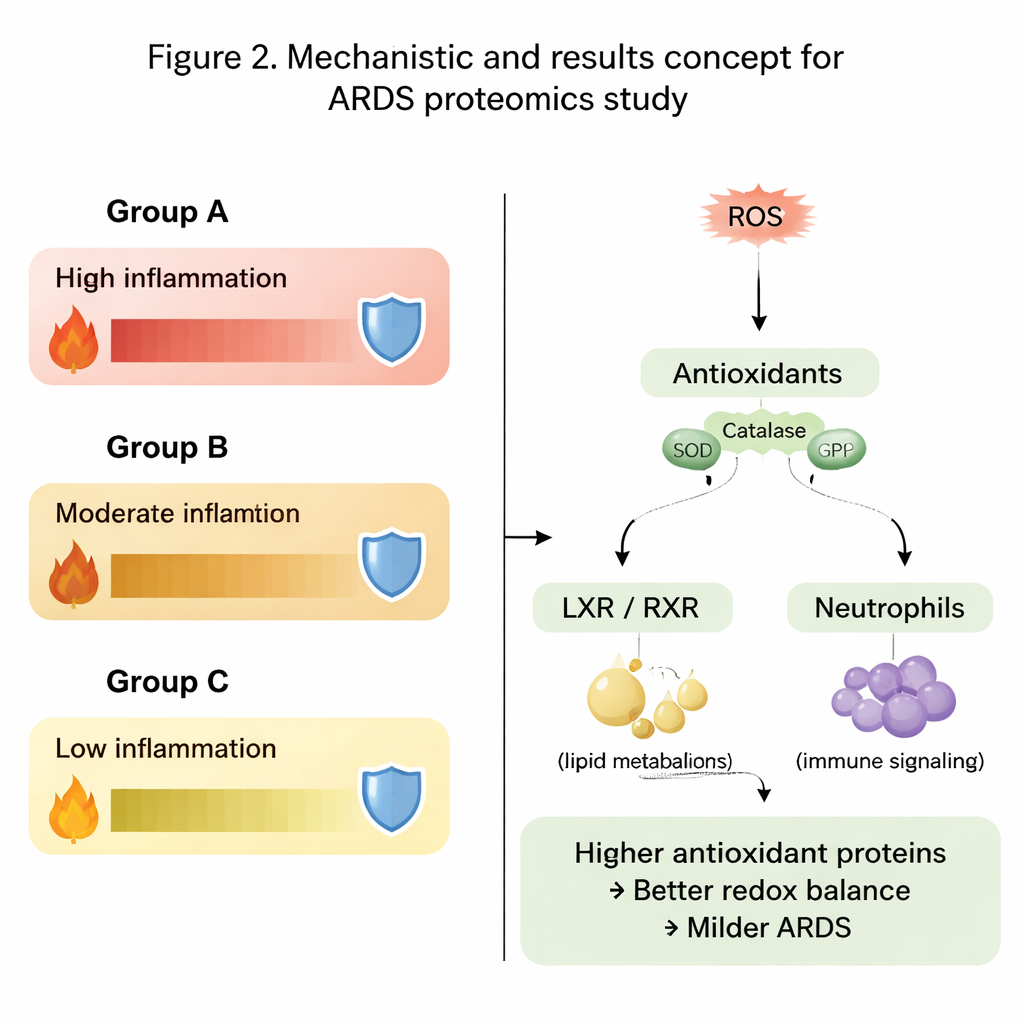
Voies de signalisation qui façonnent l’inflammation
Au-delà des protéines isolées, les auteurs ont examiné des voies biologiques entières. Ils ont constaté que les voies liées à l’inflammation, au métabolisme des lipides et au fonctionnement des cellules immunitaires se comportaient différemment selon les trois groupes. Des signaux liés à la voie du récepteur X du foie–récepteur X des rétinoïdes (LXR/RXR) et à une enzyme appelée DHCR24, qui participent ensemble à la régulation du métabolisme des lipides et des réponses immunitaires, étaient particulièrement remarquables. Dans le groupe le plus sévère, ces voies étaient prédictivement plus actives, associées à une diminution du signal de l’agent immunitaire interleukine-12. Parallèlement, les voies impliquant les espèces réactives de l’oxygène, leur détoxification, et l’activité des neutrophiles (globules blancs) montraient des schémas contrastés entre le liquide pulmonaire et le sang, soulignant que les processus locaux dans le poumon peuvent différer de ce qui est observé en circulation.
Ce que cela pourrait signifier pour les soins futurs
Cette petite étude exploratoire ne modifie pas les traitements aujourd’hui, et ses conclusions doivent être confirmées sur des cohortes beaucoup plus larges. Cependant, elle montre qu’en profilant finement les protéines et leur état redox directement dans le liquide pulmonaire — plutôt qu’en s’appuyant uniquement sur des tests sanguins ou des scores cliniques — on peut distinguer des sous-types biologiquement pertinents du SDRA. Ces sous-types diffèrent en termes de stress oxydatif, de capacité antioxydante, de métabolisme et de signalisation immunitaire, et ils restent relativement stables pendant les premiers jours critiques de la maladie. À l’avenir, ces empreintes moléculaires pourraient aider les cliniciens à classer les patients atteints de SDRA en groupes plus précis, à choisir des thérapies ciblées adaptées à chaque profil et à concevoir des essais cliniques plus intelligents avec une meilleure probabilité d’identifier des traitements réellement efficaces.
Citation: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Mots-clés: syndrome de détresse respiratoire aiguë, protéomique, stress oxydatif, lavage bronchoalvéolaire, soins intensifs