Clear Sky Science · fr
Le bévacizumab améliore la survie globale chez les patients nouvellement diagnostiqués de glioblastome avec une expression élevée de COX-2
Pourquoi cette étude sur le cancer du cerveau est importante
Le glioblastome est l’un des cancers cérébraux les plus mortels et, même avec la chirurgie, la radiothérapie et la chimiothérapie, la plupart des patients vivent moins de deux ans. Un médicament appelé bévacizumab peut réduire la taille des tumeurs et diminuer l’œdème cérébral, mais de larges essais ont suggéré qu’il n’améliore pas en moyenne la survie des patients. Cette étude pose une question plus précise : un test de laboratoire simple effectué sur la tumeur pourrait‑il identifier un sous‑groupe de patients qui vivent réellement plus longtemps avec le bévacizumab ?
Un examen approfondi d’une tumeur cérébrale tenace
Le glioblastome croît rapidement et est riche en vaisseaux sanguins anormaux qui alimentent la tumeur. Le traitement standard, souvent appelé protocole de Stupp, combine une chirurgie visant à retirer le plus de tumeur possible, suivie d’une radiothérapie et d’un comprimé de chimiothérapie nommé témozolomide. Le bévacizumab est un anticorps thérapeutique qui cible un signal de croissance utilisé pour former de nouveaux vaisseaux sanguins. Il est déjà approuvé dans de nombreux pays pour les glioblastomes récidivants, et au Japon il peut aussi être utilisé dès le départ. Cependant, comme de grands essais antérieurs ont montré que l’ajout de bévacizumab au traitement initial n’allongeait pas la survie globale chez le patient moyen, les cliniciens hésitent quant au moment — ou même à la nécessité — de l’utiliser précocement.
Un possible « interrupteur » marquant des tumeurs plus agressives
Les chercheurs se sont concentrés sur une molécule appelée COX‑2, une enzyme impliquée dans l’inflammation qui favorise aussi la formation de nouveaux vaisseaux, la dissémination tumorale et la résistance aux médicaments. Des taux élevés de COX‑2 dans le glioblastome ont depuis longtemps été associés à une survie plus faible, en faisant un marqueur d’une maladie particulièrement agressive. L’équipe a émis l’hypothèse que ces tumeurs à croissance rapide et très vascularisées pourraient être celles qui bénéficient le plus d’un médicament anti‑angiogénique comme le bévacizumab. Pour tester cela, ils ont examiné des prélèvements tumoraux de 50 adultes nouvellement diagnostiqués de glioblastome traités dans un même hôpital japonais entre 2012 et 2023. Tous les patients ont reçu la chirurgie standard, la radiothérapie et le témozolomide ; certains ont également reçu du bévacizumab dès le départ.
Diviser les patients selon un test de laboratoire tumoral
Les pathologistes ont mesuré la COX‑2 dans chaque tumeur à l’aide d’une méthode de coloration au microscope, attribuant un « score d’immunoréactivité » en fonction de l’intensité de la coloration et de la proportion de cellules positives. En utilisant la médiane du score comme seuil, les tumeurs ont été classées soit « COX‑2 élevé », soit « COX‑2 faible ». Dans un sous‑ensemble d’échantillons, ils ont aussi évalué l’activité génique de COX‑2 et ont constaté que les tumeurs fortement colorées présentaient généralement une activité génique plus élevée, ce qui appuie la fiabilité du test. Les patients ont ensuite été regroupés selon leur niveau de COX‑2 et selon qu’ils aient reçu le témozolomide seul ou le témozolomide plus bévacizumab, puis on a comparé leur délai de récidive tumorale et leur survie globale.
Qui bénéficie réellement du bévacizumab ?
En analysant l’ensemble des 50 patients, l’ajout du bévacizumab retardait la récidive tumorale mais n’allongeait pas clairement la survie, ce qui fait écho aux grands essais antérieurs. Le tableau a nettement changé, cependant, lorsque les patients ont été séparés selon le niveau de COX‑2. Parmi ceux dont la tumeur exprimait beaucoup de COX‑2, les patients ayant reçu du bévacizumab ont vécu une médiane de 25 mois, contre 18 mois pour ceux traités sans ce médicament, et leurs tumeurs sont restées sous contrôle plus longtemps. Des modèles statistiques ajustés sur l’âge, le statut fonctionnel et l’étendue de la résection ont encore montré que le bévacizumab était indépendamment associé à de meilleurs résultats dans ce groupe à COX‑2 élevé. En revanche, chez les patients dont les tumeurs avaient une faible expression de COX‑2, l’ajout de bévacizumab n’a amélioré ni le délai jusqu’à la progression ni la survie globale.
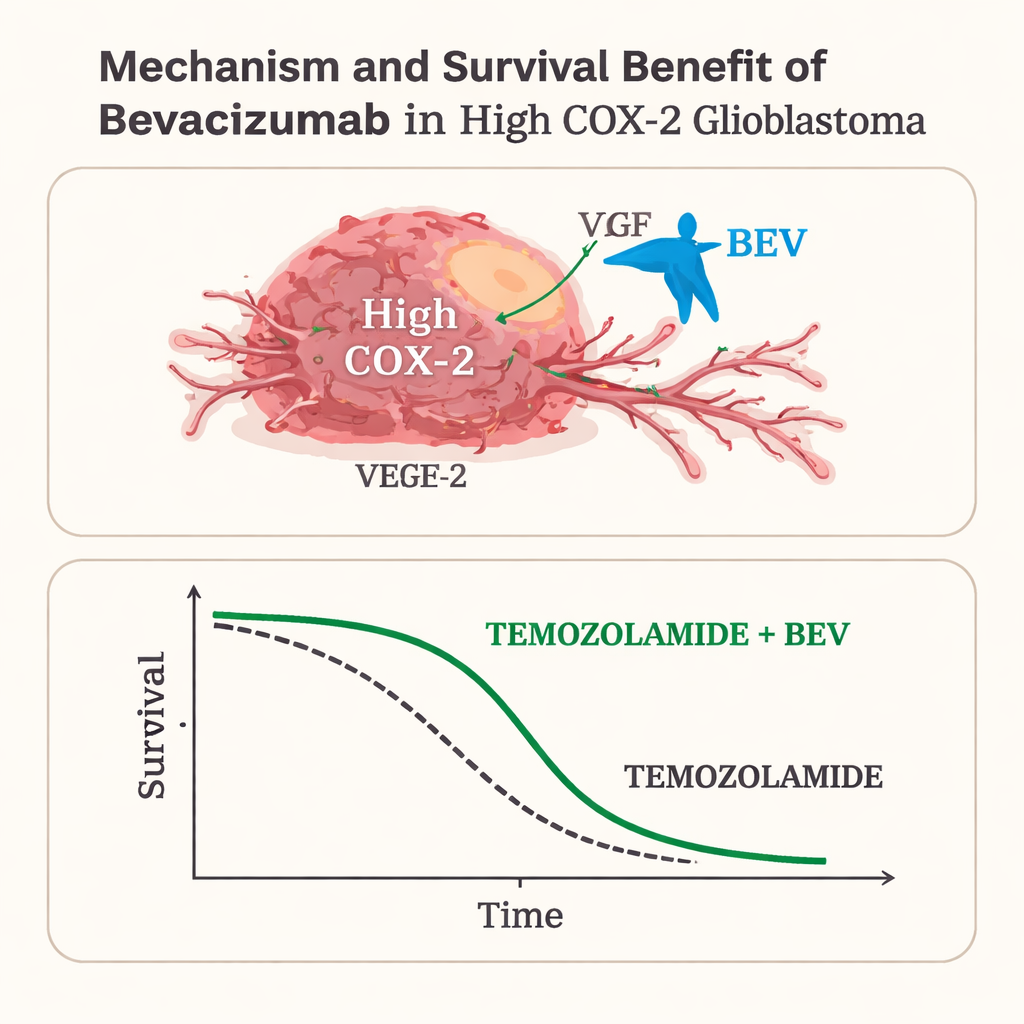
Ce que cela signifie pour les patients et les systèmes de santé
Pour les patients porteurs de tumeurs à COX‑2 élevé, le bévacizumab semblait annuler le désavantage pronostique habituellement associé à cette biologie agressive, portant leur espérance de vie proche de celle des patients à COX‑2 faible. Pour ceux à COX‑2 faible, le médicament ajoutait des coûts et des effets secondaires potentiels sans bénéfice clair. Comme il s’agissait d’une étude rétrospective relativement petite menée dans un seul centre, ces résultats doivent être confirmés par des essais prospectifs plus vastes. Néanmoins, le travail suggère qu’un test tumoral simple pourrait aider les médecins à cibler le bévacizumab vers les patients les plus susceptibles d’en tirer profit, tout en épargnant aux autres un traitement coûteux et contraignant qui pourrait ne pas prolonger leur vie.
Citation: Kesumayadi, I., Kambe, A., Kanda, H. et al. Bevacizumab enhances overall survival in newly diagnosed glioblastoma patients with high COX-2 expression. Sci Rep 16, 4974 (2026). https://doi.org/10.1038/s41598-026-35550-1
Mots-clés: glioblastome, bévacizumab, COX-2, traitement du cancer du cerveau, médecine personnalisée