Clear Sky Science · fr
Nanonaiguilles de Co3O4 croissant sur oxyde de graphène comme électrocatalyseur efficace pour une électrolyse de l’eau hybride via des réactions anodiques alternatives
Transformer les déchets de fruits en carburant du futur
L’hydrogène est souvent présenté comme un carburant propre pour l’avenir, mais sa production exige généralement beaucoup d’électricité. Cette étude montre comment quelque chose d’aussi banal que des écorces d’orange jetées peut contribuer à changer la donne. En transformant ce déchet en un matériau carboné spécial et en le combinant à un composé à base de cobalt, les chercheurs ont créé un catalyseur peu coûteux capable de produire de l’hydrogène en consommant beaucoup moins d’énergie que les méthodes conventionnelles de séparation de l’eau. Parallèlement, ils remplacent une étape inefficace de l’électrolyse par des réactions plus douces qui convertissent des substances problématiques en gaz inoffensifs.
Pourquoi la séparation traditionnelle de l’eau gaspille de l’énergie
Pour scinder l’eau en hydrogène et oxygène, un électrolyseur fait passer un courant électrique dans de l’eau contenant un sel dissous ou une base. D’un côté, le gaz hydrogène se forme facilement. De l’autre, l’oxygène est produit par une réaction lente et exigeante, car elle implique le transfert coordonné de quatre électrons. Cette étape de formation d’oxygène, appelée réaction anodique, oblige les ingénieurs à augmenter la tension, ce qui fait grimper la consommation d’énergie. Pire encore, l’oxygène est souvent simplement rejeté, ce qui signifie qu’une grande partie de l’énergie électrique injectée dans le système produit peu de valeur pratique.
Remplacer un poste gourmand en énergie par des réactions plus douces
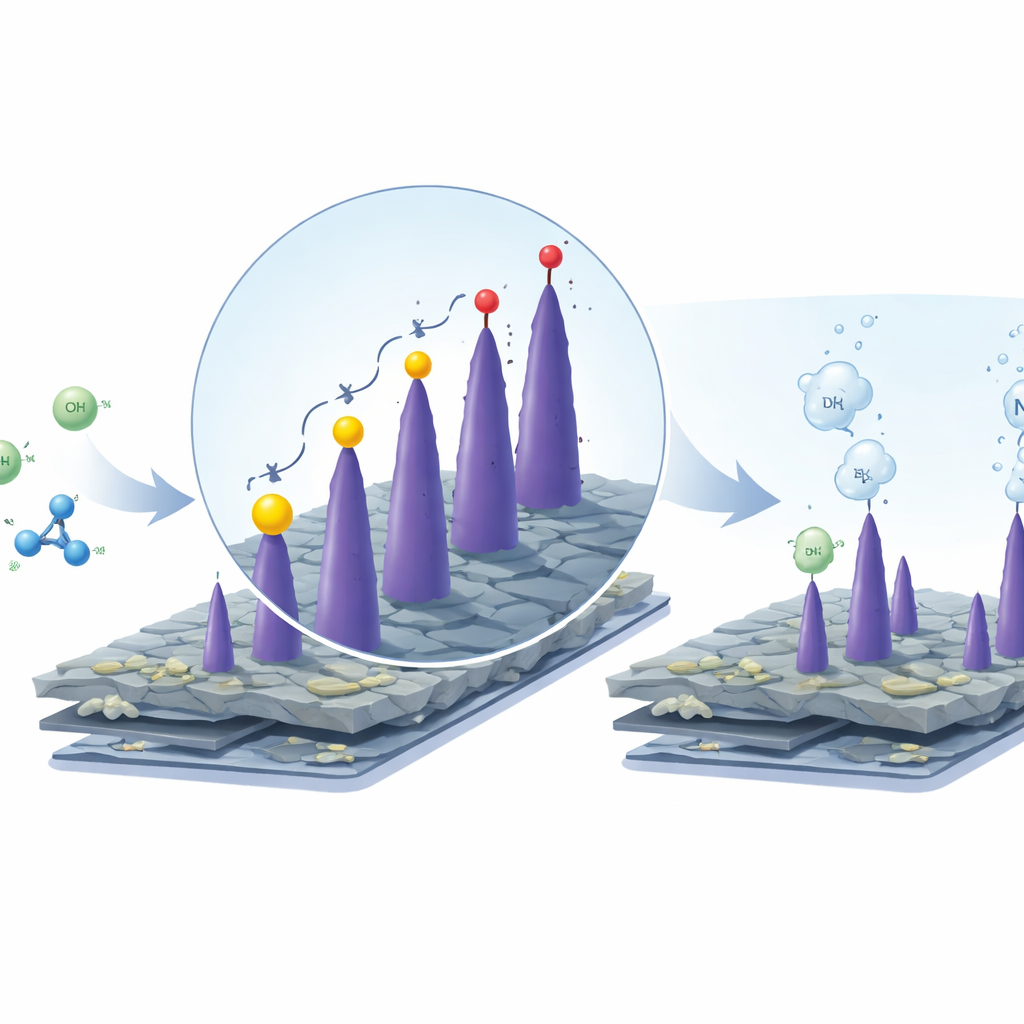
L’équipe a résolu ce goulot d’étranglement en repensant ce qui se passe du côté le plus énergivore de la cellule. Plutôt que de produire de l’oxygène à partir de l’eau, ils ont demandé : et si le système oxydait d’autres composés, plus faciles à traiter, tout en continuant à générer de l’hydrogène côté opposé ? Ils ont choisi deux composés riches en azote, l’urée et l’hydrazine, présents dans les effluents et certains procédés industriels. Lorsque ces molécules sont oxydées en solution alcaline, elles se décomposent en azote, eau et, dans le cas de l’urée, en dioxyde de carbone. Fait crucial, ces réactions démarrent à des tensions bien plus faibles que celle nécessaire pour produire de l’oxygène, ce qui permet de générer la même quantité d’hydrogène avec beaucoup moins d’énergie électrique.
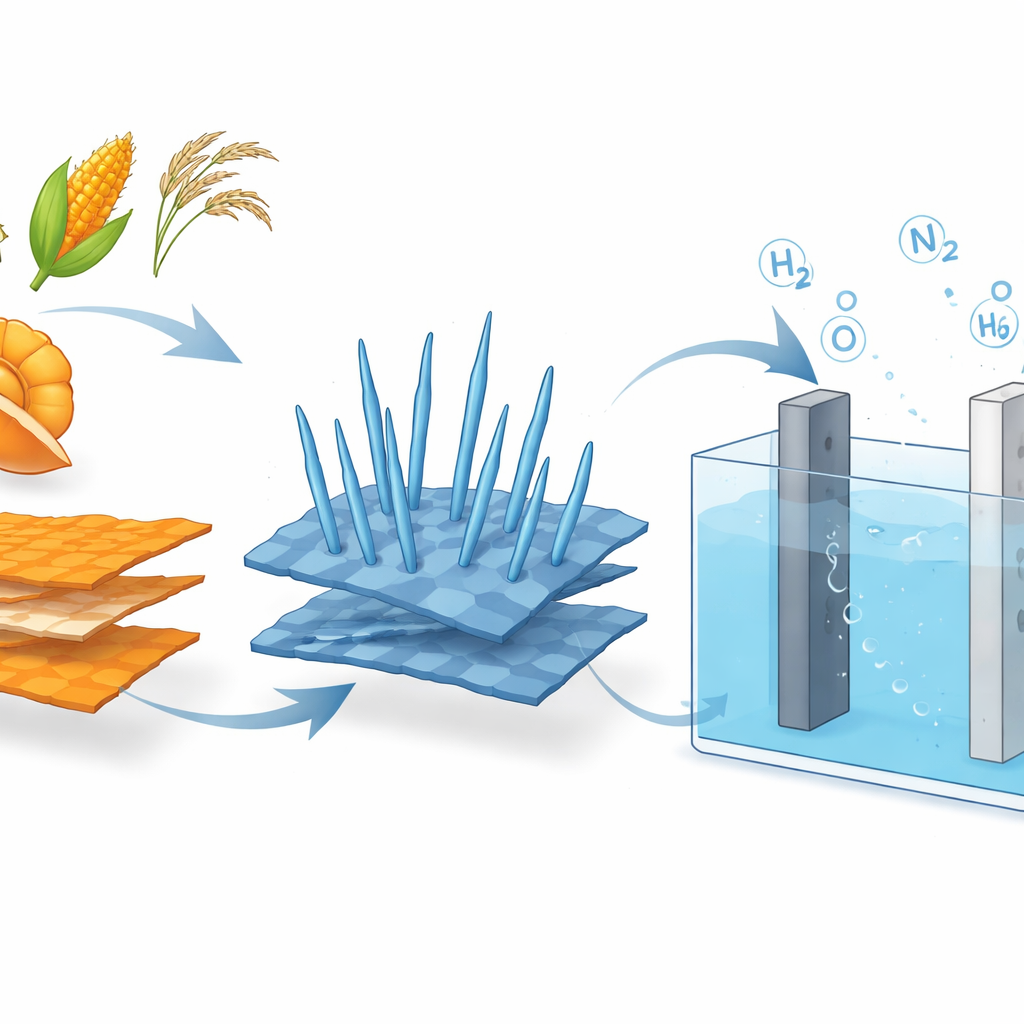
Des écorces d’orange aux électrodes intelligentes
Pour rendre cette approche praticable, les chercheurs avaient besoin d’un catalyseur bon marché, robuste et actif pour trois tâches : la production conventionnelle d’oxygène, l’oxydation de l’urée et celle de l’hydrazine. Ils ont commencé par convertir des écorces d’orange séchées en oxyde de graphène, un matériau carboné fin et conducteur, en utilisant un simple procédé de chauffage plutôt que des traitements chimiques agressifs. Sur ces feuillets, ils ont fait croître de petites « nanonaiguilles » d’oxyde de cobalt dans une enceinte sous pression. L’hybride obtenu — nanonaiguilles de Co3O4 sur oxyde de graphène — forme une surface rugueuse et spongieuse avec de nombreux sites réactifs exposés et des voies de conduction électronique efficaces. Les mesures ont montré que le support en graphène empêche l’agglomération des particules de cobalt et augmente fortement la surface effective et la conductivité électrique.
Comment le nouveau catalyseur réduit la facture énergétique
Testée en solution alcaline, la nouvelle électrode a atteint un courant de référence standard à des tensions nettement plus faibles que l’oxyde de cobalt seul. Pour la production conventionnelle d’oxygène, elle a affiché des performances comparables à certains catalyseurs commerciaux à base de métaux nobles. Lorsqu’on a ajouté de l’urée, la tension requise a encore chuté, et avec l’hydrazine l’amélioration a été spectaculaire : l’électrode n’a eu besoin que d’un petit supplément de tension au‑dessus du potentiel de référence pour maintenir le même courant. Dans une cellule complète à deux électrodes associée à une électrode standard à base de platine pour la production d’hydrogène, l’électrolyse assistée par l’hydrazine a généré de l’hydrogène à seulement 0,33 volt — environ 1,3 volt de moins que la séparation traditionnelle de l’eau dans les mêmes conditions. Le système est également resté stable pendant de nombreuses heures, la structure et la composition du catalyseur restant essentiellement inchangées.
Ce que cela signifie pour l’hydrogène propre
Pour un non-spécialiste, la conclusion est simple : en repensant à la fois le matériau de l’électrode et la réaction qui s’y déroule, les chercheurs ont montré qu’il est possible de produire de l’hydrogène en consommant beaucoup moins d’électricité et avec des ingrédients peu coûteux. Les déchets de fruits deviennent une armature carbonée haute performance ; les nanonaiguilles d’oxyde de cobalt fournissent des sites actifs ; et remplacer la formation d’oxygène par l’oxydation de l’urée ou de l’hydrazine réduit fortement la tension requise. Dans le cas de l’hydrazine, les produits secondaires sont principalement de l’azote et de l’eau, évitant des émissions carbone supplémentaires. Bien que des travaux complémentaires soient nécessaires pour gérer l’approvisionnement chimique et la sécurité à l’échelle industrielle, cette stratégie d’électrolyse hybride ouvre la voie à une production d’hydrogène plus propre et moins coûteuse, tout en valorisant les flux de déchets et la biomasse renouvelable.
Citation: Rahamathulla, N., Murthy, A.P. Co3O4 nanoneedles grown on graphene oxide as an efficient electrocatalyst for hybrid water electrolysis through alternative anodic oxidation reactions. Sci Rep 16, 8452 (2026). https://doi.org/10.1038/s41598-026-35522-5
Mots-clés: production d’hydrogène, électrolyse de l’eau, oxyde de graphène, oxydation de l’hydrazine, catalyseurs issus de la biomasse