Clear Sky Science · fr
Génomique comparative de Pseudomonas aeruginosa multirésistante et non sensible au colistine révèle des lignées émergentes en Thaïlande
Pourquoi ce germe hospitalier concerne tout le monde
Pseudomonas aeruginosa est un germe hospitalier qui s’attaque aux personnes au plus faible de leur état — après une opération, sous assistance respiratoire, ou en cas de brûlures graves ou de maladie pulmonaire. Pendant des années, les médecins se sont appuyés sur un antibiotique puissant « de dernier recours » nommé colistine lorsque les autres médicaments échouent. Cette étude examine des souches de Pseudomonas provenant d’hôpitaux à travers la Thaïlande qui ne répondent plus à la colistine ni à de nombreux autres antibiotiques. En lisant l’ADN complet de ces bactéries, les chercheurs montrent comment de nouvelles lignées fortement résistantes aux médicaments se propagent, et pourquoi cela devrait inquiéter patients, cliniciens et systèmes de santé dans le monde entier.
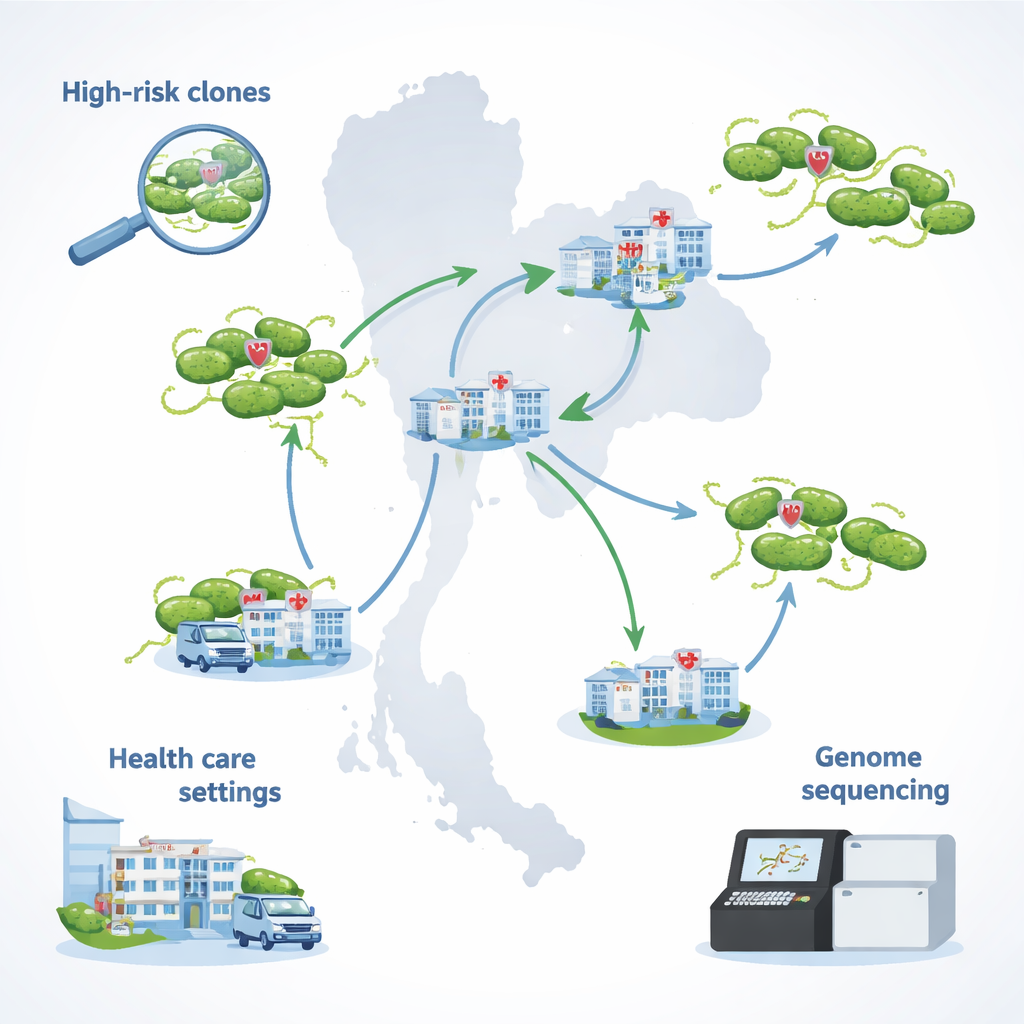
Suivre une infection difficile à traiter à travers la Thaïlande
L’équipe s’est concentrée sur 29 souches de Pseudomonas aeruginosa collectées en 2021–2022 dans des hôpitaux participant au programme national thaïlandais de surveillance de la résistance aux antibiotiques. Toutes ces souches étaient multirésistantes : elles résistaient à plusieurs grandes classes d’antibiotiques, y compris des médicaments habituellement utilisés pour les infections graves. Surtout, elles n’étaient pas pleinement sensibles à la colistine, le médicament souvent réservé aux cas menaçant le pronostic vital. La plupart des échantillons provenaient d’urine, mais d’autres venaient de sang, d’expectoration, de pus et de liquides de drains chirurgicaux — reflétant les nombreuses formes d’infections que ce germe peut causer chez les patients hospitalisés.
Lire les « empreintes » génétiques des bactéries
En combinant séquençage d’ADN à lectures courtes et longues, les chercheurs ont assemblé des génomes de haute qualité pour chaque souche. Ils ont ensuite comparé ces génomes pour classer les bactéries en familles génétiques, appelées types de séquence. Neuf types de séquence distincts ont été identifiés, révélant une diversité importante. L’un d’eux, nommé ST5340, n’avait jamais été décrit auparavant. Il s’est avéré proche d’un clone international à haut risque connu, ST357, ne différant que par un seul des sept gènes constitutifs standard. Malgré cette parenté étroite, ST5340 se distinguait parce que chacune de ses isolats résistait à tous les antibiotiques testés, le qualifiant de lignée particulièrement préoccupante.
Lignées à haut risque émergentes et leur propagation
En alignant de minuscules différences d’ADN appelées polymorphismes mononucléotidiques sur 108 génomes de Pseudomonas thaïlandais (les 29 nouveaux plus 79 issus de bases de données publiques), l’équipe a construit un arbre généalogique des souches circulant dans le pays. Cette analyse a mis en évidence plusieurs clusters dominants centrés sur ST5340, ST357, ST654 et ST235 — des lignées déjà connues, ou désormais émergentes, comme « à haut risque » car elles résistent fréquemment à plusieurs médicaments et provoquent des flambées en milieu hospitalier. ST5340 en particulier est apparu dans plusieurs provinces et régions, ce qui suggère une propagation large plutôt qu’une présence limitée à un seul hôpital. D’autres clones mondiaux à haut risque, tels que ST654 et ST235, étaient également présents, tandis que certaines lignées d’importance globale comme ST244 étaient absentes, probablement parce que l’étude n’incluait que des souches non sensibles à la colistine.
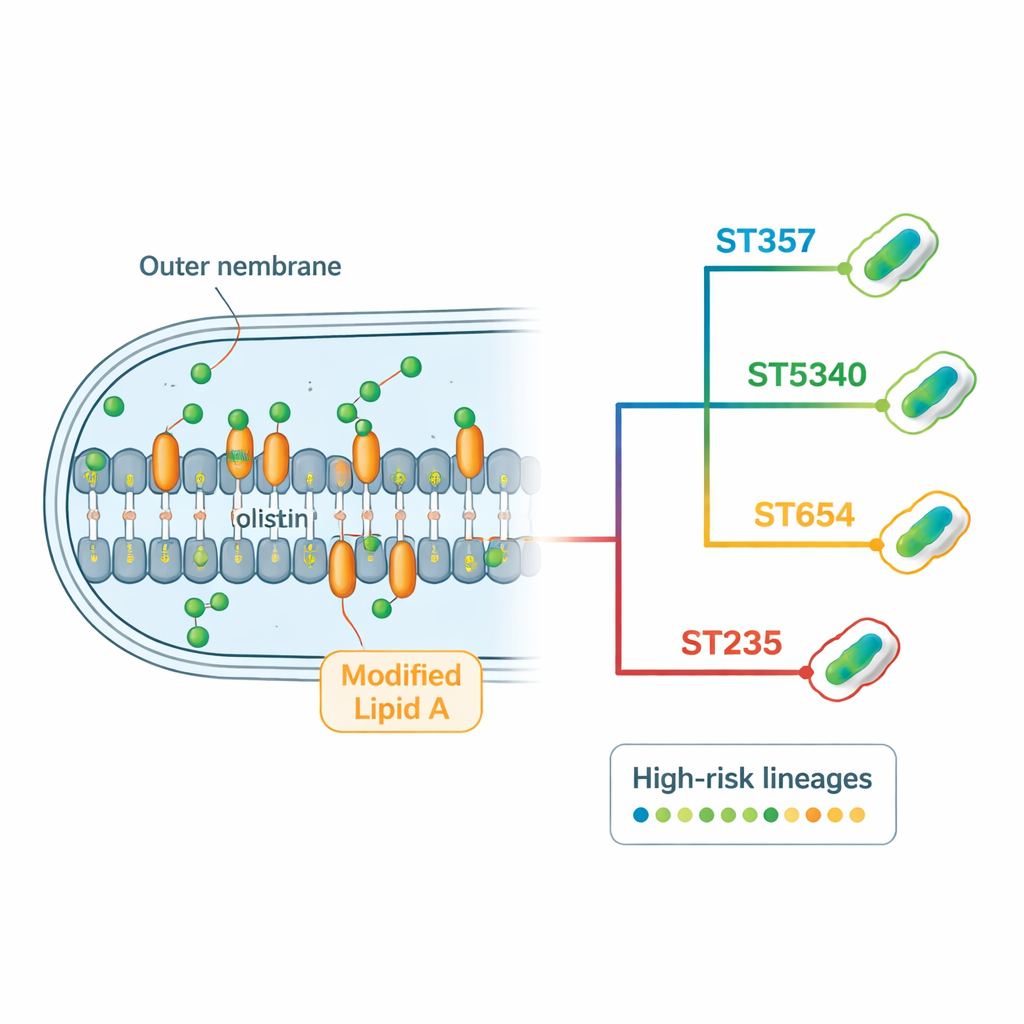
Comment ces bactéries contournent les antibiotiques
L’analyse génomique a révélé un « résistome » dense — l’ensemble complet des gènes et mutations de résistance portés par chaque souche. De nombreux isolats codaient plusieurs types de bêta‑lactamases, des enzymes qui dégradent des antibiotiques courants tels que pénicillines, céphalosporines et carbapénèmes. Le gène de carbapénèmase blaNDM‑1, associé à la résistance à certains des médicaments hospitaliers les plus puissants, est apparu dans presque toutes les souches, parfois en copies multiples. Les bactéries portaient également des gènes modifiant chimiquement les aminoglycosides, ainsi que des pompes d’efflux puissantes qui expulsent les médicaments hors de la cellule. Concernant la colistine spécifiquement, l’équipe n’a pas trouvé de gènes de résistance mobiles mais a identifié des altérations récurrentes dans des gènes chromosomiques impliqués dans la membrane externe et sa régulation. Certaines mutations dans des protéines régulatrices et des enzymes de synthèse de la lipid A étaient fortement associées à la résistance à la colistine, en particulier dans les lignées dominantes ST357 et ST5340.
Ce que cela signifie pour les patients et les hôpitaux
En combinant la surveillance nationale et le séquençage génomique moderne, cette étude montre que les hôpitaux thaïlandais font face à une menace croissante d’un clone à haut risque nouvellement identifié, ST5340, aux côtés de souches problématiques mondiales établies. Ces bactéries sont non seulement résistantes à la colistine mais aussi à de nombreux autres médicaments clés, réduisant fortement les options thérapeutiques lorsque des patients développent des infections graves. Pour le grand public, le message est clair : la résistance aux antibiotiques n’est pas un risque abstrait pour l’avenir mais une réalité actuelle qui peut affecter directement les issues des interventions chirurgicales, des traitements en soins intensifs et des thérapies contre le cancer. Les auteurs soutiennent que la poursuite de la surveillance génomique, un renforcement du contrôle des infections et une utilisation prudente des antibiotiques sont urgemment nécessaires pour empêcher ces lignées hautement résistantes de se répandre davantage et de devenir plus difficiles à contenir.
Citation: Wankaew, N., Arigul, T., Kruasuwan, W. et al. Comparative genomics of colistin-nonsusceptible multidrug-resistant Pseudomonas aeruginosa reveals emerging lineages in Thailand. Sci Rep 16, 5968 (2026). https://doi.org/10.1038/s41598-026-35520-7
Mots-clés: Pseudomonas aeruginosa, résistance aux antibiotiques, colistine, surveillance génomique, infections hospitalières