Clear Sky Science · fr
Le hsa-miR-339-5p exosomal plasmatique est associé à NOD-like receptor family CARD domain-containing 5 dans l’insuffisance cardiaque à fraction d’éjection réduite
Pourquoi de petites molécules dans le sang peuvent révéler un cœur en difficulté
L’insuffisance cardiaque à fraction d’éjection réduite (ICFEr) est une affection fréquente dans laquelle le cœur ne parvient plus à pomper suffisamment de sang pour répondre aux besoins de l’organisme. Les médecins la découvrent généralement seulement après que des dommages importants se sont déjà produits. Cette étude examine si des messages microscopiques circulant dans le sang — de petites molécules d’ARN emballées dans de minuscules bulles appelées exosomes — peuvent signaler un problème plus tôt et éclairer la manière dont le cœur se raidit et se cicatrise progressivement.
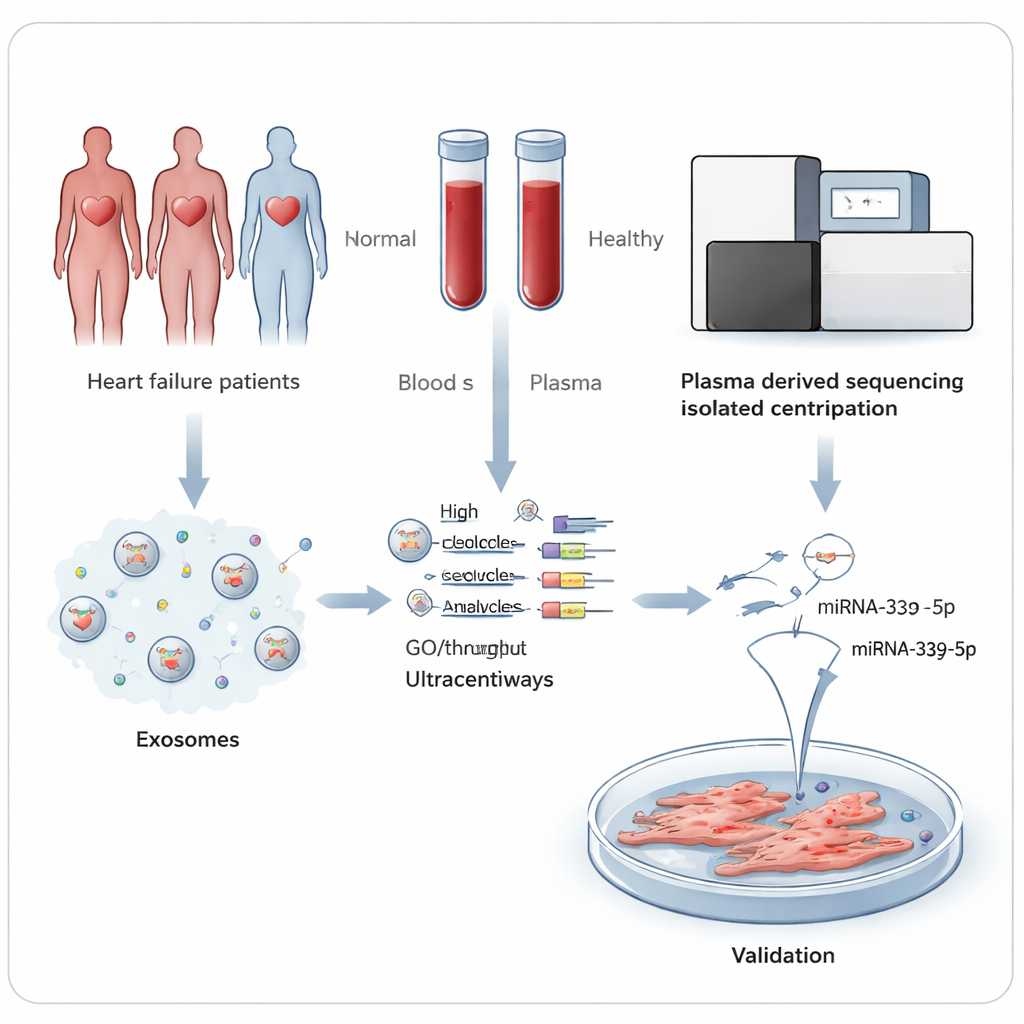
Messages cachés transportés dans la circulation sanguine
Notre sang contient d’innombrables exosomes, des sacs de taille nanométrique libérés par les cellules qui transportent des protéines et du matériel génétique d’une cellule à une autre. Parmi leur cargaison se trouvent des microARN, de courts brins qui ajustent finement l’activation ou la répression des gènes. Comme les exosomes protègent ces microARN de la dégradation, ils peuvent être mesurés de manière fiable à partir d’un simple échantillon sanguin. Les chercheurs ont émis l’hypothèse que si le cœur défaillant ou les tissus associés libèrent un mélange de microARN différent de celui d’un cœur sain, ces signatures pourraient servir d’indicateurs d’alerte et révéler les processus à l’origine de la maladie.
Comparer des patients au cœur affaibli à des volontaires sains
L’équipe a prélevé du sang chez 45 personnes atteintes d’ICFEr et 45 volontaires sains comparables dans un hôpital de Hefei, en Chine. À partir du plasma sanguin, ils ont isolé soigneusement les exosomes et confirmé leur taille et leur forme par microscopie électronique et par des instruments de suivi des particules. Dans une première étape, ils ont séquencé les petits ARN contenus dans les exosomes d’un sous‑groupe de cinq patients et cinq témoins. Cette approche haut débit a détecté des centaines de microARN connus et a mis en évidence 27 microARN dont les niveaux différaient nettement entre les deux groupes — 10 augmentés et 17 diminués chez les personnes souffrant d’insuffisance cardiaque.
Se concentrer sur un signal marquant
Pour tester la robustesse de ces changements, les scientifiques ont ensuite utilisé une méthode PCR très sensible pour mesurer six microARN prometteurs chez les 40 patients et 40 témoins restants. Plusieurs signaux se sont confirmés, mais un en particulier — appelé hsa‑miR‑339‑5p — s’est démarqué. Il était systématiquement plus élevé chez les patients atteints d’ICFEr et, analysé comme marqueur diagnostique, distinguait le mieux ces patients des individus sains. Des analyses informatiques de voies biologiques ont suggéré que ce microARN pourrait cibler un gène nommé NLRC5, lequel influence à son tour une voie centrale de croissance et de survie cellulaire connue sous le nom de voie PI3K/Akt, déjà impliquée dans l’épaississement du muscle cardiaque et la formation de cicatrices.
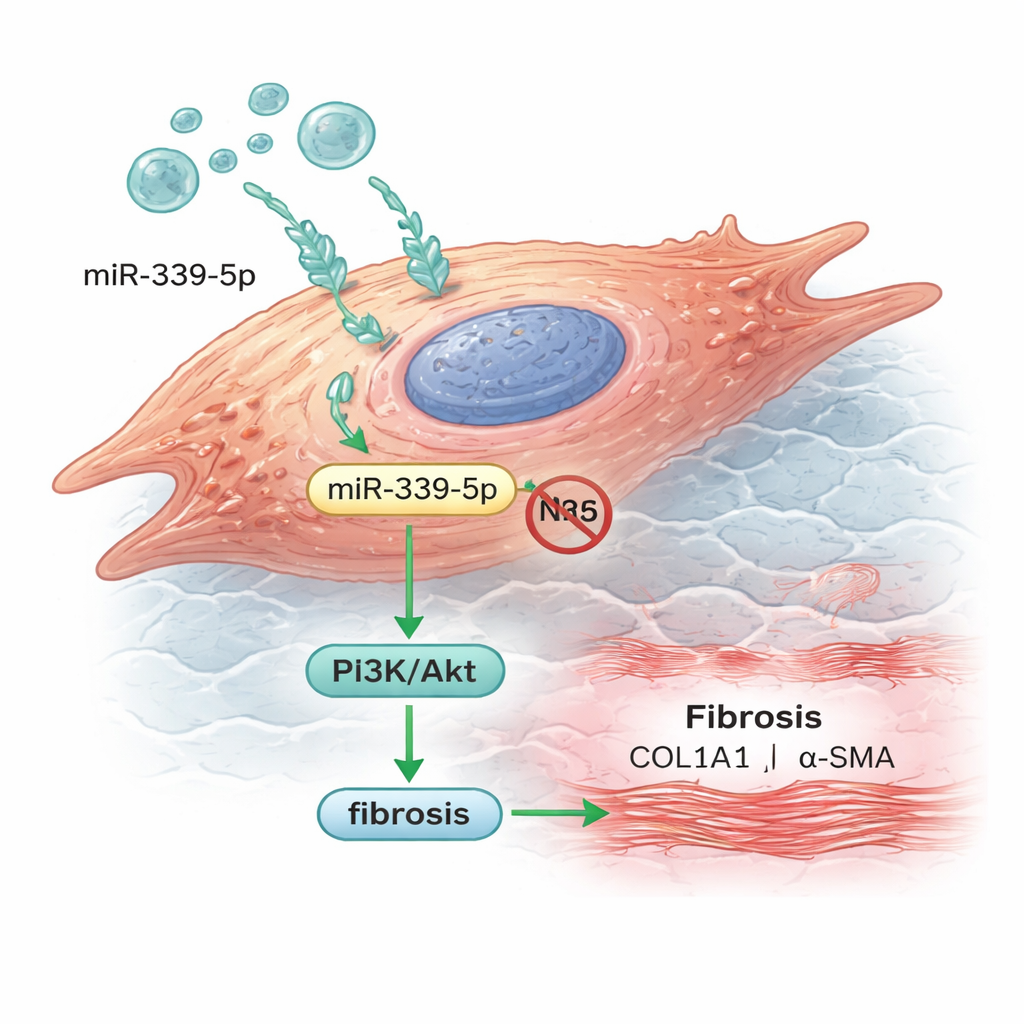
Du marqueur sanguin au moteur de la fibrose
Les chercheurs sont ensuite passés à des cellules de type cardiaque cultivées en laboratoire pour observer le comportement de ce microARN dans les tissus. Ils ont montré que les exosomes provenant des patients étaient facilement absorbés par des cardiomyocytes humains, délivrant le miR‑339‑5p à l’intérieur des cellules. Lorsqu’ils ont artificiellement augmenté miR‑339‑5p, les niveaux de NLRC5 ont diminué et la voie PI3K/Akt est devenue plus active. Parallèlement, les cellules ont produit davantage de collagène et une protéine appelée actine alpha muscle lisse — deux marqueurs caractéristiques d’un tissu fibreux et raidi plutôt que d’un muscle sain et souple. Lorsque miR‑339‑5p a été bloqué, ces changements ont été inversés, suggérant que ce microARN unique contribue à pousser les cellules cardiaques vers un état propice à la formation de cicatrices.
Ce que cela signifie pour les patients et les soins futurs
En cartographiant cette chaîne d’événements — de l’élévation de miR‑339‑5p dans les exosomes plasmatiques à la réduction de NLRC5, à l’activation du signal PI3K/Akt et à l’augmentation des protéines de cicatrisation — l’étude relie un marqueur sanguin mesurable à un mécanisme plausible de dommage à l’intérieur du cœur. Pour les patients, cela ouvre la possibilité qu’un test sanguin de routine puisse un jour aider à détecter plus tôt le remodelage nuisible que ne le permettent les examens d’imagerie et les marqueurs biologiques actuels. Cela suggère également que des médicaments visant à réduire miR‑339‑5p, ou à restaurer l’activité de NLRC5, pourraient ralentir le raidissement et la fibrose qui aggravent progressivement l’insuffisance cardiaque. Bien que des études plus larges et de plus longue durée soient nécessaires, ces minuscules messagers ARN pourraient offrir à la fois un témoin d’alerte sur le tableau de bord et une nouvelle cible sous le capot.
Citation: Cheng, D., Hu, J., Zhao, M. et al. Plasma exosomal hsa-miR-339-5p is associated with NOD-like receptor family CARD domain-containing 5 in heart failure with reduced ejection fraction. Sci Rep 16, 5690 (2026). https://doi.org/10.1038/s41598-026-35519-0
Mots-clés: insuffisance cardiaque, exosomes, microARN, fibrose, biomarqueurs