Clear Sky Science · fr
SHP2 favorise l’ostéosarcome en régulant la voie STAT3/TET3/HOXB2
Pourquoi cette étude sur le cancer des os est importante
L’ostéosarcome est le cancer primitif de l’os le plus fréquent chez les enfants et les adolescents, et malgré la chimiothérapie moderne et la chirurgie, la survie des patients atteints de maladie avancée ou récurrente a à peine progressé depuis plusieurs décennies. Cette étude explore le fonctionnement interne des cellules d’ostéosarcome pour identifier quelles molécules jouent le rôle de « commutateurs maîtres » favorisant la croissance tumorale, la dissémination et la résistance au traitement. En dévoilant une voie de contrôle clé centrée sur une protéine nommée SHP2, ce travail met en évidence de nouvelles cibles médicamenteuses susceptibles, un jour, de rendre les thérapies contre l’ostéosarcome plus efficaces et plus précises.
Suivre les indices dans l’activité génique tumorale
Les chercheurs ont d’abord abordé l’ostéosarcome comme un problème de données. Ils ont exploité des jeux de données publics d’expression génique comparant des échantillons tumoraux et du tissu osseux normal, puis utilisé des outils statistiques pour repérer les gènes systématiquement surexprimés ou sous‑exprimés dans le cancer. Des centaines de gènes différaient, et nombre d’entre eux se regroupaient dans des voies cancéreuses bien connues qui pilotent la prolifération, la survie et la mobilité cellulaire. Parmi eux, une protéine, SHP2, s’est distinguée comme un nœud fortement lié à plusieurs autres : le facteur de signalisation STAT3, l’enzyme de modification de l’ADN TET3 et le régulateur du développement HOXB2. Cela suggérait que ces molécules pourraient former une chaîne connectée aidant les cellules d’ostéosarcome à adopter un comportement agressif. 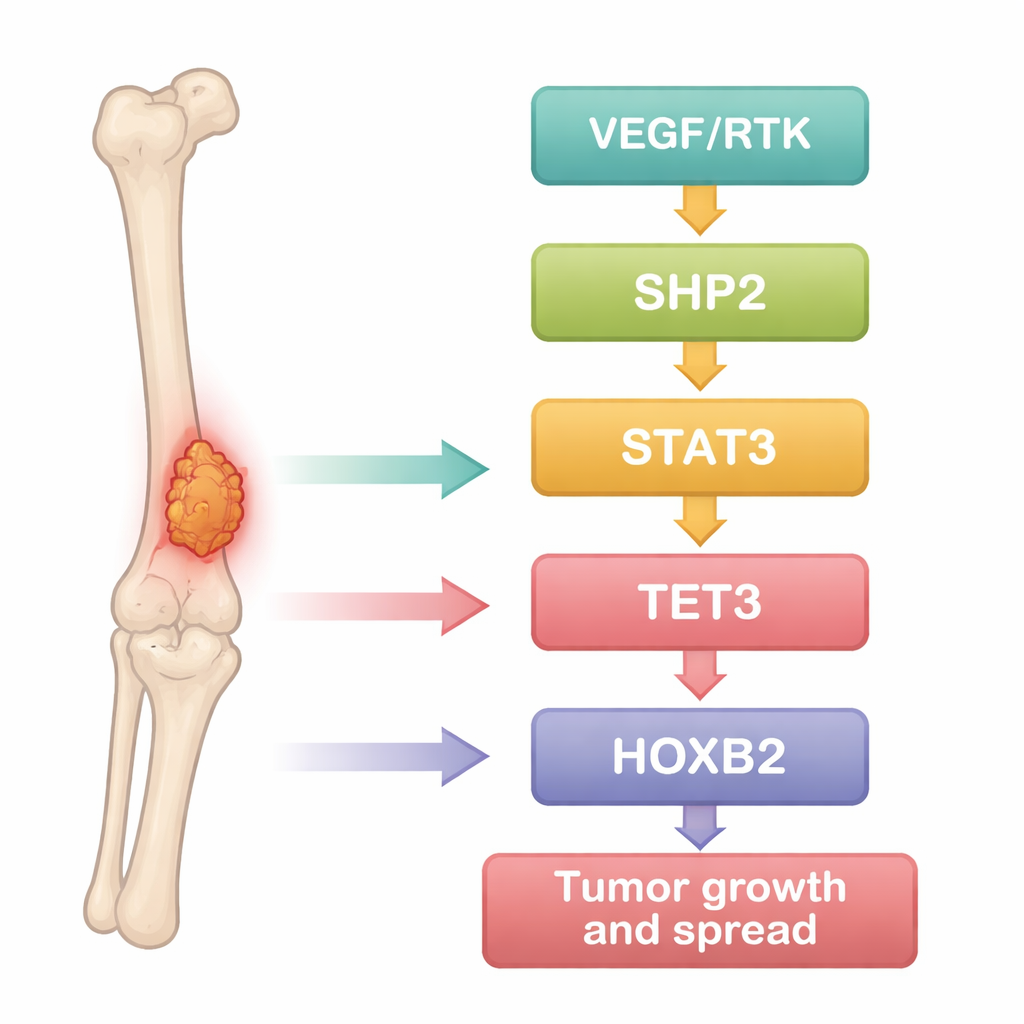
Tester le rôle de SHP2 dans les cellules cancéreuses
Pour aller au‑delà des corrélations, l’équipe a modifié des lignées humaines d’ostéosarcome (143B et MG63) pour réduire ou augmenter l’expression de SHP2. Lorsqu’ils ont réduit SHP2, la capacité des cellules à se multiplier, à migrer sur une surface et à envahir à travers une membrane a nettement diminué. Les niveaux des protéines STAT3, TET3 et HOXB2, ainsi que des marqueurs associés au cancer tels que c‑Myc, NANOG et NUSAP1, ont également baissé. Lorsque STAT3 a été réactivé ou que HOXB2 a été surexprimé, beaucoup de ces effets ont été inversés, indiquant que SHP2 se situe en amont d’une chaîne qui aboutit finalement à des gènes contrôlant la division cellulaire, les caractéristiques de type cellule‑souche et la machinerie de la mitose.
Construire une voie cancéreuse étape par étape
En recoupant les expériences, les auteurs proposent un modèle séquentiel. Dans l’environnement tumoral, des niveaux élevés de facteur de croissance de l’endothélium vasculaire (VEGF) stimulent des récepteurs tyrosine kinases (RTK) à la surface cellulaire. Ceux‑ci activent à leur tour SHP2 à l’intérieur de la cellule. SHP2 actif active STAT3, un facteur de transcription qui migre vers le noyau et favorise l’augmentation de la production de TET3. TET3 modifie alors les marques chimiques sur l’ADN, en particulier en éliminant des groupes méthyle dans la région du gène HOXB2. Cette déméthylation agit comme la levée d’un frein, permettant une expression accrue de HOXB2. HOXB2, un gène normalement impliqué dans le développement, stimule alors l’activité de c‑Myc, NANOG et NUSAP1, qui ensemble alimentent la prolifération tumorale incontrôlée, renforcent le comportement invasif et soutiennent des caractéristiques associées aux métastases.
Du milieu de culture aux animaux vivants
Pour vérifier si cette voie avait un rôle dans des tumeurs entières, les scientifiques ont implanté sous la peau de souris des cellules d’ostéosarcome modifiées. Les tumeurs formées à partir de cellules surexprimant SHP2 étaient plus grosses et plus lourdes que les tumeurs témoins. Lorsque TET3 a été silencé dans ces cellules riches en SHP2, la croissance tumorale a ralenti et les niveaux de HOXB2 ont chuté, bien que SHP2 et STAT3 demeurent actifs. La réintroduction de HOXB2 a restauré la vigueur tumorale. Partout, les mesures des niveaux protéiques dans les tissus tumoraux reflétaient les observations en culture cellulaire, renforçant l’idée que SHP2, STAT3, TET3 et HOXB2 forment un axe connecté qui pousse l’ostéosarcome vers un comportement plus malin. 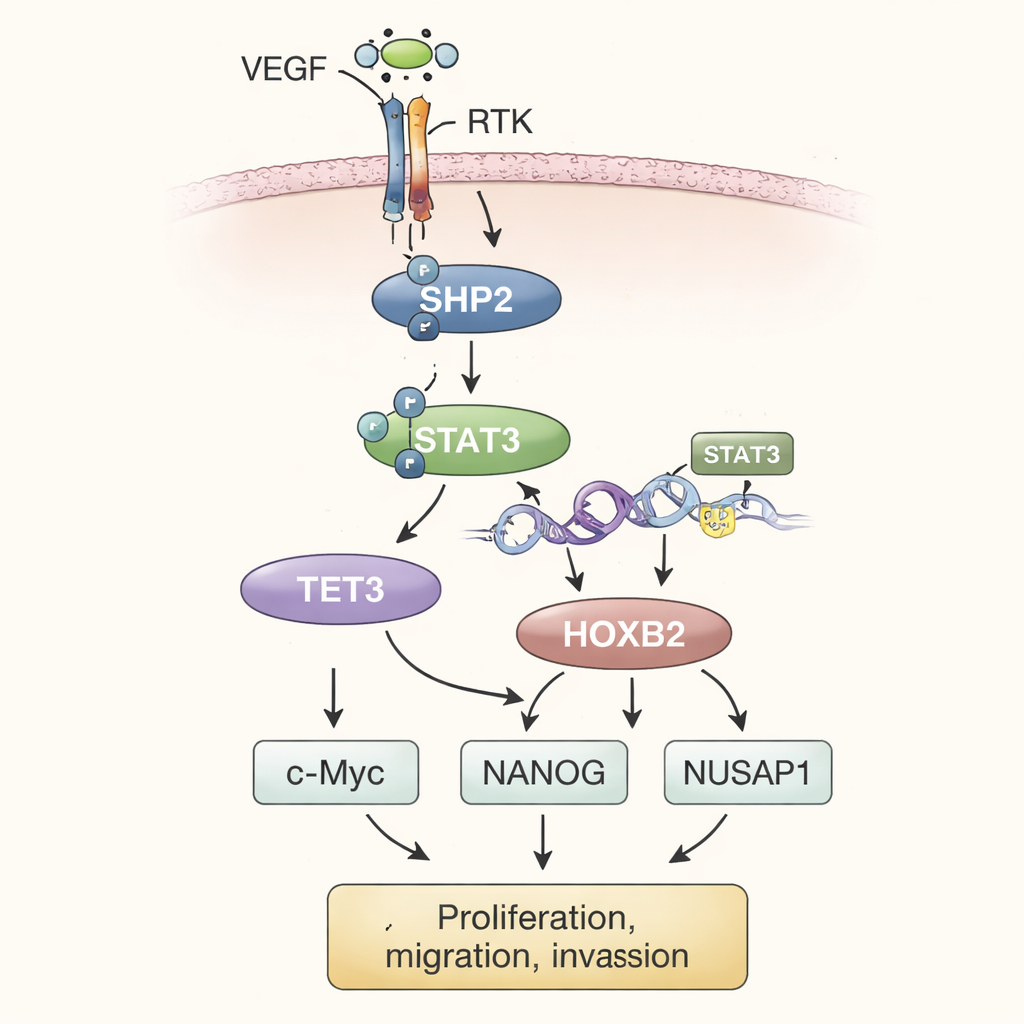
Ce que cela signifie pour les traitements futurs
Pour un lecteur non spécialiste, la conclusion est que les chercheurs ont tracé une chaîne de signal claire — du VEGF et de ses récepteurs de surface, via SHP2 et STAT3, jusqu’à TET3, HOXB2 et plusieurs gènes puissants de croissance — qui aide à expliquer pourquoi l’ostéosarcome peut croître rapidement et se disséminer tôt. Étant donné que SHP2 et STAT3 sont des enzymes susceptibles, en principe, d’être bloquées par des médicaments de petite taille, et que TET3 et HOXB2 marquent des étapes plus en aval du même parcours, cette voie offre plusieurs points d’intervention potentiels pour de futures thérapies. Bien que cette étude ait été réalisée sur des lignées cellulaires et des souris, elle fournit une carte détaillée que les développeurs de médicaments peuvent utiliser pour concevoir des traitements combinés visant à couper les commutateurs centraux de la tumeur plutôt que de n’attaquer que ses conséquences finales.
Citation: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Mots-clés: ostéosarcome, SHP2, voie STAT3, signalisation tumorale, thérapie ciblée