Clear Sky Science · fr
Conception et évaluation par immunoinformatique d’un vaccin multi-épitope contre Vibrio fluvialis
Pourquoi un nouveau vaccin compte pour les amateurs de fruits de mer
Vibrio fluvialis est un cousin moins connu des bactéries responsables du choléra, qui vit dans les eaux côtières chaudes et peut contaminer les fruits de mer et l’eau potable. Il provoque des diarrhées sévères et des infections intestinales et devient plus fréquent avec le réchauffement des océans et la perte d’efficacité des antibiotiques. Pourtant, il n’existe actuellement aucun vaccin pour les humains. Cette étude utilise des méthodes informatiques avancées pour concevoir un nouveau type de vaccin expérimental, composé de petits fragments choisis du germe, dans le but à long terme de protéger les personnes exposées via l’alimentation, l’eau ou des inondations liées au climat.

D’une menace cachée à une cible claire
Vibrio fluvialis a souvent été confondu avec d’autres espèces de Vibrio, ce qui signifie que son rôle dans les maladies d’origine alimentaire a probablement été sous-estimé. Des épidémies ont été liées à des fruits de mer contaminés et à de l’eau polluée, et des tempêtes et inondations récentes ont poussé ces bactéries à l’intérieur des terres, rendant des personnes malades loin des côtes. Beaucoup de patients nécessitent des soins hospitaliers, et un nombre inquiétant de souches résistent désormais à plusieurs antibiotiques. Comme la surface du microbe ressemble à celle d’espèces apparentées, les médecins peuvent mal diagnostiquer les infections, retardant ainsi le traitement approprié. Tout cela crée un fort besoin de prévention plutôt que de ne compter que sur les médicaments.
Concevoir un vaccin dans un ordinateur
Plutôt que de cultiver des bactéries entières en laboratoire, les chercheurs se sont tournés vers l’« immunoinformatique » — l’utilisation de logiciels pour prédire quelles petites portions de Vibrio fluvialis sont les plus susceptibles d’être reconnues et attaquées par le système immunitaire humain. Ils se sont concentrés sur deux protéines de membrane situées à la surface de la bactérie et importantes pour sa survie et sa capacité à provoquer la maladie. À partir de ces protéines, l’équipe a extrait dix courts segments, appelés épitopes, qui peuvent être reconnus à la fois par les lymphocytes T et B, les principaux acteurs de notre défense immunitaire. Ils ont ensuite assemblé ces morceaux en une seule chaîne de 246 acides aminés, ajoutant de courts segments d’espacement pour que le système immunitaire puisse traiter chaque fragment correctement, ainsi qu’un fragment adjuvant pour renforcer la réponse globale.
Vérifier la puissance, la sécurité et la portée mondiale
Une fois le vaccin virtuel construit, l’équipe a effectué une série de tests entièrement in silico, c’est‑à‑dire sur des ordinateurs plutôt que sur des animaux ou des humains. Des programmes ont prédit que le construit combiné serait fortement « visible » pour le système immunitaire tout en ayant peu de chances de déclencher des allergies ou une toxicité. Les épitopes choisis correspondaient à des variantes courantes de gènes immunitaires dans le monde entier, ce qui suggère qu’environ 99,97 % de la population mondiale devrait être capable de répondre, y compris les populations de régions fortement touchées comme l’Asie du Sud et de l’Est. La protéine vaccin semblait aussi stable, suffisamment hydrophile pour bien se dissoudre, et compatible avec une production efficace dans des bactéries de laboratoire standard, rendant la fabrication éventuelle plus pratique.
Comment le vaccin pourrait déclencher la protection
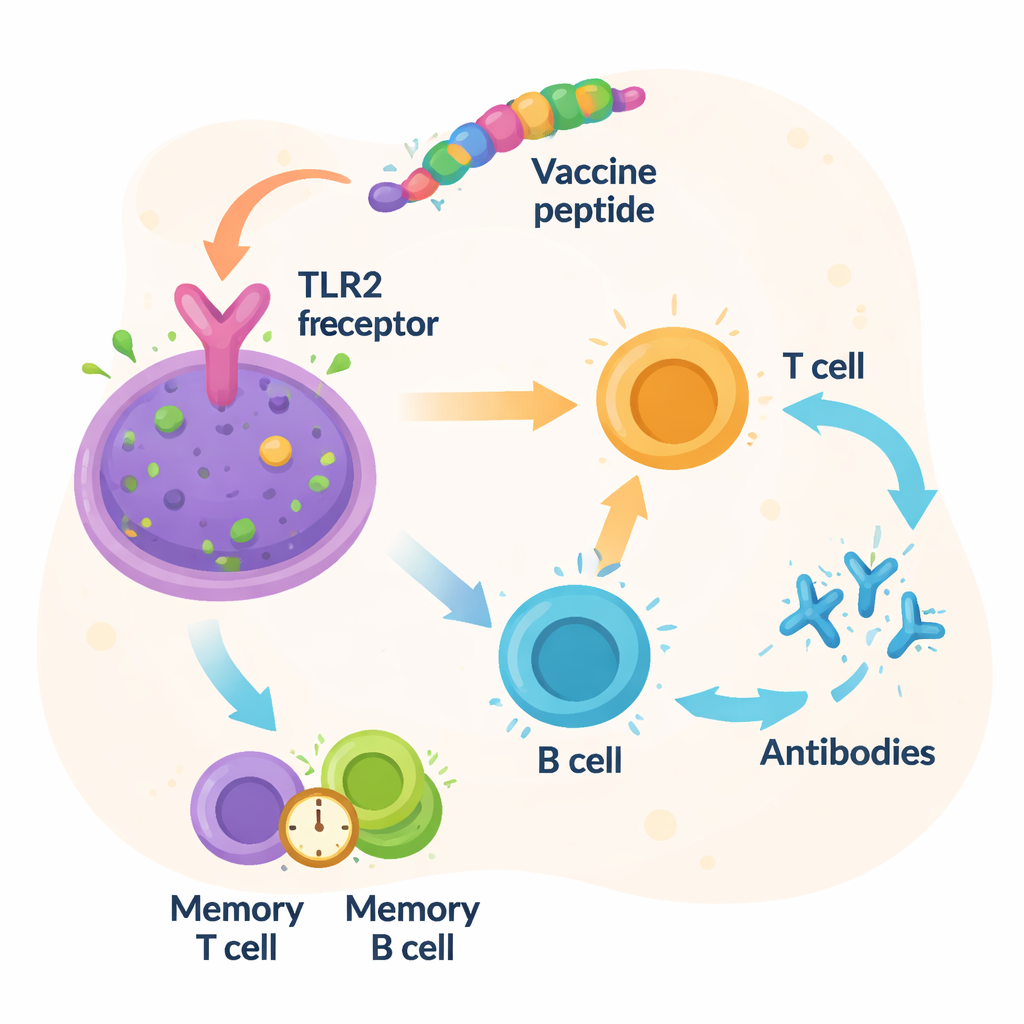
Les chercheurs se sont ensuite demandé si la protéine conçue interagirait de manière plausible avec un véritable capteur immunitaire. En utilisant des outils modernes de prédiction de structures, ils ont construit un modèle tridimensionnel du vaccin puis simulé son ancrage sur le récepteur Toll‑like 2 (TLR2), une molécule présente sur les cellules immunitaires qui détecte des composants bactériens. Le docking informatique a suggéré un ajustement serré entre le vaccin et TLR2, soutenu par de nombreux contacts moléculaires stabilisants. Des simulations de mouvement longues et détaillées sur 100 nanosecondes ont indiqué que le couple vaccin‑récepteur restait stable et compact au fil du temps. Des simulations supplémentaires du système immunitaire ont prédit de fortes vagues d’anticorps et d’activité des lymphocytes T, ainsi que la formation de cellules mémoire qui, en principe, pourraient fournir une protection durable contre Vibrio fluvialis.
Du plan numérique à la protection dans le monde réel
Concrètement, ce travail propose un « plan » numérique pour un futur vaccin contre Vibrio fluvialis construit à partir des fragments les plus importants de la bactérie, organisés pour être largement efficaces et potentiellement plus sûrs que des vaccins à cellule entière. L’étude montre que ce construit devrait être reconnaissable par la plupart des systèmes immunitaires humains, se lier efficacement à un capteur immunitaire clé et être fabriquable avec des outils standard. Toutefois, tous ces résultats proviennent de modèles informatiques. Les prochaines étapes nécessiteront la production du vaccin en laboratoire, des tests sur des cellules et des animaux, puis éventuellement des essais humains pour confirmer qu’il protège réellement contre l’infection sans causer de dommages. Si ces essais réussissent, de tels vaccins multi-épitope pourraient devenir de nouveaux outils puissants contre les bactéries d’origine alimentaire dans un monde qui se réchauffe et se densifie.
Citation: Naveed, M., Husnain, M., Aziz, T. et al. Immunoinformatics-based design and evaluation of a multi-epitope vaccine against Vibrio fluvialis. Sci Rep 16, 4100 (2026). https://doi.org/10.1038/s41598-026-35434-4
Mots-clés: Vibrio fluvialis, vaccin multi-épitope, infection d’origine alimentaire, immunoinformatique, résistance aux antibiotiques