Clear Sky Science · fr
Développement d’un système de criblage global pour détecter les interactions protéine–protéine par complémentation de luminescence chez la levure de division
Éclairer la vie cachée des protéines
Chaque battement de cœur, pensée et respiration de notre corps dépend des associations de protéines à l’intérieur des cellules. Ces petites collaborations, appelées interactions protéine–protéine, contrôlent tout, de la lecture des gènes à la réponse cellulaire au stress. Pourtant, beaucoup de ces associations sont fugitives ou fragiles, ce qui les rend difficiles à détecter avec les outils actuels. Cette étude décrit un nouveau système de criblage « basé sur la lumière », très sensible, développé dans un organisme modèle simple — la levure de division — pour révéler simultanément des milliers de ces connexions protéiques cachées.
Pourquoi les partenariats protéiques sont si difficiles à voir
Les protéines travaillent rarement seules. Elles se lient à différents partenaires à différents moments, parfois seulement pour un instant, et leur comportement peut être modifié par des modifications chimiques ou par leur localisation dans la cellule. Les méthodes traditionnelles d’étude de ces interactions extraient souvent les protéines de leur environnement naturel ou s’appuient sur des artifices génétiques qui ne détectent pas toutes les associations. En conséquence, les cartographies existantes des interactions cellulaires sont incomplètes. Les auteurs ont cherché à améliorer cette image en créant un système plus flexible et plus sensible capable d’examiner presque toutes les protéines de la levure de division dans des cellules vivantes.
Transformer le contact en lumière
Au cœur de la nouvelle approche se trouve une enzyme scindée qui émet de la lumière. Une partie, appelée LgBiT, est fixée à une protéine « appât » que les chercheurs veulent étudier. L’autre partie, SmBiT, est fixée à de nombreux partenaires « proies » possibles, un par souche de levure. Pris séparément, ces deux fragments d’enzyme interagissent à peine. Mais lorsque protéines appât et proie se lient dans la cellule, les deux fragments s’assemblent, reconstituant une enzyme active qui brille en présence d’un substrat chimique. En mesurant la quantité de lumière produite par chaque souche de levure, l’équipe peut déterminer quelles protéines se rencontrent réellement dans la cellule et l’intensité de leur interaction. Pour éviter de manquer des partenaires parce que l’étiquette gêne la fonction normale, la protéine appât existe en deux versions, avec LgBiT fixé à l’une ou l’autre extrémité, augmentant fortement les chances qu’au moins une orientation fonctionne. 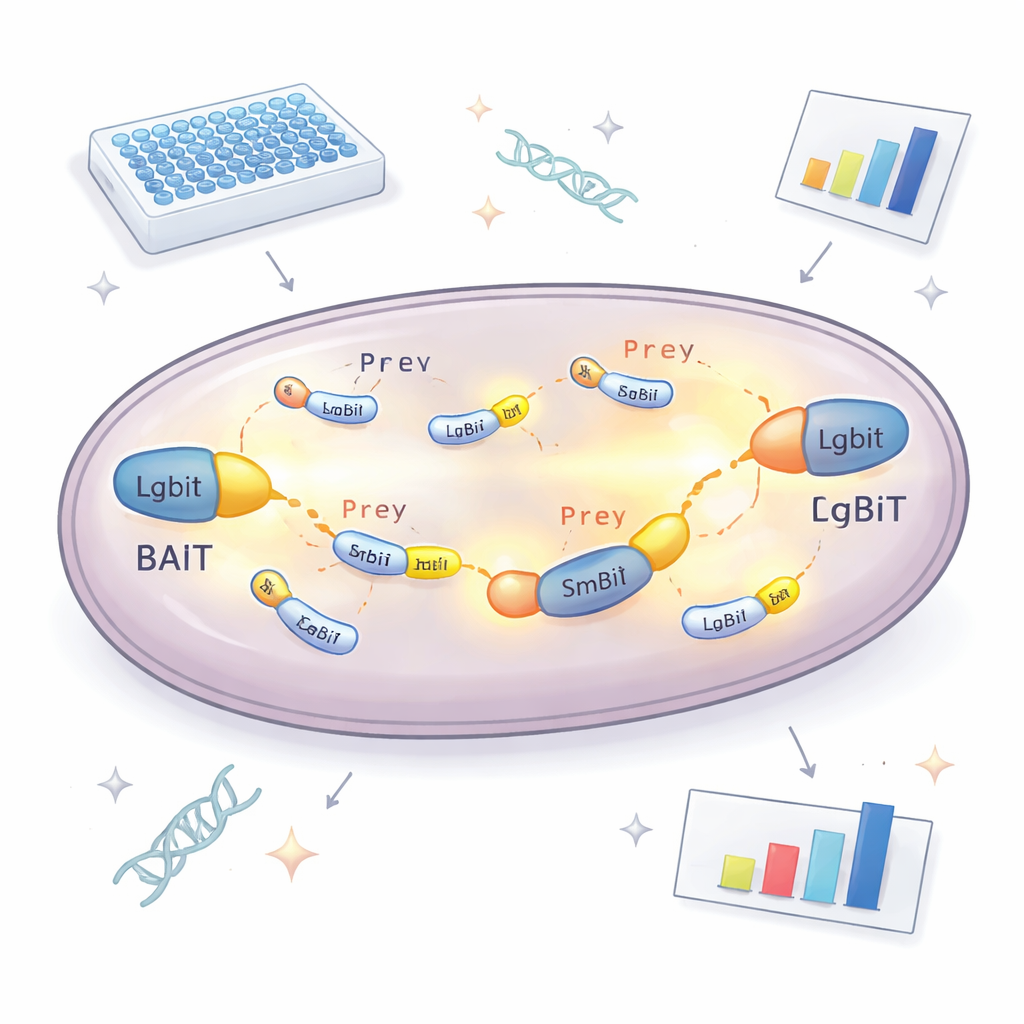
Conception d’une bibliothèque et d’un système de souches de levure
La mise au point de cette plateforme a nécessité plus qu’une enzyme ingénieuse. Les chercheurs ont également dû introduire des milliers de protéines proies dans la levure de façon contrôlée et en copie unique. Ils ont conçu un vecteur d’ADN spécifique pour les protéines proies qui s’insère à un emplacement défini du génome de la levure et porte un marqueur fluorescent rouge. L’intensité de ce signal rouge reflète le nombre de copies insérées, permettant à l’équipe de sélectionner facilement des colonies contenant exactement une copie, ce qui est essentiel pour des comparaisons fiables. Ils ont aussi créé des vecteurs dédiés pour les appâts plaçant LgBiT au début ou à la fin de la protéine appât, séparé par des linkers flexibles pour que la protéine puisse se replier et bouger normalement. Des souches de levure soigneusement conçues ont ensuite été construites pour accueillir simultanément deux constructions d’appât et une construction de proie, en utilisant des marqueurs nutritionnels pour s’assurer que seules les cellules correctement combinées survivent.
Éprouver le système
Pour vérifier si leur conception améliorait réellement la détection, les scientifiques ont d’abord examiné des protéines ayant des partenaires bien connus. Ils ont confirmé que l’intensité du signal dépendait fortement de l’endroit où l’étiquette luminescente était attachée : certaines interactions n’apparaissaient que lorsque LgBiT était à une extrémité de l’appât et pas à l’autre. L’expression simultanée des deux versions augmentait la production de lumière, prouvant que la stratégie à double appât facilite la capture d’interactions faibles ou sensibles à l’orientation. Le système a également détecté des contacts impliquant des protéines membranaires, une classe notoirement difficile à étudier avec les méthodes traditionnelles du deux-hybride chez la levure. Forts de cette validation, les auteurs ont étendu leur approche à un criblage à l’échelle du génome, en utilisant une protéine liée à la transcription, appelée Tfs1, comme appât. En testant plus de 4 600 protéines proies, ils ont identifié 31 candidats solides, comprenant plusieurs partenaires déjà connus et de nombreuses nouveautés, certaines situées en dehors du noyau, comme dans les mitochondries ou à la surface cellulaire. 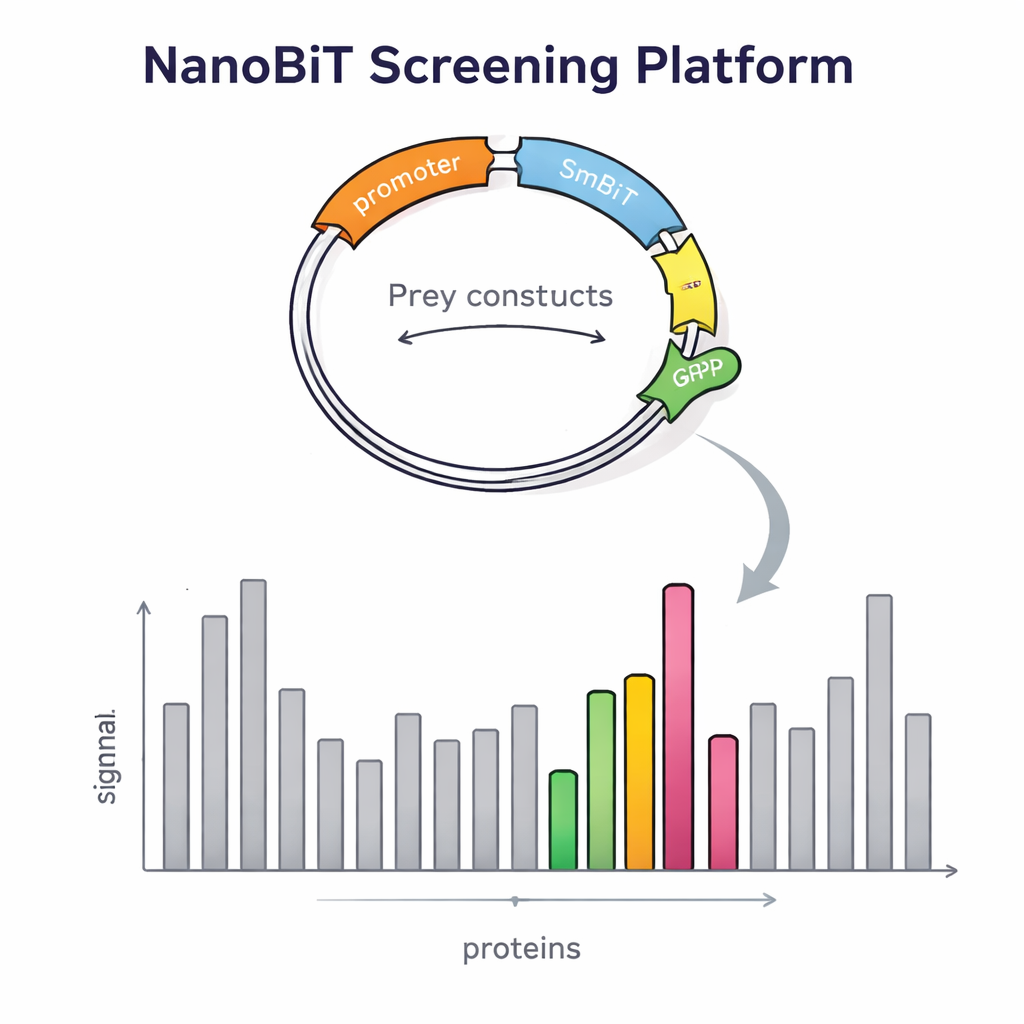
Ce que cela implique pour la biologie et la découverte de médicaments
Pour un non-spécialiste, le message clé est que les auteurs ont construit un « radar d’interactions » intracellulaire plus sensible. En convertissant des poignées de main protéiques brèves en éclats de lumière mesurables, et en organisant ingénieusement la génétique pour exprimer trois protéines marquées simultanément, leur système révèle des partenaires protéiques connus et jusque-là invisibles. Bien que des vérifications supplémentaires par d’autres techniques restent nécessaires pour confirmer chaque nouvelle association, cette plateforme comble des lacunes importantes dans nos cartographies des réseaux cellulaires. Parce que les souches ont aussi été conçues pour être plus sensibles aux petites molécules, le même montage pourrait être adapté pour rechercher des médicaments qui perturbent des associations protéiques nocives ou stabilisent des associations bénéfiques, offrant un nouvel outil puissant pour la biologie fondamentale et la découverte de médicaments en phase précoce.
Citation: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Mots-clés: interactions protéiques, levure de division, test de luminescence, criblage à haut débit, outils de découverte de médicaments