Clear Sky Science · fr
Secretome dépendant du particle de reconnaissance du signal chez l'humain
Comment les cellules décident quelles protéines quittent la cellule
Nos cellules expédient en permanence des protéines qui forment des hormones, des anticorps et l’armature entre les tissus. Mais toute protéine n’est pas destinée à voyager. Cette étude pose une question simple mais restée sans réponse : comment les cellules humaines déterminent-elles quelles protéines comptent sur un assistant clé, la particule de reconnaissance du signal (SRP), pour atteindre le centre d’acheminement interne de la cellule, et lesquelles peuvent y parvenir sans elle ? En cartographiant cette décision à l’échelle de milliers de protéines simultanément, les auteurs révèlent qui dépend du SRP, qui n’en dépend pas, et ce qui se passe lorsque ce système se dérègle — un sujet pertinent pour de nombreuses maladies liées à des protéines sécrétées mal routées ou absentes.
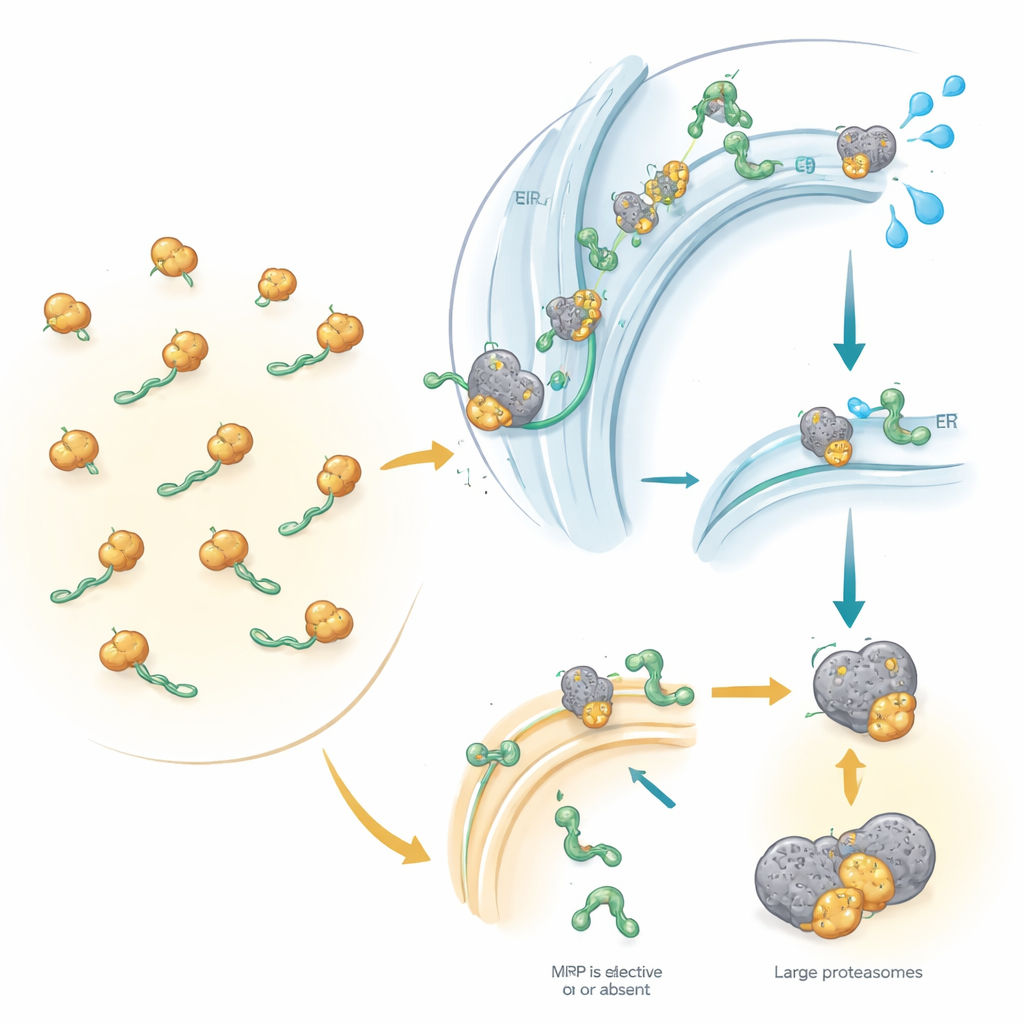
Le quai d’embarquement cellulaire et son guide principal
Environ une protéine humaine sur trois est destinée soit à la surface cellulaire, aux membranes cellulaires, soit à être libérée à l’extérieur de la cellule. Pour atteindre le bon emplacement, la plupart de ces protéines doivent d’abord entrer dans un réseau de membranes internes appelé réticulum endoplasmique, le quai d’embarquement de la cellule. Le SRP joue le rôle de guide : il reconnaît une petite « étiquette d’adresse » au début des protéines nouvellement synthétisées et suspend temporairement leur production. Cette pause donne au ribosome — la machine de fabrication des protéines — le temps de se positionner sur le réticulum endoplasmique, où la production reprend et la protéine naissante est insérée dans ou à travers la membrane. Certaines protéines, cependant, utilisent des voies alternatives qui ne requièrent pas le SRP, en particulier les protéines très petites ou celles ancrées par leur extrémité C-terminale. Jusqu’à présent, les scientifiques ne savaient pas, à l’échelle globale, quelles protéines humaines nécessitent réellement le SRP et lesquelles peuvent le contourner.
Réduire le SRP pour voir ce qui casse
Pour répondre à cette question, les chercheurs ont réduit sélectivement les niveaux d’un composant essentiel du SRP, SRP54, dans des cellules humaines HeLa. Ils ont ensuite utilisé une technique sensible, la spectrométrie de masse, pour mesurer plus de 6 000 protéines à l’intérieur des cellules et près de 2 000 protéines présentes dans le liquide environnant, appelé milieu conditionné. En comparant les cellules avec un SRP54 normal à celles appauvries en SRP54, ils ont pu identifier quelles protéines diminuaient, lesquelles augmentaient et lesquelles restaient inchangées. Une forte baisse du niveau d’une protéine — en particulier à la fois à l’intérieur de la cellule et dans le milieu — a été interprétée comme un signe que cette protéine dépend du SRP pour être produite et acheminée correctement.
Qui dépend du SRP et qui s’en passe
L’analyse a montré que la plupart des protéines normalement sécrétées dans le milieu dépendent clairement du SRP. Lorsque SRP54 était réduit, la majorité de ces protéines sécrétées, en particulier celles portant une étiquette d’adresse classique, ont fortement diminué. De nombreuses protéines membranaires intracellulaires ont également diminué, les révélant comme clientes du SRP. Un ensemble plus restreint de protéines avec des étiquettes semblables n’a été que peu affecté, les classant comme indépendantes du SRP ; celles-ci utilisent probablement des voies alternatives pour atteindre le réticulum endoplasmique. Les chercheurs ont aussi découvert que des caractéristiques spécifiques de l’étiquette d’adresse — comme une région chargée positivement à son début — étaient plus fréquentes chez les protéines dépendantes du SRP, suggérant des règles subtiles qui aident le SRP à choisir son chargement. Parallèlement, certaines protéines impliquées dans le marquage des protéines endommagées pour destruction et dans la fonction mitochondriale ont augmenté, suggérant que les cellules activent des systèmes de secours et la production d’énergie lorsque leur guide d’acheminement principal est compromis.
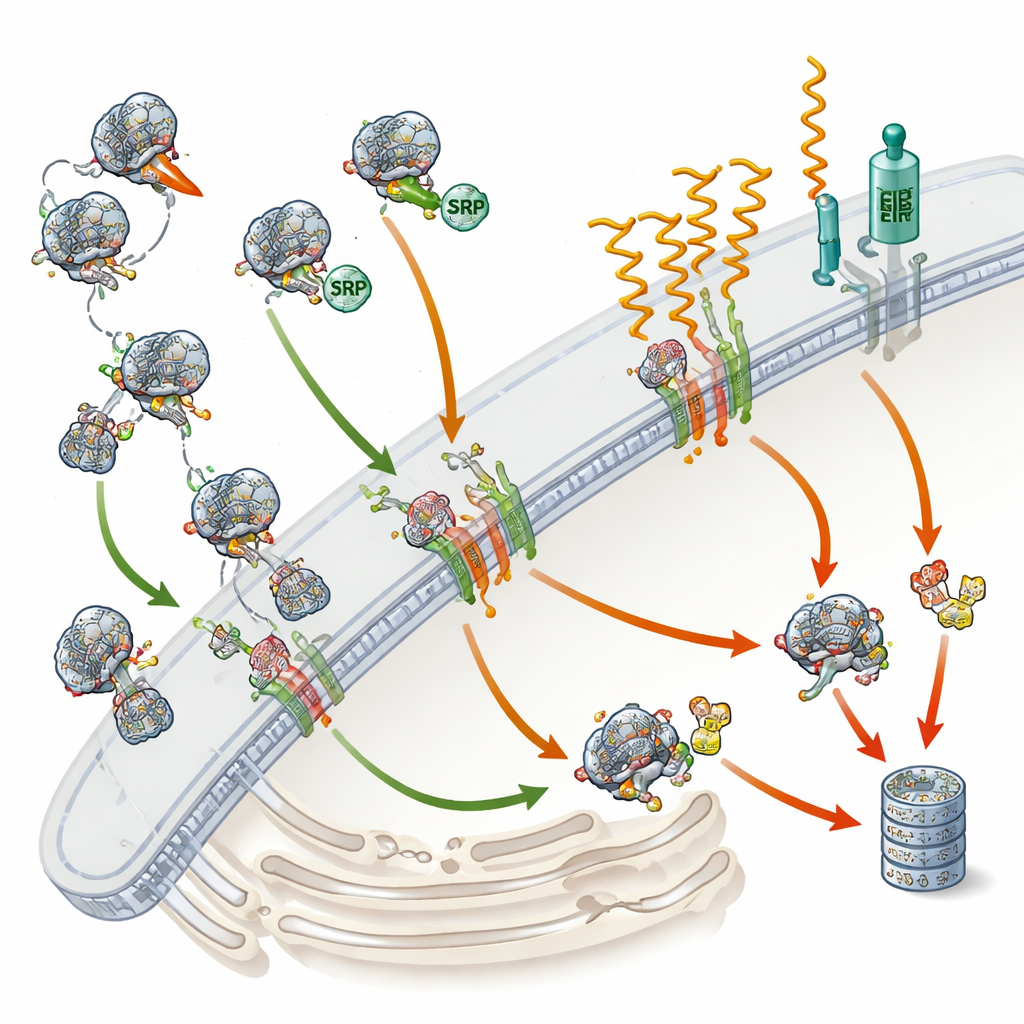
Contrôle de qualité lorsque le ciblage rate
L’étude est allée au‑delà du simple comptage des protéines : elle a comparé ces variations aux changements de l’ARN messager, les plans utilisés pour fabriquer les protéines. De nombreuses protéines dépendantes du SRP ont perdu non seulement la protéine mais aussi leurs plans ARN, impliquant une voie de contrôle qualité connue sous le nom de RAPP. Lorsque le SRP ne peut pas s’engager correctement sur une protéine sécrétoire ou membranaire naissante, cette voie semble déclencher la dégradation de l’ARN correspondant, empêchant la production supplémentaire d’une protéine mal routée. Parallèlement, les protéines incomplètes qui n’atteignent pas le réticulum endoplasmique sont probablement marquées par de petits drapeaux moléculaires et dirigées vers des « broyeuses » cellulaires appelées protéasomes. Fait intéressant, les voies classiques de stress du réticulum endoplasmique n’étaient pas fortement activées, laissant entendre qu’un SRP défectueux provoque un type distinct de réponse de stress cellulaire.
Ce que cela signifie pour la santé et la maladie
En cartographiant, pour la première fois chez l’humain, quelles protéines sécrétées et membranaires sont dépendantes du SRP et lesquelles sont indépendantes, ce travail fournit une carte de référence des règles d’acheminement cellulaires. Les résultats montrent que la plupart des protéines exportées reposent réellement sur le SRP et que, lorsque le SRP faiblit, les cellules réagissent en dégradant à la fois les protéines et leurs plans tout en activant des mécanismes d’adaptation alternatifs. Parce que de nombreuses mutations pathogènes affectent les « étiquettes d’adresse » des protéines sécrétées, comprendre précisément comment le SRP reconnaît ses clientes et comment la RAPP élimine les défectueuses peut aider à expliquer pourquoi certaines mutations entraînent des déficits hormonaux, des problèmes immunitaires ou une neurodégénérescence — et pourrait éventuellement indiquer de nouvelles voies pour ajuster l’acheminement des protéines en médecine humaine.
Citation: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Mots-clés: sécrétion des protéines, particule de reconnaissance du signal, secretome, contrôle de qualité des protéines