Clear Sky Science · fr
L’inhibition séquentielle au platine et de PARP améliore l’efficacité de l’immunothérapie anti‑PD1 dans un cancer du pancréas murin muté en Brca2
Pourquoi cette recherche est importante pour les patients
Le cancer du pancréas est l’un des cancers les plus meurtriers, et même lorsque les médecins identifient une vulnérabilité exploitable — comme une mutation du gène BRCA2 — les traitements actuels contrôlent rarement la maladie sur le long terme. Cette étude utilise un modèle murin réaliste pour poser une question pratique que se posent aujourd’hui de nombreux patients et oncologues : après une chimiothérapie intensive puis un inhibiteur de PARP, l’ajout d’une immunothérapie moderne peut‑il prolonger significativement la survie, et pourquoi les tumeurs récidivent‑elles si souvent ?
Un cancer tenace avec un point faible génétique
L’adénocarcinome canalaire pancréatique est notoirement difficile à traiter, avec un taux de survie à cinq ans encore à un chiffre. Une petite fraction de patients porte des défauts hérités ou spécifiques à la tumeur dans BRCA2, un gène nécessaire pour réparer l’ADN cassé. Ces tumeurs sont exceptionnellement sensibles aux médicaments qui endommagent l’ADN, comme les chimiothérapies à base de platine, et aux inhibiteurs de PARP, qui fragilisent davantage la capacité des cellules cancéreuses à réparer l’ADN. La prise en charge standard actuelle pour les cancers du pancréas avancés mutés BRCA consiste en plusieurs mois de chimiothérapie au platine suivis d’un traitement d’entretien par inhibiteur de PARP. Pourtant, dans l’essai clinique clé POLO, cette stratégie n’a pas prolongé la survie globale, ce qui souligne la nécessité de comprendre la résistance et de concevoir de meilleures approches d’entretien.
Construire un modèle murin plus fidèle
Beaucoup de modèles de laboratoire existants éliminent les composantes immunitaires et stromales qui entourent les tumeurs réelles chez les patients. Pour y remédier, les auteurs ont mis au point des souris développant des tumeurs pancréatiques déficientes en BRCA2 dans le contexte d’un système immunitaire pleinement fonctionnel. À partir de ces tumeurs spontanées, ils ont dérivé des lignées cellulaires clonales pouvant être greffées dans des souris génétiquement appariées. Ces tumeurs Brca2‑mutées ressemblaient et se comportaient beaucoup comme les cancers du pancréas humains : elles étaient fortement fibreuses, excluaient en grande partie les lymphocytes T et présentaient des niveaux élevés de dommages spontanés de l’ADN. De façon cruciale, les tumeurs étaient très sensibles à une association au platine courante (gemcitabine plus cisplatine), tandis que le traitement par inhibiteur de PARP seul n’avait qu’un effet modeste et de courte durée chez l’animal, malgré une forte activité contre ces mêmes cellules en culture. 
La chimiothérapie redessine le micro‑environnement tumoral
L’équipe a ensuite examiné ce qui se passe à l’intérieur de la tumeur après une chimiothérapie au platine. Dix jours après le traitement, les tumeurs avaient diminué mais n’étaient pas éradiquées. Les analyses d’expression génique ont révélé un basculement marqué vers une activité liée au système immunitaire : des voies associées à l’activation des lymphocytes T et à l’immunité adaptative étaient mises en marche. On retrouvait davantage de lymphocytes T dans les tumeurs traitées, et beaucoup de ces T présentaient des marqueurs d’épuisement — signes qu’ils avaient été activés mais devenaient inefficaces. Des schémas similaires d’augmentation des lymphocytes T ont été observés dans des cancers du pancréas humains porteurs de mutations BRCA ou PALB2 apparentées après que des patients ont reçu une chimiothérapie à base de platine avant la chirurgie. Parallèlement, les cellules tumorales augmentaient leur expression de PD‑L1, une protéine de surface capable d’éteindre les lymphocytes T en engageant le récepteur PD‑1, suggérant que les tumeurs se défendaient contre cette nouvelle pression immunitaire.
Pourquoi le PARP seul ne suffit pas — et où la résistance apparaît
À l’image de la prise en charge clinique, les chercheurs ont administré aux souris un traitement initial de gemcitabine et cisplatine, suivi d’un entretien par l’inhibiteur de PARP olaparib. Cette séquence a amélioré le contrôle tumoral et la survie par rapport à la chimiothérapie seule, confirmant que la chimiothérapie préalable peut rendre les tumeurs plus sensibles au blocage de PARP. Cependant, aucune souris n’a été guérie : les tumeurs ont finalement repoussé sous l’entretien par PARP. Les tumeurs résistantes présentaient un aspect plus différencié et une forte augmentation de l’expression du régulateur du développement CDX2. Cela suggère que, du moins dans ce modèle, la résistance n’émerge pas simplement par la restauration du défaut initial de réparation de l’ADN, mais peut impliquer un changement d’identité cellulaire de la tumeur. CDX2 pourrait potentiellement servir de biomarqueur de résistance émergente chez les patients.
Déverrouiller l’immunothérapie avec le bon ordre
Les médicaments ciblant les points de contrôle immunitaires, comme les anticorps anti‑PD1, ont transformé le traitement de plusieurs cancers, mais le cancer du pancréas est resté majoritairement non réceptif. Conformément à cela, l’anti‑PD1 (avec ou sans un autre inhibiteur de point de contrôle, l’anti‑CTLA4) n’a pas aidé lorsqu’il a été administré à des tumeurs BRCA2‑mutantes non préalablement traitées, et n’a guère amélioré les choses lorsqu’il a simplement été ajouté à une thérapie par inhibiteur de PARP. Le tableau a changé lorsque la séquence complète a été utilisée : chimiothérapie au platine d’abord, puis inhibition de PARP plus anti‑PD1 en entretien. Dans ce contexte, les tumeurs ont régressé plus profondément et les souris ont vécu plus longtemps que sous chimiothérapie plus PARP ou anti‑PD1 seul. L’ajout d’anti‑CTLA4 à l’entretien par PARP n’a pas apporté d’avantages similaires, ce qui suggère que le micro‑environnement tumoral amorcé par la chimiothérapie est spécifiquement prêt à répondre au blocage de PD‑1. 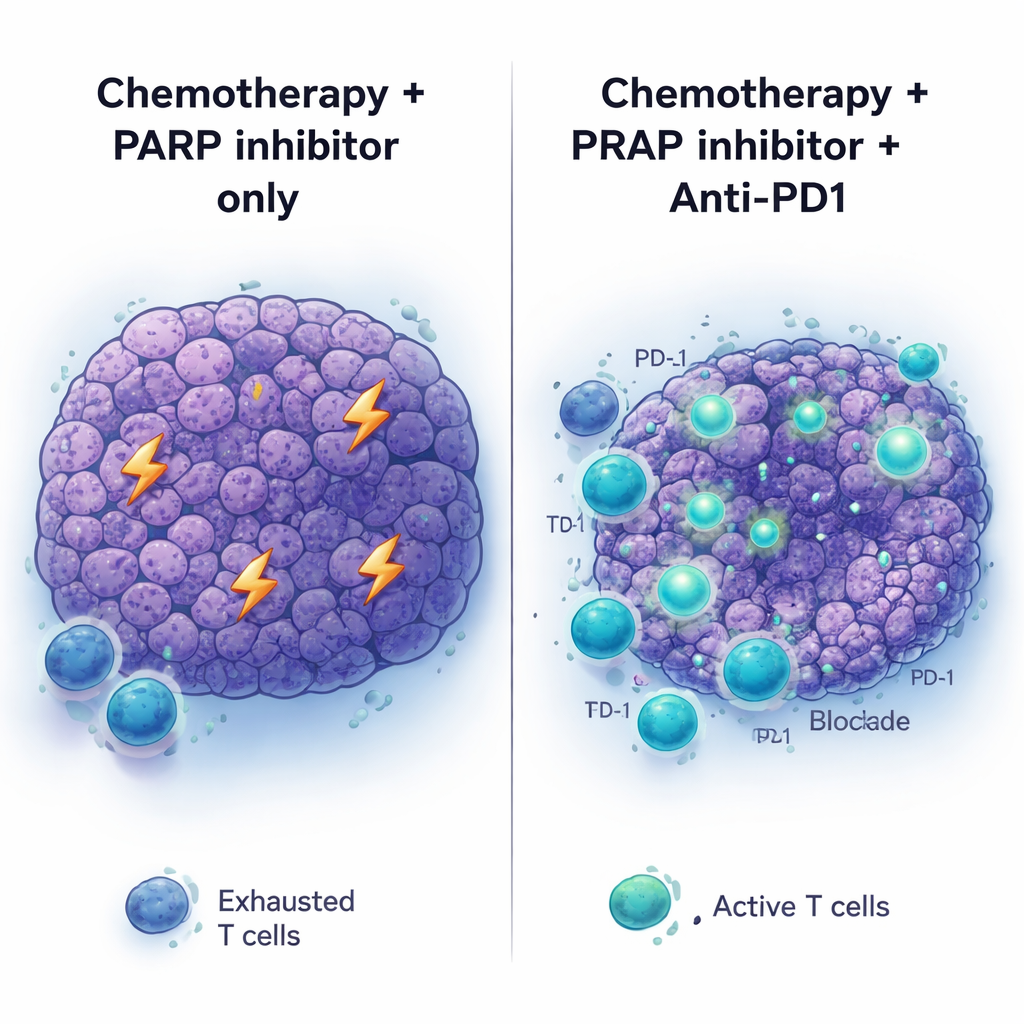
Ce que cela pourrait signifier pour les soins futurs
Globalement, l’étude soutient que, pour les cancers du pancréas mutés BRCA, l’ordre et la combinaison des traitements ont une importance cruciale. Une chimiothérapie fortement dommageable pour l’ADN n’attaque pas seulement les cellules tumorales directement, elle suscite aussi une réponse immunitaire, même si cette réponse est initialement atténuée par l’épuisement et les défenses PD‑L1. Les inhibiteurs de PARP peuvent prolonger le bénéfice mais sont peu susceptibles d’être curatifs seuls et peuvent pousser les tumeurs vers un état résistant, à forte expression de CDX2. En superposant une immunothérapie anti‑PD1 à l’entretien par PARP après une chimiothérapie au platine, il pourrait être possible de convertir ce paysage immune brièvement inflammé et épuisé en une attaque anti‑tumorale plus efficace et durable. Les essais cliniques en cours combinant inhibiteurs de PARP et immunothérapie dans les cancers du pancréas liés à BRCA seront déterminants pour savoir si cette stratégie minutieusement ordonnancée peut se traduire par des vies plus longues et de meilleure qualité pour les patients.
Citation: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Mots-clés: cancer du pancréas, mutation BRCA2, chimiothérapie au platine, inhibiteur de PARP, immunothérapie anti‑PD‑1