Clear Sky Science · fr
Synthèse efficace d’amides sans solvant via la réaction de Ritter catalysée par un nanocomposite réutilisable Fe3O4/g‑C3N4/NTMPA
Pourquoi une chimie plus propre compte
Beaucoup des médicaments que nous prenons, des plastiques qui nous entourent et même des fibres à haute performance sont construits à partir d’un type simple de liaison chimique appelé liaison amide. La fabrication industrielle de ces liaisons exige généralement des acides forts et corrosifs et de grands volumes de solvant, ce qui génère des déchets et pose des problèmes de sécurité. Cet article décrit un nouveau catalyseur solide réagissant aux champs magnétiques qui permet de former des amides en haut rendement sans utiliser de solvant, ouvrant la voie à une production plus sûre et plus durable de médicaments et de matériaux.
Un maillon clé dans les médicaments et les matériaux
Les amides sont les liaisons qui maintiennent les protéines et se retrouvent aussi dans d’innombrables produits pharmaceutiques, agrochimiques et polymères comme le nylon. Les chimistes disposent de nombreuses méthodes pour former des liaisons amide, mais la plupart nécessitent soit des précurseurs activés soit des conditions sévères. La réaction de Ritter se distingue car elle unit directement un alcool (ou un alcène) et une nitrile en une seule étape. Cependant, sous sa forme classique, la réaction de Ritter dépend d’acides minéraux concentrés comme l’acide sulfurique ou chlorhydrique. Ces acides liquides sont corrosifs, difficiles à séparer des produits et difficiles à recycler, ce qui les rend peu compatibles avec la chimie durable.
Un petit aimant que l’on peut agiter
Les chercheurs ont conçu un catalyseur solide et séparables magnétiquement pouvant remplacer ces acides liquides. Leur matériau combine trois composants : des nanoparticules d’oxyde de fer (Fe3O4), qui confèrent des propriétés magnétiques ; un solide stratifié riche en carbone et en azote (nitrure de carbone graphitique, g‑C3N4), qui sert de support protecteur ; et une molécule fortement acide appelée nitrilotri(méthylphosphonique) (NTMPA), qui fournit l’acidité nécessaire à la réaction. Ces éléments sont assemblés de sorte que la NTMPA soit ancrée à la surface du g‑C3N4, tandis que de petites particules de Fe3O4 sont dispersées dans l’ensemble. Comme le composite entier répond à un aimant, il peut être retiré du mélange réactionnel simplement en plaçant un aimant à l’extérieur du ballon.
Caractériser la structure du catalyseur
Pour confirmer qu’ils avaient construit le matériau prévu, les auteurs ont utilisé un ensemble d’outils de science des matériaux. La spectroscopie infrarouge a montré des signaux provenant des groupes phosphoniques, du réseau carbone‑azote et des liaisons fer–oxygène, tous présents ensemble dans le composite final. La diffraction des rayons X a indiqué que l’oxyde de fer magnétique conservait sa forme cristalline, tandis que le nitrure de carbone restait sous forme d’un solide stratifié et quelque peu désordonné. La microscopie électronique a révélé des particules en feuillets décorées de sphères uniformément dispersées d’environ 10–20 nanomètres, et la cartographie élémentaire a montré du fer, du carbone, de l’azote, de l’oxygène et du phosphore répartis de façon homogène. Les mesures de surface spécifique et de taille de pores ont confirmé une structure mésoporeuse — pleine de canaux à l’échelle nanométrique qui permettent aux réactifs d’atteindre les sites actifs — tandis que l’analyse thermique a montré que le matériau reste stable jusqu’à plusieurs centaines de degrés Celsius.
Réactions rapides sans solvant
Une fois la structure établie, l’équipe a testé le catalyseur dans la réaction de Ritter entre divers alcools et nitriles. Ils ont constaté que les meilleures conditions étaient étonnamment simples : des quantités équimolaires d’alcool et de nitrile, une faible dose du catalyseur solide, chauffage à 80 °C et aucun solvant ajouté. Dans ces conditions, de nombreux réactifs différents ont été convertis en leurs amides correspondants avec des rendements élevés à excellents, souvent supérieurs à 90 %. Les alcools tertiaires et benzyliques (qui forment plus facilement l’intermédiaire réactif nécessaire à la réaction de Ritter) ont réagi en seulement 1–4 heures, tandis que des substrats plus exigeants ont demandé un peu plus de temps. Les nitriles aromatiques et aliphatiques ont bien fonctionné, les substituants fortement attracteurs sur les nitriles aromatiques rendant la réaction encore plus efficace. Globalement, l’étude a montré que le catalyseur solide peut égaler ou surpasser de nombreux acides liquides, tout en évitant les milieux corrosifs et les solvants supplémentaires.
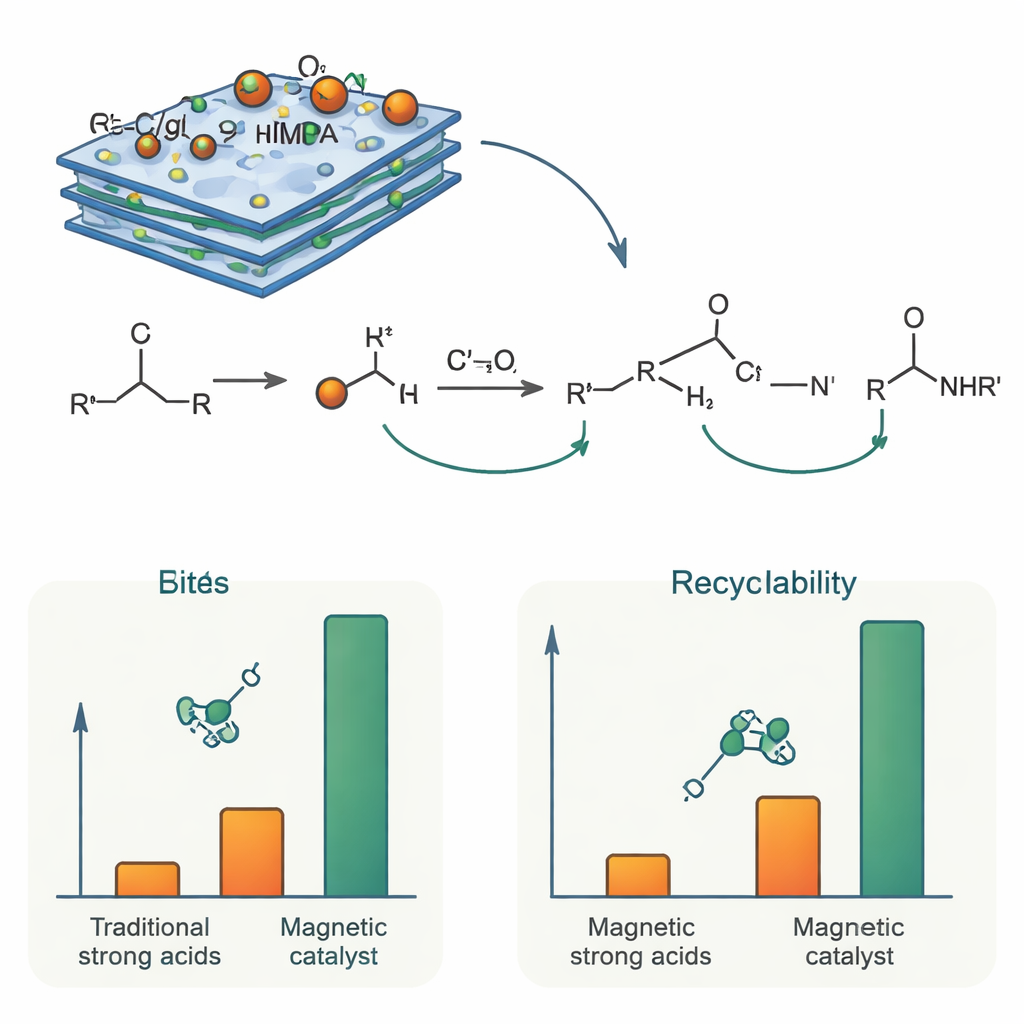
Comment cela fonctionne et pourquoi il dure
Du point de vue chimique, le rôle du catalyseur est de protoner brièvement l’alcool et d’aider sa déshydratation, générant une espèce chargée positivement de courte durée. Une molécule de nitrile attaque ensuite cet intermédiaire pour former une nouvelle liaison carbone–azote, qui est finalement convertie en amide par réaction avec l’eau formée au cours du processus. Les groupes phosphoniques de la NTMPA apportent une acidité contrôlée, suffisamment forte pour piloter ces étapes mais modérée par la surface de nitrure de carbone environnante de sorte que les réactions secondaires indésirables soient minimisées. Parce que les unités actives de NTMPA sont chimiquement liées au support solide, elles ne se lessivent pas pendant la réaction. Des mesures de magnétisation ont confirmé que les particules restent fortement magnétiques, permettant d’éliminer rapidement le catalyseur usé à l’aide d’un aimant. Lors de tests de réutilisation, le même lot de catalyseur a été employé au moins six fois avec seulement une faible baisse d’activité, et les analyses structurelles après usage ont montré que sa composition et sa morphologie étaient en grande partie inchangées.
Ce que cela signifie pour une production plus verte
Pour un lecteur non spécialiste, l’idée principale est que les auteurs ont développé une poudre réutilisable et réactive magnétiquement qui aide les chimistes à assembler des liaisons amide importantes sans dépendre des acides liquides agressifs et des solvants supplémentaires habituellement requis. Cette approche réduit les déchets, simplifie la purification des produits et facilite le recyclage du catalyseur, autant d’éléments importants pour une chimie industrielle plus verte. Bien que le travail se concentre sur un type de réaction, les mêmes principes de conception — ancrer des groupes acides puissants sur un support robuste et magnétique — pourraient s’appliquer à de nombreuses autres transformations qui sous-tendent la production de médicaments et de matériaux avancés.
Citation: Karimitabar, H., Sardarian, A.R. Efficient solvent-free amide synthesis via Ritter reaction catalyzed by a reusable Fe3O4/g-C3N4/ NTMPA nanocomposite. Sci Rep 16, 6494 (2026). https://doi.org/10.1038/s41598-026-35371-2
Mots-clés: synthèse d’amides, réaction de Ritter, <keyword>chimie sans solvant, catalyse verte