Clear Sky Science · fr
Classification multi‑classe des maladies oculaires par apprentissage profond : techniques de fusion EfficientNetB0
Pourquoi les examens oculaires précoces sont importants
La perte de la vue s’installe souvent en silence. Des troubles oculaires fréquents comme la cataracte, le glaucome et les atteintes rétiniennes liées au diabète peuvent voler la vision longtemps avant que les symptômes ne deviennent évidents. Partout dans le monde, il n’y a pas suffisamment de spécialistes pour examiner tout le monde à temps, notamment en milieu rural ou dans les zones à faibles revenus. Cette étude explore comment un système informatique intelligent capable d’analyser des photographies du fond d’œil pourrait aider les médecins à détecter plusieurs maladies oculaires majeures tôt et de façon fiable, en utilisant le même type d’intelligence artificielle qui alimente la recherche d’images et la reconnaissance faciale modernes.
Détecter la maladie sur une seule image
Les ophtalmologistes utilisent déjà des photographies en couleur de la rétine — la couche sensible à la lumière au fond de l’œil — pour rechercher des signes de maladie. Sur ces images, la cataracte apparaît comme une opacification du trajet optique, le glaucome modifie la forme du nerf optique et la rétinopathie diabétique parcourt la rétine de petites fuites et cicatrices. Les chercheurs ont rassemblé 4 217 images rétiniennes haute résolution, équilibrées entre quatre groupes : yeux sains, cataracte, glaucome et rétinopathie diabétique. En travaillant avec un ensemble équilibré issu de plusieurs sources publiques, ils ont réduit le risque que l’ordinateur apprenne des raccourcis liés à un hôpital, un appareil photo ou un type de maladie plutôt qu’aux véritables signes pathologiques. 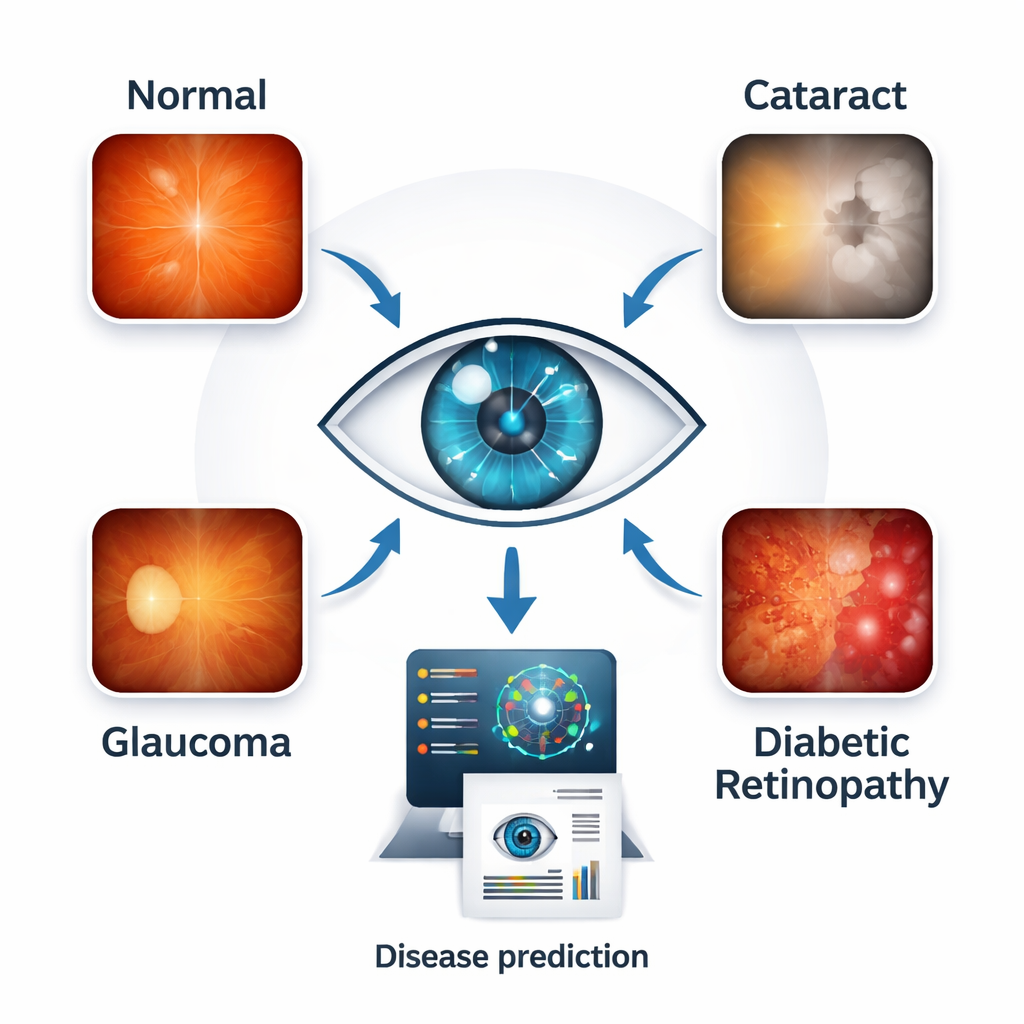
Laisser deux cerveaux travailler ensemble
Les programmes modernes d’analyse d’images, appelés modèles d’apprentissage profond, excellent pour repérer des motifs mais chacun a ses forces et ses angles morts. Plutôt que de s’appuyer sur un seul modèle, l’équipe a construit des systèmes « à double backbone » qui exécutent deux réseaux d’image bien connus en parallèle puis fusionnent leurs observations. L’un de ces réseaux, EfficientNetB0, est un modèle compact et efficace qui saisit la structure générale des images ; il a été utilisé systématiquement comme base. Il a été associé, tour à tour, à trois autres modèles — ResNet50, InceptionV3 et AlexNet — qui se spécialisent dans la reconnaissance de motifs profonds, multi‑échelles ou légère. Les systèmes combinaient ensuite les deux ensembles de caractéristiques de différentes manières : en les joignant simplement, en les additionnant, en les pondérant différemment ou en laissant chaque modèle voter pour la réponse finale.
Soumettre le système à l’épreuve
Les chercheurs ont entraîné et ajusté 12 combinaisons de modèles différentes sur la majeure partie de leurs images rétiniennes, en réservant un échantillon pour évaluer les performances. Lors de ce test interne, la meilleure approche a joint les caractéristiques d’EfficientNetB0 et de ResNet50, atteignant environ 95 % de précision globale et un score quasi parfait sur une mesure standard de qualité diagnostique. Des combinaisons similaires avec InceptionV3 et AlexNet ont également affiché de bonnes performances. Pour vérifier si le système pouvait gérer la diversité du monde réel plutôt que de mémoriser son jeu d’entraînement, l’équipe a ensuite testé tous les modèles sur 400 images provenant de deux collections indépendantes prises dans des hôpitaux différents avec des appareils différents. Là, la précision a encore augmenté, atteignant environ 95 à 98 %, et tous les modèles ont conservé des scores très élevés pour la séparation des yeux malades et sains.
Regarder à l’intérieur de la boîte noire
Les médecins et les régulateurs demandent de plus en plus non seulement « Quelle est sa précision ? » mais aussi « Pourquoi prend‑il cette décision ? ». Pour répondre, les auteurs ont utilisé des outils de visualisation tels que Score‑CAM et LIME. Ces outils mettent en évidence les zones d’une image qui influencent le plus le verdict du modèle, transformant « l’attention » du système en cartes de chaleur superposées à la rétine. Pour la rétinopathie diabétique, les zones mises en évidence correspondaient aux vaisseaux sanguins qui fuient et aux taches proches de la macula, le centre de vision fine. Pour le glaucome, l’attention portait sur la tête du nerf optique et les tissus environnants, là où surviennent les lésions. Les décisions liées à la cataracte mettaient l’accent sur une opacification diffuse le long du trajet visuel. Crucialement, les yeux normaux n’affichaient pas de points chauds forts et déplacés. Cette concordance étroite entre le foyer du modèle et l’anatomie des manuels suggère que le système se concentre sur les mêmes caractéristiques que les cliniciens utilisent en pratique. 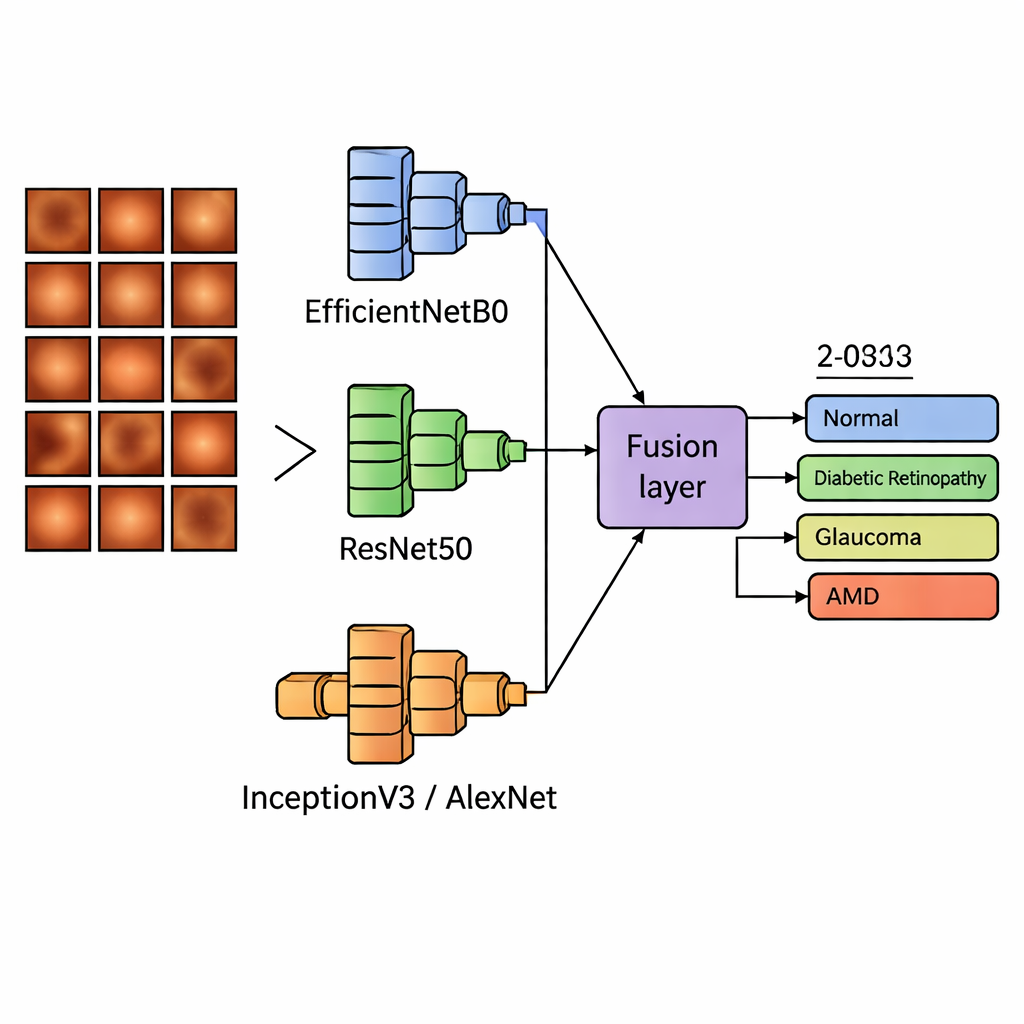
Ce que cela pourrait signifier pour les soins quotidiens
Pour un non‑spécialiste, l’essentiel est qu’une seule photographie rétinienne, prise avec un appareil standard, pourrait bientôt aider à dépister plusieurs causes majeures de cécité à la fois. La conception à double réseau et les méthodes intelligentes de fusion de leurs sorties ont apporté non seulement une grande précision mais aussi des résultats stables lorsque les images provenaient de nouvelles cliniques et d’appareils différents — condition essentielle pour une utilisation réelle. Si des tests supplémentaires sur des populations plus larges et plus diverses restent nécessaires, en particulier avant que la technologie puisse guider le traitement de façon autonome, ce travail montre que la combinaison de différents « yeux » artificiels peut fournir des seconds avis rapides et fiables. Dans les hôpitaux surchargés, les petites cliniques ou les unités mobiles de dépistage, de tels outils pourraient aider à repérer les personnes qui doivent le plus urgemment consulter un spécialiste, préservant potentiellement la vue de millions de personnes.
Citation: Sah, U.K., Chatterjee, J.M. & Sujatha, R. Multi-class eye disease classification using deep learning EfficientNetB0 fusion techniques. Sci Rep 16, 6368 (2026). https://doi.org/10.1038/s41598-026-35357-0
Mots-clés: maladie oculaire, imagerie rétinienne, apprentissage profond, glaucome, rétinopathie diabétique