Clear Sky Science · fr
Optimisation et mécanismes d’adsorption pour l’élimination du vanadium par du bentonite pillé au fer en tant qu’adsorbant efficace
Pourquoi il est important d’éliminer le vanadium de l’eau
Des industries modernes comme la sidérurgie et le raffinage de pétrole libèrent discrètement dans l’eau un métal peu connu, le vanadium. À fortes concentrations, le vanadium peut être toxique pour l’homme et la vie aquatique, mais il représente aussi une ressource précieuse susceptible d’être récupérée. Cette étude explore une méthode peu coûteuse pour purifier l’eau du vanadium en utilisant une argile naturellement abondante qui a été « calée » par des atomes de fer pour en faire une éponge plus efficace contre la pollution.
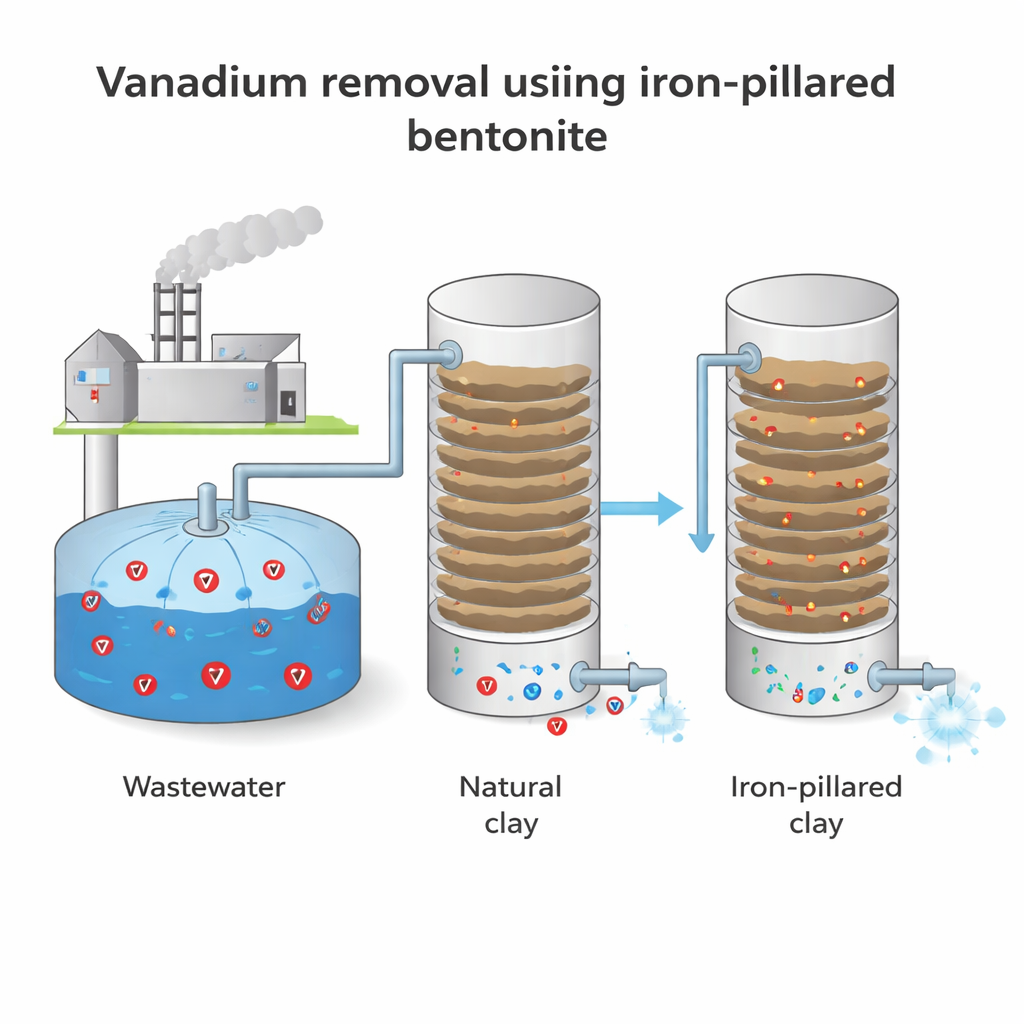
Transformer une argile commune en une éponge plus intelligente
Les chercheurs ont commencé par la bentonite, une argile douce déjà employée dans la litière pour animaux, les boues de forage et le nettoyage environnemental. À elle seule, cette argile peut piéger des ions métalliques, mais ses espaces internes sont limités. Pour améliorer ses performances, l’équipe a élaboré une « bentonite pillée au fer ». Ils ont trempé l’argile purifiée dans une solution riche en fer puis l’ont chauffée pour que de petits agrégats d’oxyde de fer forment des piliers permanents entre les couches d’argile. Des analyses par rayons X, infrarouge, mesures de surface et microscopie électronique ont confirmé que les couches étaient écartées, que la surface augmentait et que la structure devenait plus poreuse et aérée. En bref, « l’immeuble » interne de l’argile a gagné des étages supplémentaires et des couloirs plus larges pour accueillir le vanadium.
Tester l’efficacité du nouveau matériau pour purifier l’eau
Puis, les scientifiques ont évalué l’efficacité de l’argile modifiée pour éliminer le vanadium de l’eau. Ils se sont concentrés sur trois paramètres pratiques qu’un opérateur peut ajuster : l’acidité de l’eau (pH), la concentration initiale en vanadium et la quantité d’argile ajoutée. À l’aide d’un outil statistique appelé méthode de surface de réponse, ils ont cartographié l’interaction de ces facteurs. Dans les conditions optimales identifiées — eau légèrement acide (environ pH 5,8), faible concentration initiale en vanadium (50 milligrammes par litre) et dose d’argile relativement élevée (6 grammes par litre) avec trois heures de contact — la bentonite pillée au fer a éliminé environ 60 % du vanadium. C’est à peu près 20 % de mieux que la même argile à l’état naturel, montrant que l’amélioration structurelle se traduit par un gain de performance concret.
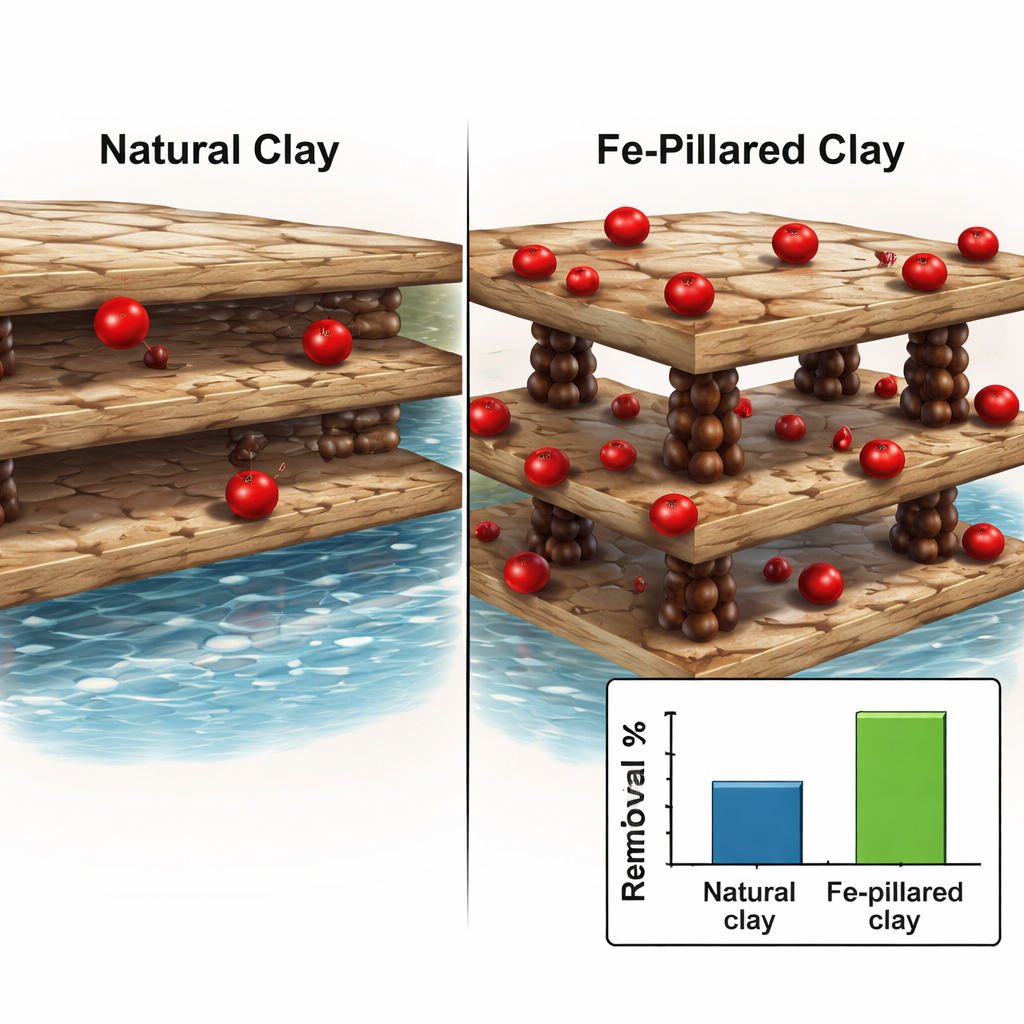
Ce qui se passe à l’échelle microscopique
Pour comprendre les phénomènes à l’échelle microscopique, l’équipe a analysé la façon dont le vanadium se fixe à la surface de l’argile et la vitesse à laquelle cela se produit. Les données suivent un comportement de type isotherme de Langmuir, compatible avec la formation d’une unique couche organisée d’ions vanadium sur une surface relativement homogène plutôt qu’un empilement aléatoire. Le comportement en fonction du temps correspond à un modèle cinétique dit d’ordre deux, ce qui indique un processus contrôlé par des liaisons chimiques, comme un échange d’ions entre le vanadium en solution et des sites réactifs sur la bentonite pillée au fer. Des tests supplémentaires sur les variations d’énergie ont montré que le processus est spontané (il a tendance à se produire de lui‑même), devient plus favorable à des températures plus élevées et augmente légèrement le désordre à l’interface eau/solide, autant d’indices d’un processus d’adsorption robuste et efficace.
Concevoir des systèmes pour le traitement réel
Les auteurs ont également étudié comment la variation de la concentration en vanadium et de la dose d’argile influence l’élimination, en utilisant des surfaces de réponse tridimensionnelles pour visualiser les performances. Comme prévu, une augmentation de la concentration initiale en vanadium finit par dépasser les sites disponibles sur l’argile, réduisant le pourcentage d’élimination. Augmenter la quantité d’adsorbant améliore l’élimination, mais seulement jusqu’à ce que la surface soit saturée. La fenêtre de pH optimale s’explique par le fait que la charge de l’argile et la forme chimique du vanadium changent avec l’acidité ; dans la plage identifiée, la surface de la bentonite pillée au fer est chargée négativement et attire fortement les espèces de vanadium chargées positivement. Ensemble, ces connaissances fournissent un guide pour les ingénieurs afin d’ajuster les systèmes de traitement pour différents types d’effluents industriels.
Ce que cela signifie pour une eau plus sûre et plus propre
En termes accessibles, ce travail montre qu’une argile naturelle peu coûteuse peut être réingénierée intelligemment avec du fer pour devenir un meilleur aimant pour un métal problématique dans l’eau. En écartant les couches d’argile et en créant de nouveaux « points d’accroche » chimiques, la bentonite pillée au fer élimine davantage de vanadium que l’argile brute et le fait de manière prévisible et contrôlable. Bien qu’elle n’élimine pas complètement le vanadium, elle constitue une étape prometteuse et peu coûteuse vers des effluents industriels plus propres et une récupération facilitée d’un métal utile, en particulier dans les régions où les technologies de traitement avancées sont trop coûteuses ou complexes à déployer.
Citation: Etaati, A., Soleimani, M. Optimization and adsorption mechanisms of vanadium removal by Fe-Pillared bentonite as an efficient adsorbent. Sci Rep 16, 4915 (2026). https://doi.org/10.1038/s41598-026-35348-1
Mots-clés: élimination du vanadium, bentonite pillée au fer, traitement de l’eau, adsorption des métaux, eaux usées industrielles