Clear Sky Science · fr
Motifs informés et spatiaux pour données d'immunofluorescence multiplexées
Pourquoi le voisinage des cellules tumorales compte
Le cancer du pancréas est l’un des plus mortels, en partie parce que ses tumeurs évoluent au sein d’un « quartier » complexe composé de cellules immunitaires et de soutien qui peuvent soit combattre la tumeur, soit l’aider à se dissimuler. Cette étude présente une nouvelle manière d’analyser l’agencement spatial de ces cellules dans des images au microscope, révélant comment le système immunitaire se comporte différemment dans l’adénocarcinome canalaire pancréatique (PDAC) — forme agressive — par rapport à son homologue précancéreux, le néoplasme mucineux papillaire intraductal (IPMN). Comprendre ces motifs cachés pourrait ouvrir la voie à de meilleurs diagnostics et à des traitements plus ciblés et intelligents.
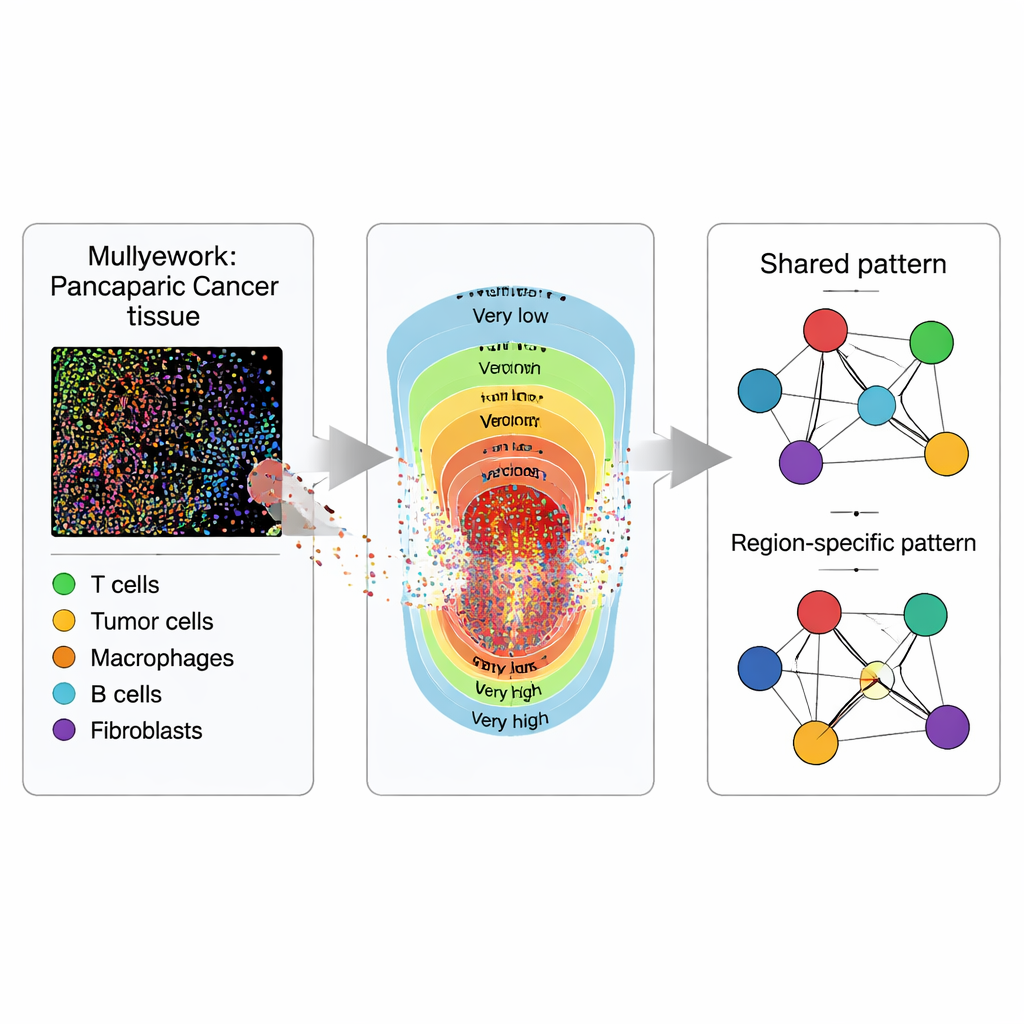
Voir les tissus comme des cartes, pas seulement comme des images
Plutôt que de considérer une coupe tumorale comme une image plate, les chercheurs la traitent comme une carte remplie de points. Grâce à l’imagerie d’immunofluorescence multiplexée, ils colorent des échantillons de tissus provenant de 119 patients PDAC et 53 patients IPMN afin que différents types cellulaires brillent dans des couleurs distinctes. Un logiciel spécialisé transforme chaque cellule visible en un point avec des coordonnées et une étiquette : cellules tumorales (épithéliales), plusieurs types de lymphocytes T capables d’attaquer ou de réguler la réponse immunitaire, et cellules présentatrices d’antigènes qui montrent des fragments tumoraux aux lymphocytes T. La question essentielle n’est pas seulement combien de chaque type de cellule sont présents, mais où ils se situent les uns par rapport aux autres dans le tissu.
Diviser la tumeur en zones
Pour saisir comment la tumeur évolue du centre vers l’extérieur, chaque échantillon tissulaire est divisé en cinq zones selon la densité des cellules tumorales, allant de l’intensité tumorale « très faible » à « très élevée ». Ces zones représentent un gradient de charge tumorale et d’encombrement cellulaire que les pathologistes observent souvent au microscope mais quantifient rarement. Dans chaque zone, l’équipe estime des « cartes d’intensité » lissées pour chaque type cellulaire, transformant en quelque sorte des points épars en cartes de chaleur continues montrant où chaque type cellulaire a tendance à se regrouper. Cette zonation leur permet de comparer non seulement comment les cellules interagissent globalement, mais aussi comment ces interactions changent des régions tumorales clairsemées aux régions très denses.
Transformer les voisinages cellulaires en réseaux
Ensuite, les chercheurs traduisent les motifs spatiaux en réseaux, où chaque type cellulaire est un nœud et les liens représentent la force avec laquelle deux types cellulaires tendent à apparaître ensemble après avoir tenu compte des autres. En utilisant un cadre statistique bayésien qu’ils appellent ISPat (Informed Spatially aware Patterns), ils séparent les caractéristiques partagées par toutes les zones de celles spécifiques à une zone donnée. ISPat peut aussi intégrer des connaissances biologiques a priori quand elles sont disponibles, ce qui aide à stabiliser les estimations dans des jeux de données complexes. Des simulations montrent qu’ISPat peut retrouver de manière fiable des motifs connus et le fait beaucoup plus rapidement que les méthodes classiques, ce qui le rend pratique pour des études d’imagerie à grande échelle.
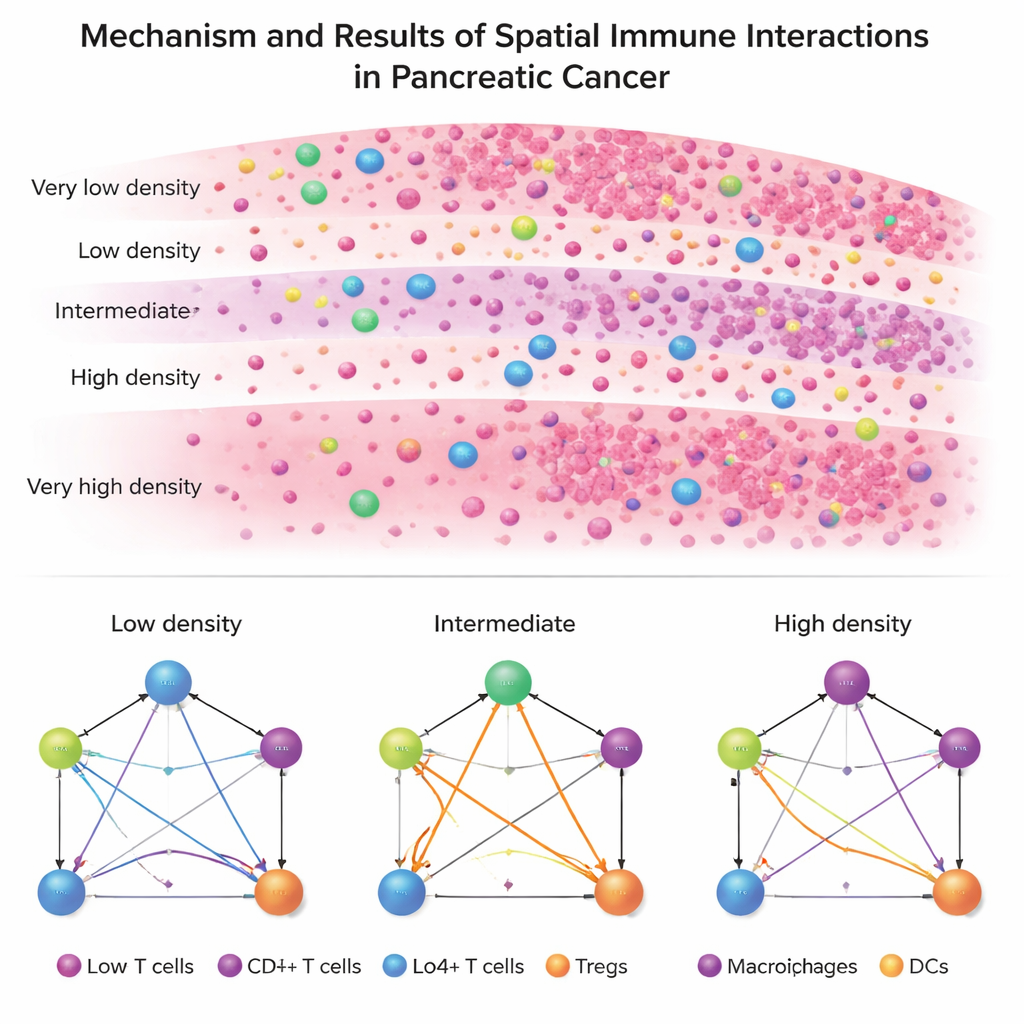
Deux maladies, deux architectures immunitaires
En appliquant ISPat aux données de patients, un contraste saisissant apparaît entre PDAC et IPMN. Le PDAC affiche une architecture immunitaire rigide et uniforme : dans presque toutes les zones, cellules tumorales, lymphocytes T auxiliaires, lymphocytes T cytotoxiques, lymphocytes T régulateurs et cellules présentatrices d’antigènes conservent pratiquement le même schéma de relations. Cela suggère un environnement immunosuppresseur stable et profondément enraciné, difficile à perturber. En revanche, l’IPMN montre beaucoup plus de variation d’une zone à l’autre, en particulier dans la manière dont les lymphocytes T régulateurs se connectent aux autres cellules immunitaires. Dans l’IPMN, ce sont les zones de densité intermédiaire — ni complètement saturées de cellules tumorales ni quasiment exemptes — qui présentent les remaniements les plus marqués des interactions immunitaires.
Points chauds pour l’évasion immunitaire et la thérapie
En creusant plus loin, l’étude identifie des paires spécifiques de types cellulaires dont les interactions diffèrent systématiquement entre PDAC et IPMN, particulièrement dans ces zones de densité intermédiaire. Beaucoup impliquent des lymphocytes T régulateurs, capables d’atténuer les attaques immunitaires, ainsi que des cellules présentatrices d’antigènes et des lymphocytes T cytotoxiques, qui déclenchent et exécutent les réponses anti-tumorales. Fait notable, les interactions favorisant la présentation d’antigènes et le meurtre direct de la tumeur, ainsi que celles renforçant la suppression immunitaire, divergent le plus fortement dans ces zones intermédiaires du gradient, et non pas dans les régions tumorales les plus extrêmes. Ce schéma suggère que le terrain décisif du contrôle immunitaire se situe dans les zones de transition où la tumeur et le système immunitaire sont encore en pleine négociation.
Ce que cela signifie pour les patients
Pour un non-spécialiste, la conclusion est que la position des cellules au sein d’une tumeur importe autant que leur identité. Le PDAC semble verrouiller une « configuration » immunitaire stable et suppressive, tandis que le paysage immunitaire de l’IPMN reste plus flexible et dépendant de la région. Ces empreintes spatiales pourraient devenir des biomarqueurs pour distinguer des tumeurs dangereuses de lésions précancéreuses et pour prédire quels patients pourraient bénéficier de certaines immunothérapies. Le cadre ISPat offre un outil général pour lire ces codes spatiaux dans de nombreuses maladies, soutenant un avenir où le traitement du cancer serait guidé non seulement par la génétique et les types cellulaires, mais aussi par la géographie fine des cellules dans la tumeur de chaque patient.
Citation: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
Mots-clés: cancer du pancréas, microenvironnement tumoral, imagerie spatiale, interactions immunitaires, oncologie de précision