Clear Sky Science · fr
Un système d’étiquette REC sans lysine pour les applications de biotinylation de proximité
Pourquoi les petites étiquettes sur les protéines comptent
À l’intérieur de chaque cellule, les protéines travaillent rarement seules — elles forment des partenariats changeants qui gouvernent la santé et la maladie. Pour étudier ces partenariats, les scientifiques attachent souvent de petites « étiquettes nominatives » aux protéines afin de pouvoir les suivre, les isoler d’un mélange ou les visualiser au microscope. Une méthode populaire appelée biotinylation de proximité permet de cartographier qui se trouve à proximité de qui dans la cellule, mais elle comporte un problème caché : nombre de ces étiquettes se modifient chimiquement et disparaissent effectivement au moment où elles sont le plus nécessaires. Cette étude présente un nouveau type d’étiquette, appelée étiquette REC, conçue pour rester détectable dans ces conditions exigeantes.
Un marqueur chimique pour les voisins protéiques
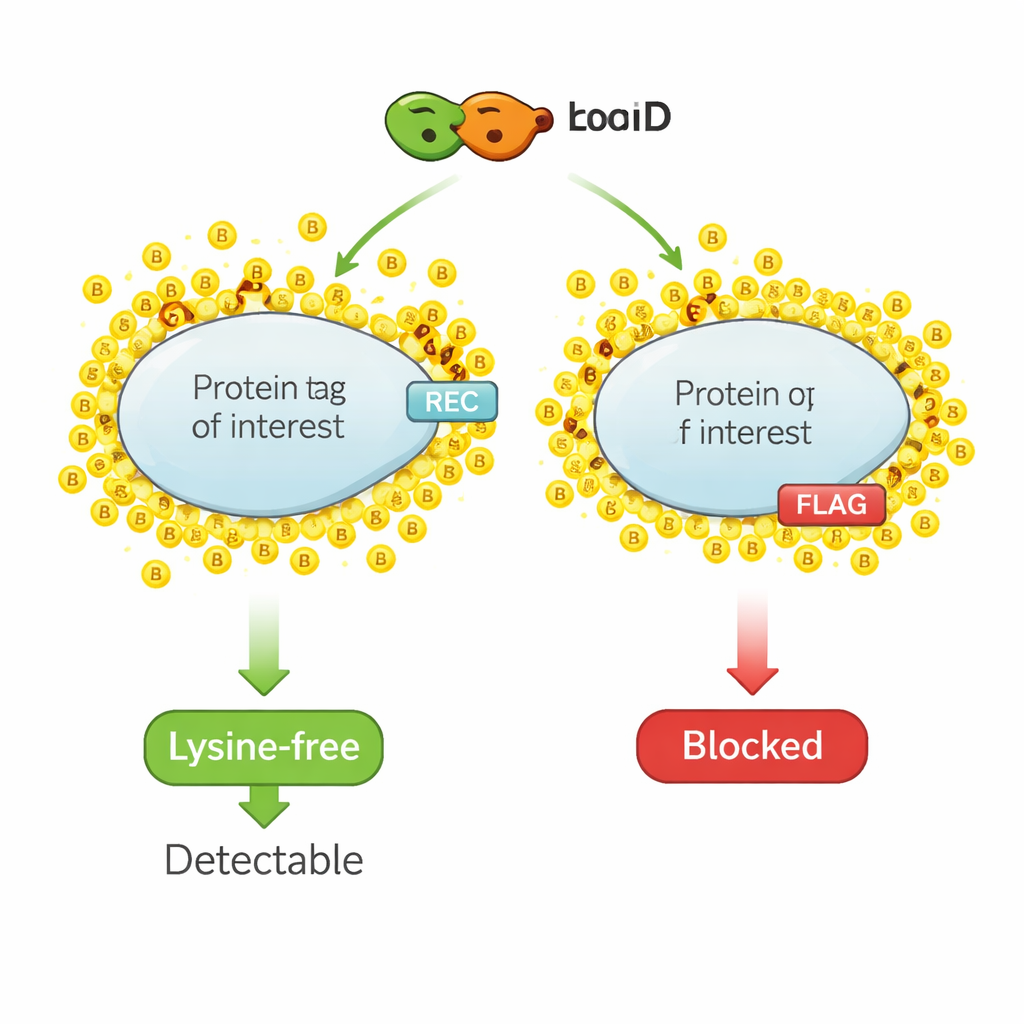
La biotinylation de proximité fonctionne comme un surligneur moléculaire. Une enzyme conçue, comme TurboID, est fusionnée à une protéine d’intérêt. Lorsqu’on ajoute de la biotine — une petite vitamine — TurboID attache rapidement des molécules de biotine aux protéines voisines. Les chercheurs récupèrent ensuite toutes les protéines marquées par la biotine et les identifient, obtenant ainsi une image du voisinage local de la protéine. Cependant, la même chimie qui étiquette les protéines voisines cible aussi les petits épitopes usuellement utilisés pour la détection, car ces étiquettes contiennent souvent de la lysine, un acide aminé qui est le principal site d’attaque pour la biotine. Lorsque les lysines de l’étiquette sont couvertes par la biotine, les anticorps ne peuvent plus reconnaître l’étiquette et le signal dans les méthodes de détection standard chute voire disparaît.
Concevoir une étiquette qui refuse la modification
Pour résoudre ce problème, les auteurs ont cherché à créer une nouvelle étiquette totalement dépourvue de lysine. Ils sont partis d’un fragment d’une protéine du parasite du paludisme appelée PfRipr5, qui présente peu de similarité aux protéines humaines, réduisant le risque de réactions croisées indésirables. En utilisant une méthode de criblage sur puce chez le lapin, ils ont généré 22 anticorps monoclonaux contre PfRipr5 et identifié un clone, nommé clone n° 6, présentant une affinité particulièrement forte et spécifique. En raccourcissant et en mutant systématiquement le fragment PfRipr5, ils ont réduit la cible de l’anticorps à une séquence de 11 acides aminés. Cette séquence minimale contenait une seule lysine, qu’ils ont remplacée par un acide aminé similaire, l’arginine. Remarquablement, l’anticorps liait toujours tout aussi bien. Cette séquence optimisée, sans lysine, a été nommée étiquette REC, et l’anticorps correspondant, l’anticorps REC.
Mettre l’étiquette REC à l’épreuve
L’équipe a ensuite testé si l’étiquette REC pouvait remplacer des étiquettes largement utilisées comme FLAG dans des techniques de laboratoire courantes. Lorsqu’elle était fusionnée à des protéines fluorescentes ou de signalisation et exprimée dans des systèmes sans cellules et dans des cellules mammifères, les protéines marquées REC étaient facilement détectées par immunoblot, par un test sensible en lumière sur plaque appelé AlphaScreen, et par immunomarquage dans les cellules. L’intensité de détection était similaire à celle de l’étiquette FLAG et à celle d’un autre système d’étiquette sans lysine (AGIA), et l’anticorps REC montrait très peu de bruit de fond sur une variété de lignées cellulaires humaines et simiesques. Fait important, l’étiquette fonctionnait qu’elle soit placée à l’extrémité N- ou C-terminale d’une protéine, et sur des protéines localisées dans des régions cellulaires diverses, y compris le noyau, les mitochondries, le réticulum endoplasmique et la membrane plasmique.
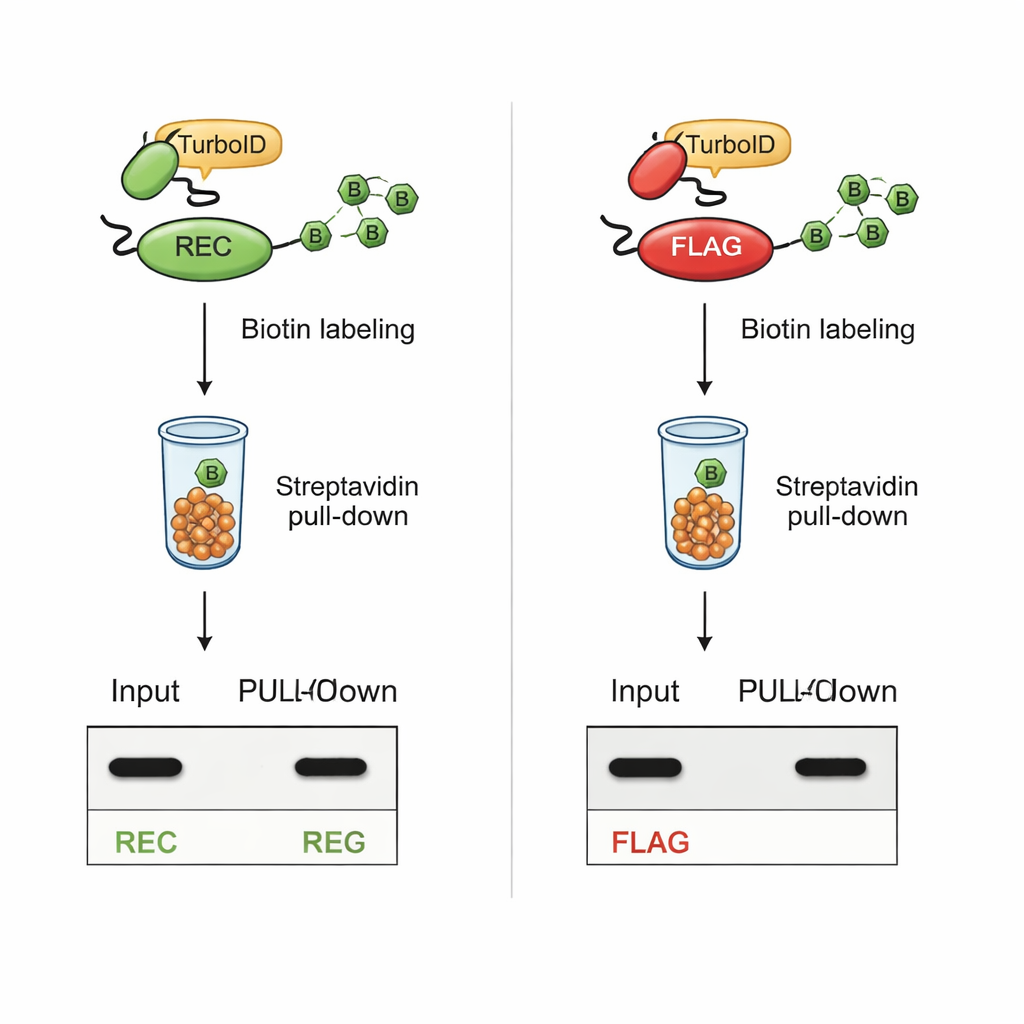
Rester visible lors d’un marquage intense
Le test critique était de savoir si REC resterait détectable après une biotinylation basée sur TurboID. Dans des cellules où TurboID était fusionné à des partenaires d’interaction connus, les protéines portant l’étiquette REC restaient clairement visibles tant dans les extraits cellulaires complets que dans la fraction purifiée marquée par la biotine. En revanche, les protéines portant l’étiquette FLAG classique perdaient leur signal FLAG une fois TurboID actif, bien que les protéines elles-mêmes soient encore présentes. Des expériences supplémentaires avec des peptides synthétiques ont montré que TurboID biotinyle directement les lysines de la séquence FLAG, empêchant physiquement l’accès des anticorps. L’étiquette REC, dépourvue de lysine, n’était pas affectée par TurboID et restait facile à détecter.
Ce que cela signifie pour les expériences futures
Pour les chercheurs explorant les réseaux protéiques à l’intérieur de cellules vivantes, l’étiquette REC offre un nouvel outil pratique : elle se comporte comme les étiquettes familières dans les essais quotidiens mais continue à fonctionner même lorsque des enzymes de marquage de proximité puissantes sont actives. Cela permet aux scientifiques de confirmer plus fiablement que leurs protéines marquées sont présentes et correctement capturées, et d’étudier d’autres modifications basées sur la lysine — telles que l’ubiquitination et l’acétylation — sans que l’étiquette elle-même n’interfère. En bref, REC est un petit changement de conception avec un fort impact, aidant à rendre les expériences de cartographie protéique complexes plus claires et plus fiables.
Citation: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Mots-clés: marquage de protéines, biotinylation de proximité, TurboID, interactions protéiques, étiquettes d’épitope