Clear Sky Science · fr
Interaction entre la méthylation de l’ADN d’ELMO1 et Med31 favorise l’EMT et la métaplasie intestinale induites par H. pylori via la polarisation M2
Pourquoi les bactéries de l’estomac comptent pour le risque de cancer
La plupart d’entre nous hébergent des milliards de bactéries dans le tube digestif, et l’une d’elles — Helicobacter pylori — peut vivre discrètement dans l’estomac pendant des décennies. Pour certaines personnes, cette infection est inoffensive, mais pour d’autres elle constitue la première étape vers un cancer gastrique, l’un des cancers les plus meurtriers au monde. Cette étude examine comment un petit changement chimique de l’ADN dans les cellules de l’estomac contribue à transformer une infection persistante en lésion précancéreuse et, finalement, en un environnement propice à la croissance tumorale.
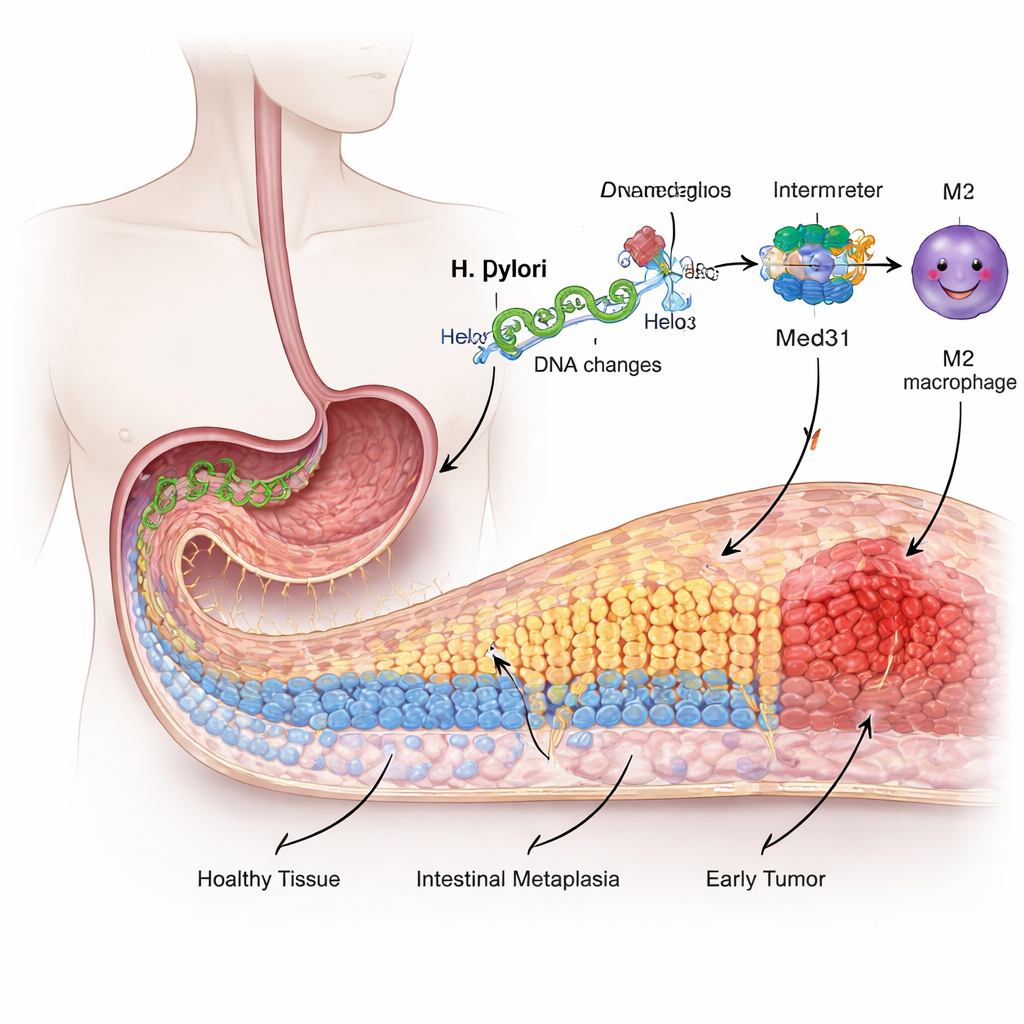
De la muqueuse protectrice à une transformation à risque
La surface interne de l’estomac est tapissée de cellules spécialisées adaptées à la gestion d’un acide puissant, et non à la digestion des aliments comme l’intestin. Après des années d’irritation et d’inflammation liées à H. pylori, certaines de ces cellules gastriques commencent à « se redécorer », adoptant des caractéristiques des cellules intestinales dans un processus appelé métaplasie intestinale. Ce changement est considéré comme un stade précancéreux. Les chercheurs ont utilisé une lignée cellulaire gastrique humaine pour modéliser l’infection et ont constaté que l’exposition à H. pylori rendait ces cellules plus proliférantes, plus mobiles et déclenchait des marqueurs de type intestinal — autant de signes que la muqueuse s’éloigne de son identité normale.
Petites étiquettes chimiques, grandes conséquences
Notre ADN peut être marqué par de petites étiquettes chimiques appelées groupes méthyle qui agissent comme des interrupteurs marche‑arrêt pour les gènes sans altérer le code génétique lui‑même. L’équipe s’est concentrée sur un gène nommé ELMO1, déjà connu pour son rôle dans le mouvement cellulaire et la dissémination tumorale. Ils ont montré que l’infection par H. pylori augmentait la méthylation du gène ELMO1 et, de manière quelque peu contre‑intuitive, stimulait son activité et ses niveaux protéiques dans les cellules gastriques. Lorsque les chercheurs ont utilisé un médicament qui élimine ces marques de méthylation, les cellules ont perdu une grande partie des changements induits par l’infection : elles se divisaient moins, se déplaçaient moins et présentaient moins de signes de métaplasie intestinale. Cela indique que la méthylation d’ELMO1 constitue un interrupteur crucial activé par la bactérie.
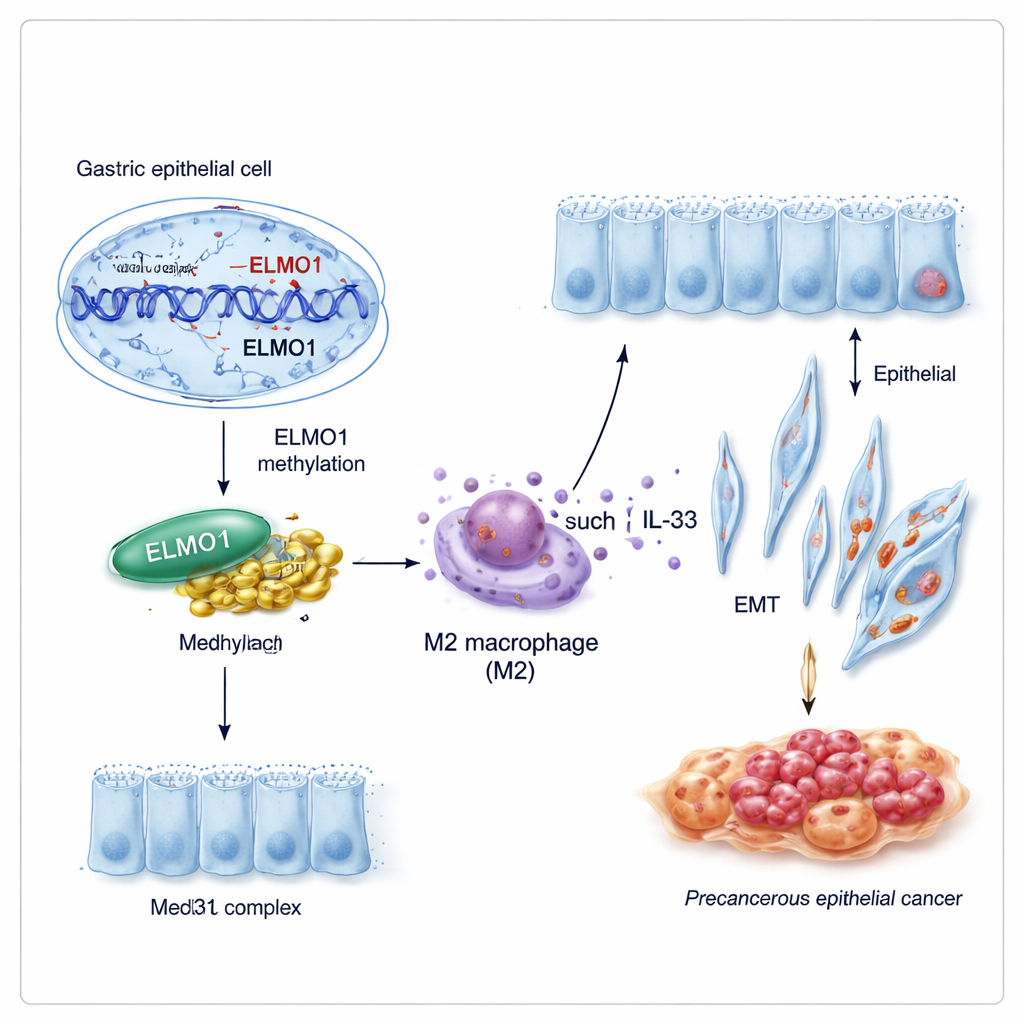
Un nouveau partenariat qui reprogramme le comportement cellulaire
Les gènes n’agissent que rarement seuls. Les chercheurs ont découvert que l’ELMO1 méthylé favorise une association avec une autre protéine, Med31, qui fait partie d’un vaste « panneau de contrôle » aidant à décider quels gènes une cellule active. Dans des conditions favorisant la méthylation de l’ADN, les niveaux d’ELMO1 augmentaient, Med31 augmentait aussi, et les deux se liaient physiquement, tandis qu’un partenaire connu plus ancien d’ELMO1, DOCK10, était mis à l’écart. Cette nouvelle équipe ELMO1–Med31 semble modifier le programme d’expression génique des cellules gastriques de manière à les pousser à adopter des traits intestinaux et à se comporter de façon plus agressive.
Comment les cellules immunitaires sont poussées à aider la tumeur
Le cancer ne se développe pas en isolation ; il croît au sein d’un voisinage complexe de cellules immunitaires et de soutien. L’étude montre que les cellules gastriques infectées et porteuses d’ELMO1 méthylé libèrent des niveaux plus élevés d’IL‑33, un signal qui incite les cellules immunitaires voisines appelées macrophages à adopter un état « M2 » favorable à la tumeur. Dans un système de coculture, les auteurs ont trouvé que les macrophages exposés à ces signaux basculaient fortement vers le phénotype M2 et, à leur tour, sécrétaient des facteurs qui poussaient de nouvelles cellules gastriques à devenir plus mobiles, plus invasives et plus proches des cellules intestinales. Les marqueurs de la transition épithélio‑mésenchymateuse — lorsque des cellules de revêtement stationnaires se transforment en cellules migrantes capables d’envahir — augmentaient fortement sous l’influence de ces macrophages M2.
Ce que cela signifie pour la prévention du cancer de l’estomac
Pris ensemble, les résultats décrivent une chaîne d’événements : l’infection par H. pylori modifie la méthylation de l’ADN d’ELMO1, cet ELMO1 modifié s’associe à Med31, les cellules infectées émettent des signaux qui convertissent les cellules immunitaires voisines en auxiliaires M2, et ces auxiliaires favorisent à la fois la métaplasie intestinale et un état cellulaire plus invasif. Pour les non‑spécialistes, l’idée clé est qu’une bactérie gastrique commune peut remodeler à la fois la muqueuse gastrique et la réponse immunitaire locale via des marques chimiques réversibles sur l’ADN. Mieux comprendre cette voie pourrait ouvrir la voie à de nouveaux tests sanguins détectant tôt des schémas de méthylation à risque, ainsi qu’à des médicaments visant à interrompre l’axe ELMO1–Med31–M2 avant qu’une infection chronique n’évolue vers un cancer gastrique.
Citation: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Mots-clés: cancer gastrique, Helicobacter pylori, méthylation de l’ADN, métaplasie intestinale, microenvironnement tumoral