Clear Sky Science · fr
Évaluation des bases biochimiques sous-jacentes à la résistance contre l’amyloïdose systémique
Quand de minuscules changements protéiques bloquent une accumulation mortelle
De nombreuses maladies inflammatoires chroniques, de la polyarthrite rhumatoïde à la tuberculose, peuvent déclencher une complication rare mais souvent fatale appelée amyloïdose AA systémique. Dans cette affection, une protéine sanguine normale s’accumule sous forme de fibres rigides qui obstruent les organes. Cette étude pose une question étonnamment encourageante : de petits changements naturels dans cette protéine peuvent-ils rendre certains animaux largement immunisés contre la maladie — et si oui, comment ?
La menace cachée des amas protéiques
L’amyloïdose AA débute par un signal inflammatoire dans le sang appelé amyloïde sérique A (SAA). Lors d’une inflammation sévère ou prolongée, les taux de SAA peuvent augmenter de milliers de fois par rapport à la normale. Chez certains humains et animaux, une partie de cette protéine se replie mal et s’empile en longues fibres, appelées fibrilles amyloïdes, qui se propagent dans des organes comme la rate et les reins. Avec le temps, ces fibres compromettent la fonction des organes. Pourtant, tous les individus ayant des taux élevés de SAA ne développent pas l’amyloïdose, et certaines souches de souris restent étonnamment résistantes même lorsqu’on les pousse vers la maladie en laboratoire. Comprendre pourquoi pourrait indiquer de nouvelles stratégies pour prévenir l’accumulation d’amyloïde chez l’homme.
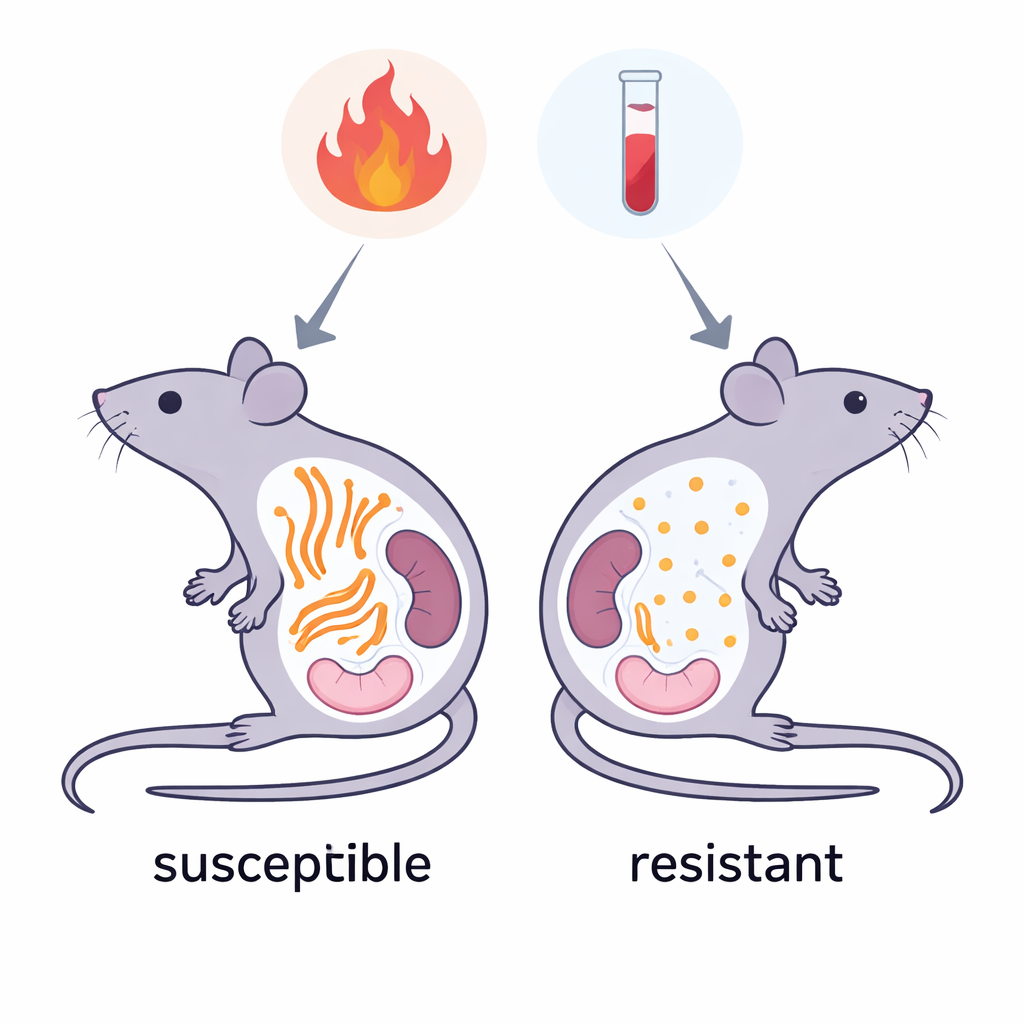
Des souris résistantes et leurs versions protéiques particulières
Chez la souris, la plupart des fibrilles amyloïdes AA proviennent d’une version de la SAA nommée SAA1.1, fortement associée à la maladie. Cependant, certaines souches produisent principalement des variantes légèrement modifiées, appelées SAA1.5 et SAA2.2, et ces souches développent rarement une amyloïdose AA systémique. Les protéines ne diffèrent que par une poignée de blocs constitutifs (acides aminés), mais ces différences se concentrent dans une région très compacte qui forme le cœur interne des fibres pathogènes. Les chercheurs ont proposé que ces petites différences n’empêchent pas les protéines de s’agréger en général, mais les empêchent d’adopter la forme fibreuse très spécifique qui est nuisible.
Mettre les protéines à l’épreuve en laboratoire
Pour tester cette idée, l’équipe a produit les trois variantes murines de SAA dans des bactéries et a observé leur comportement dans des expériences en éprouvette. Ils ont suivi la formation de fibrilles à l’aide d’un colorant fluorescent qui s’allume lorsque l’amyloïde se forme, et vérifié les structures avec des microscopes électroniques. La SAA1.1 liée à la maladie formait aisément de longues fibrilles droites. La SAA2.2 pouvait aussi former des fibrilles, mais elles étaient plus épaisses, plus torsadées et structurellement plus hétérogènes, et elles n’entraînaient pas le même signal coloré intense. La SAA1.5, en revanche, n’a pas réussi à former des fibrilles dans les conditions testées. Lorsque les scientifiques ont ajouté de minuscules échantillons de vraies fibrilles pathogènes prélevées sur des rates de souris malades en guise de « graines », la SAA1.1 a rapidement allongé de nouvelles fibrilles qui copiaient étroitement la structure de l’original, comme un prion. Fait frappant, la SAA1.5 et la SAA2.2 n’ont pas du tout été recrutées par ces graines ex vivo ; les fibrilles isolées ne pouvaient pas les convertir en la forme pathogène.
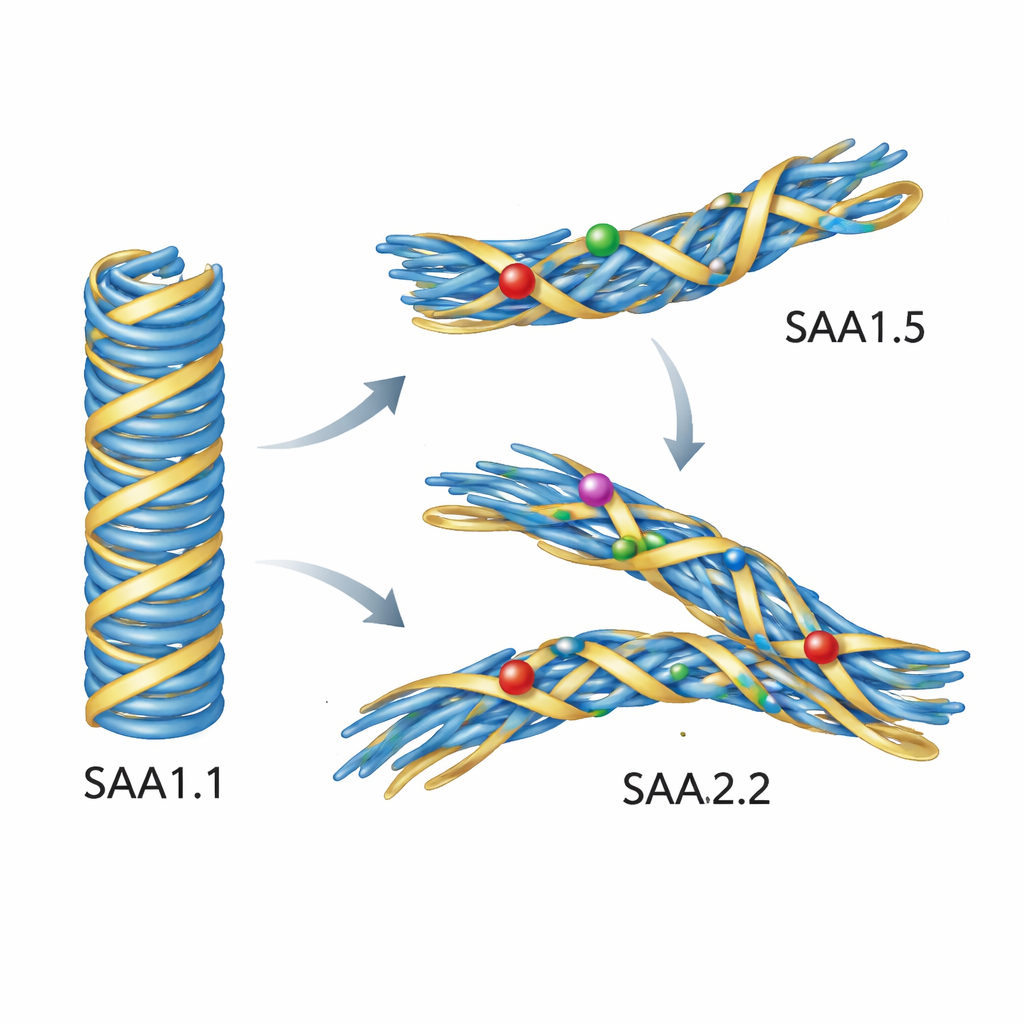
Des simulations révèlent pourquoi les protéines mutantes refusent la mauvaise forme
Les expériences seules ne pouvaient pas montrer précisément ce qui dysfonctionne au niveau atomique, aussi les auteurs ont eu recours à des simulations informatiques détaillées. Ils sont partis d’une structure haute résolution d’une fibrille AA pathogène de souris construite à partir de SAA1.1, puis ont substitué par calcul les séquences SAA1.5 et SAA2.2. Lorsqu’ils ont simulé ces fibrilles en eau à température corporelle, le modèle basé sur SAA1.1 est resté remarquablement stable. En revanche, les fibrilles construites à partir de SAA1.5 ou SAA2.2 ont bougé et se sont déformées. Une boucle clé dans le cœur s’est déplacée vers l’extérieur et a relâché son contact avec le segment initial de la protéine, et plusieurs chaînes latérales ont basculé en de nouvelles orientations. Ces réarrangements subtils ont perturbé l’emboîtement serré qui définit le repli pathogène. Autrement dit, les séquences variantes pouvaient former des fibrilles en général — mais elles ne pouvaient pas s’ajuster confortablement au plan de construction de la fibrille AA pathogène.
Comment le design de la nature indique des pistes thérapeutiques
En somme, le travail montre que les souches de souris « résistantes à l’amyloïde » ne sont pas protégées parce que leur SAA ne peut pas s’agréger du tout. Au contraire, leurs versions de la SAA sont structurellement incompatibles avec la forme fibrillaire particulière qui provoque l’amyloïdose AA systémique. Les protéines peuvent toujours s’assembler, mais elles le font en formes alternatives apparemment bénignes. Des mutations protectrices similaires sont connues dans d’autres maladies de mauvais repliement protéique, y compris certains cas de prionose et d’Alzheimer. Cela suggère un principe plus large : modifier une protéine susceptible de provoquer une maladie pour qu’elle ne puisse plus adopter son architecture toxique — tout en conservant sa fonction normale — peut suffire à prévenir la maladie. À long terme, des thérapies inspirées de ces variantes naturelles « résistantes », ou de courts fragments dérivés de celles-ci, pourraient aider à orienter les protéines loin des repliements dangereux vers des conformations inoffensives.
Citation: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
Mots-clés: Amyloïdose AA, amyloïde sérique A, mauvais repliement des protéines, résistance aux amyloïdes, modèles murins