Clear Sky Science · fr
Modélisation et vérification expérimentale de la précipitation de nanoparticules de polycaprolactone
Pourquoi de minuscules sphères plastiques comptent pour la médecine
Imaginez enfermer un médicament puissant dans une particule si petite qu’elle peut se faufiler dans les vaisseaux sanguins et libérer sa charge exactement là où elle est nécessaire. Ces particules, appelées nanoparticules polymères, sont au cœur de nombreux traitements et outils d’imagerie émergents. Mais les fabriquer avec une taille correcte et reproductible est étonnamment difficile. Cette étude montre comment un modèle informatique simple fondé sur la physique peut prédire et ajuster la taille d’une nanoparticule biodégradable largement utilisée, ce qui pourrait réduire de plusieurs années les essais‑erreurs dans le développement de nouvelles nanomédecines.
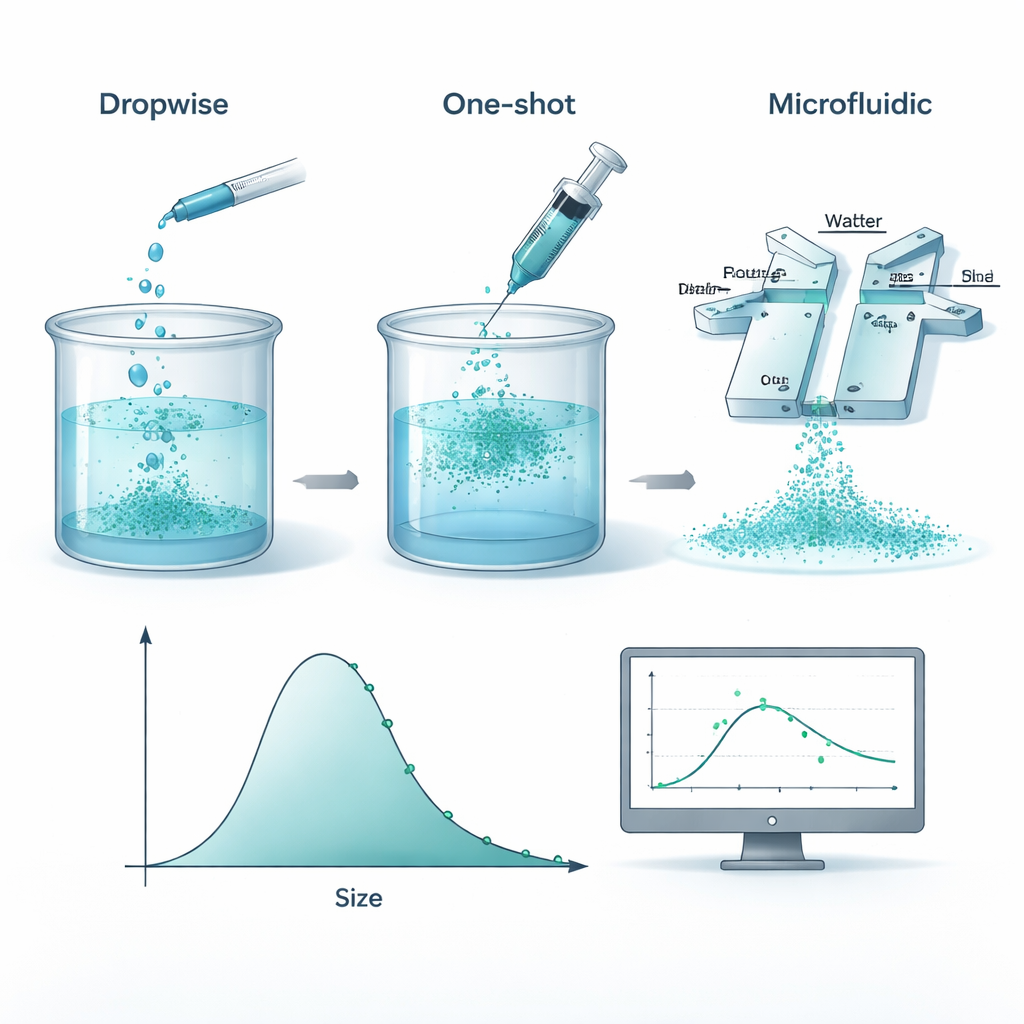
Du mélange de cuisine à la précision de laboratoire
Pour créer ces nanoparticules, les chercheurs dissolvent un plastique biodégradable appelé polycaprolactone (PCL) dans un solvant organique puis le mélangent à de l’eau, de sorte que le polymère « sorte » de la solution et forme de minuscules sphères. L’équipe a comparé trois méthodes pratiques : ajouter lentement la solution de polymère goutte à goutte, la verser d’un seul coup, ou faire passer les deux liquides dans une puce microfluidique où ils se rencontrent dans des canaux étroits. Dans des conditions soigneusement contrôlées, les trois approches ont produit des particules avec des tailles moyennes et des dispersions de taille très similaires. Cela signifie que, au moins dans les plages étudiées, ce qui compte plus que le dispositif de mélange est ce que vous mettez dedans — les quantités de polymère et de stabilisant — plutôt que la façon dont vous agitez.
Comment la viscosité et les molécules auxiliaires façonnent les particules
Les chercheurs ont ensuite exploré comment les ingrédients de la recette contrôlent la taille finale des particules. Augmenter la quantité de PCL dans la phase organique rend ce liquide plus épais, c’est‑à‑dire plus visqueux. Pensez à essayer de mélanger du sirop dans de l’eau plutôt que du jus : un sirop plus épais se brise en gouttelettes plus grosses. Ici, des solutions de polymère plus visqueuses ont conduit à des nanoparticules plus grandes et à des distributions de taille légèrement plus larges. L’ajout d’un second solvant, l’éthanol, a aidé à maintenir la stabilité du procédé même pour des teneurs en polymère très élevées, mais au prix de particules plus grosses à la concentration maximale. Un second ingrédient, un tensioactif appelé Pluronic F‑127, agit comme un agent anti‑agglomérant moléculaire. À faibles concentrations de tensioactif, les particules ont tendance à se heurter et à coller, devenant plus grosses et moins uniformes. À mesure que la concentration en tensioactif augmente, il enrobe les surfaces particulaires, empêche leur fusion et donne des nanoparticules plus petites et plus stables — jusqu’à un certain point où les gains deviennent modestes et la distribution de tailles peut même se diversifier.
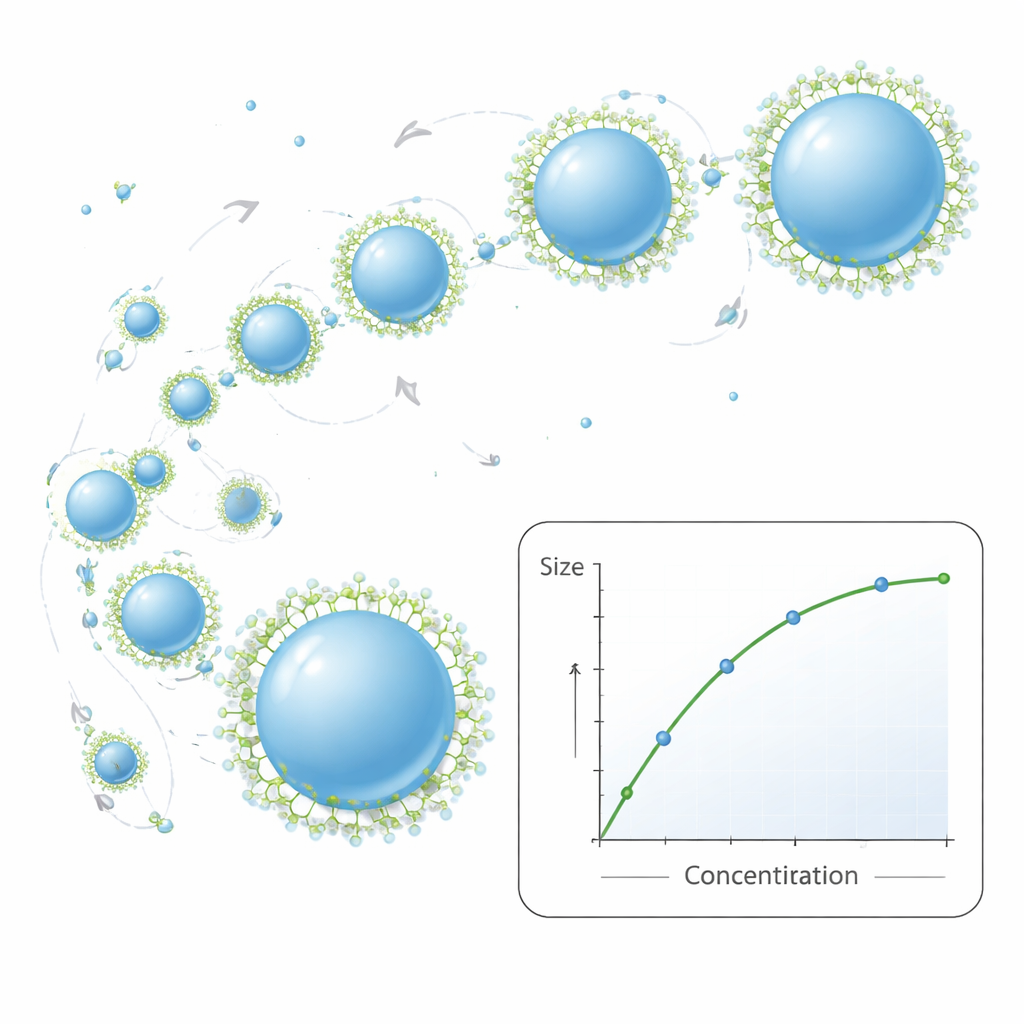
Une règle simple de croissance qui correspond à la réalité
Le cœur du travail est un modèle mathématique compact qui décrit comment les nanoparticules croissent après leur apparition initiale. Il traite leur mouvement comme un brassage aléatoire dans le liquide, où les collisions conduisent parfois à la fusion de deux particules en une plus grosse. Les modèles antérieurs supposaient que chaque rencontre entraînait une fusion instantanée et la formation de sphères parfaites. Le nouveau modèle ajoute deux éléments réalistes : d’abord, il permet un temps fini pour que deux particules en contact se relâchent d’une forme allongée vers une unique sphère ; ensuite, il laisse les molécules de tensioactif « bloquer » progressivement la surface, ralentissant ou arrêtant les fusions ultérieures. Avec seulement quelques paramètres mesurables — tels que la température, la viscosité du liquide et la concentration initiale en polymère — le modèle prédit comment la taille moyenne des particules doit varier en fonction des conditions de formulation. Sur de nombreuses expériences, les tailles prédites correspondaient étroitement à celles mesurées par diffusion de la lumière, tout en capturant les tendances générales de l’élargissement de la distribution de tailles.
Utiliser le modèle comme outil de conception
Pour tester l’utilité de l’approche, l’équipe a inversé le problème : au lieu de demander au modèle d’expliquer des données passées, elle lui a demandé de proposer des recettes devant produire trois tailles et degrés d’uniformité nanoparticulaires spécifiques. Ils ont ensuite préparé ces formulations « conçues » en laboratoire. Les diamètres mesurés différaient des cibles de seulement 1 à 7 % — bien dans la variation expérimentale habituelle — montrant que le modèle peut orienter de manière fiable les choix de formulation. Les prédictions sur la largeur de la distribution de tailles étaient moins exactes, mais suffisantes pour distinguer des populations relativement resserrées de populations plus étalées. Comparé à des méthodes de simulation lourdes qui suivent chaque molécule ou chaque tourbillon d’écoulement, ce modèle épuré s’exécute rapidement sur des ordinateurs modestes et est facile à adapter à d’autres polymères et configurations de traitement.
Ce que cela signifie pour la nanomédecine future
Pour les non‑spécialistes, le message clé est que la fabrication de nanoparticules utiles n’a plus à reposer uniquement sur des essais laborieux et de l’erreur en laboratoire. En capturant la physique essentielle de la façon dont de petites gouttelettes plastiques se déplacent, se percutent et sont protégées par des tensioactifs, ce travail fournit une « carte » pratique reliant les choix de formulation — quantité de polymère, mélange de solvants, quantité de stabilisant — à la taille finale des particules. Parce que le PCL est un matériau biodégradable courant utilisé en délivrance de médicaments, en implants et en agents d’imagerie, ce modèle pourrait aider les chercheurs à concevoir des nanomédecines plus sûres et plus efficaces, plus rapidement et avec moins de matériaux gaspillés. Les mêmes principes peuvent être étendus à d’autres polymères, apportant plus de prévisibilité et d’efficacité au domaine des thérapies à l’échelle nanométrique.
Citation: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Mots-clés: nanoparticules polymères, nanoprécipitation, libération de médicaments, modélisation numérique, polycaprolactone