Clear Sky Science · fr
La nicorandil atténue la douleur neuropathique et inflammatoire via les voies TNF-α, IL6/MAPKERK1/2 et NO/cGMP
Pourquoi il est important d'atténuer la douleur nerveuse
Des millions de personnes souffrent de douleurs brûlantes, lancinantes ou picotantes qui persistent longtemps après la guérison d'une blessure. Cette douleur « neuropathique » peut résister aux analgésiques courants et s'accompagner d'effets indésirables liés à un traitement prolongé. L'étude résumée ici examine si la nicorandil — un médicament cardiaque déjà administré aux patients souffrant d'angine — pourrait également calmer des voies de la douleur trop actives dans le système nerveux, et comment elle agit au niveau cellulaire.
Un médicament cardiaque exploré en recherche sur la douleur
La nicorandil est prescrite pour traiter l'angine car elle détend les vaisseaux sanguins. Elle agit par deux principaux mécanismes : le don de faibles quantités de monoxyde d'azote, une molécule de signalisation, et l'ouverture de certains canaux potassiques cellulaires. Des travaux antérieurs chez l'animal laissaient entendre que la nicorandil peut aussi réduire la douleur en agissant sur des récepteurs nerveux impliqués dans la sensation de chaleur et celle des piments, et en mobilisant le système opioïde endogène. Dans la présente étude, les auteurs ont cherché à cartographier ce qui se passe en aval de ces premiers effets, en se concentrant sur l'inflammation, le stress oxydatif (une sorte de « rouille » chimique) et des voies de signalisation spécifiques à l'intérieur des neurones sensoriels.
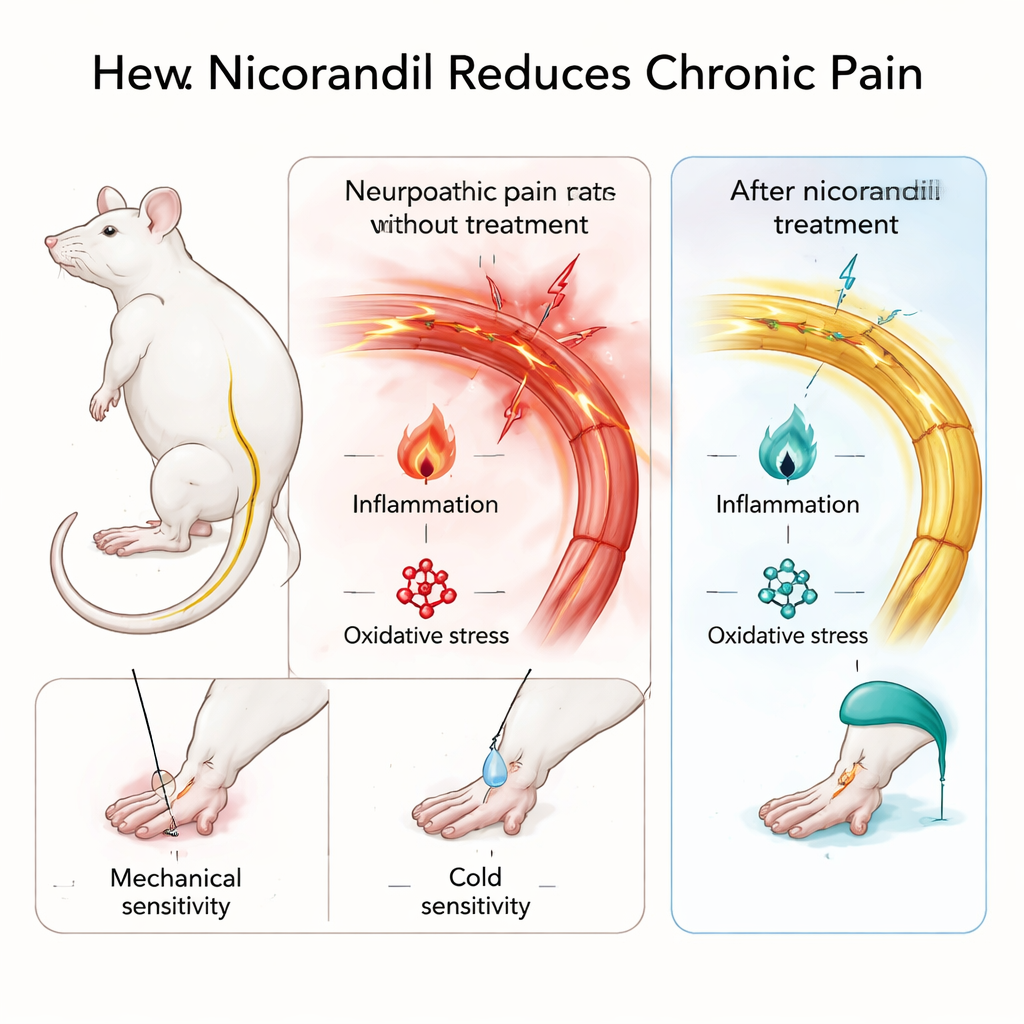
Tester la nicorandil dans des modèles de douleur persistante
Pour reproduire une douleur nerveuse durable, l'équipe a légèrement ligaturé le nerf sciatique chez des rats, une procédure classique qui provoque une sensibilité au toucher et au froid semblable à la douleur neuropathique humaine. Ils ont aussi utilisé le test de la formol, où un irritant chimique doux est injecté dans une patte pour induire une douleur inflammatoire prolongée et bien définie. Les rats ont reçu de la nicorandil par voie orale à deux doses, et les scientifiques ont mesuré leurs réactions au toucher léger et au froid sur la patte lésée, ainsi que le nombre de lèchements ou de sursauts après la formol. Il est important de noter que la nicorandil n'a pas rendu les animaux somnolents ou instables dans un test de champ ouvert, ce qui suggère que la réduction du comportement douloureux n'était pas simplement due à une sédation.
Atténuer les « signaux d'alarme » chimiques
La nicorandil a clairement réduit à la fois la douleur induite par la lésion nerveuse et la douleur provoquée par la formol. Les rats traités toléraient mieux le toucher et le froid et montraient moins de sursauts et des temps de lèchement plus courts. Les analyses sanguines ont montré que la nicorandil diminuait les niveaux de puissants médiateurs inflammatoires — le facteur de nécrose tumorale alpha (TNF-α) et l'interleukine-6 (IL‑6) — ainsi que la cyclooxygénase‑2, une enzyme qui participe à la production de prostaglandines liées à la douleur. Elle a également réduit le malondialdéhyde, un marqueur du stress oxydatif, indiquant moins de lésions chimiques des membranes cellulaires. Au microscope, les nerfs des animaux traités à la nicorandil semblaient en meilleures conditions : on observait moins de dommages structuraux et d'œdème dans le nerf sciatique et dans le ganglion spinal dorsal, ensemble des corps cellulaires des neurones sensoriels.
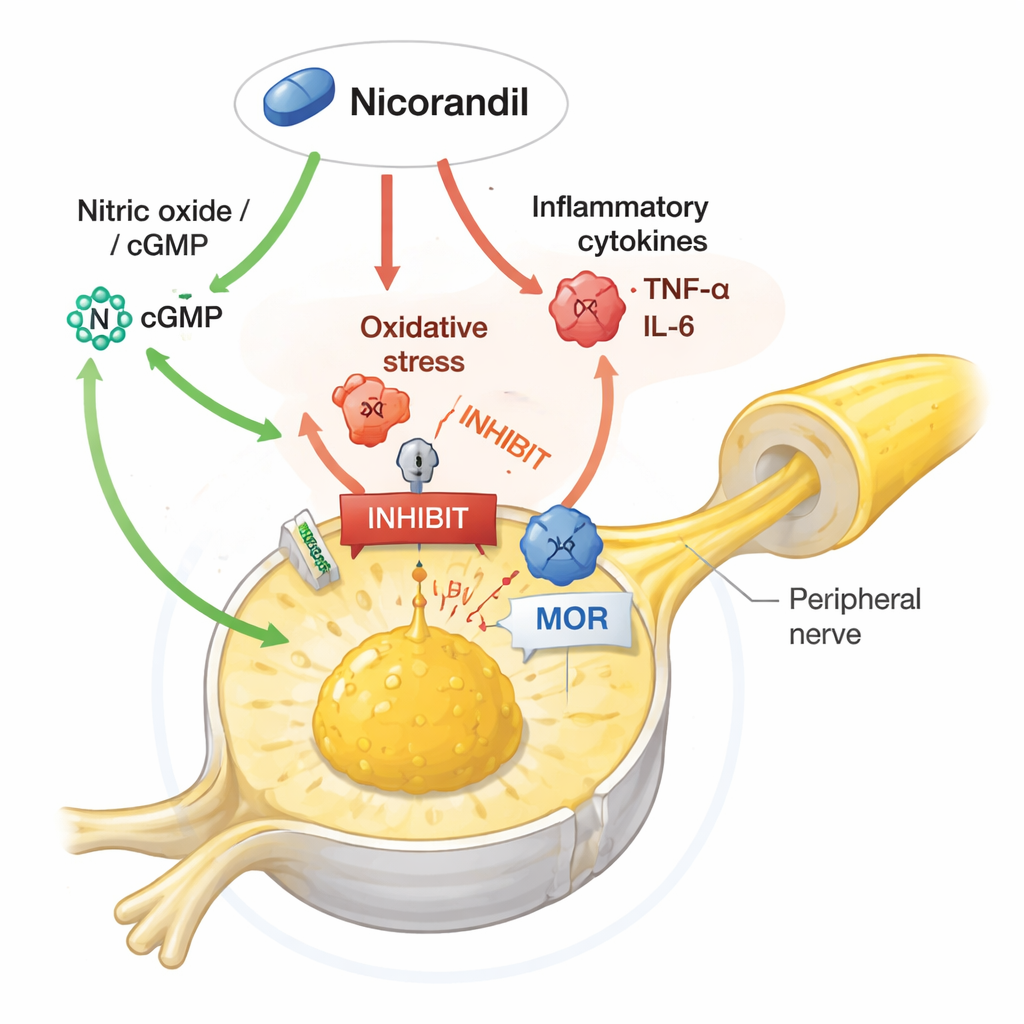
Démêler le réseau de signalisation au sein des neurones douloureux
L'étude est allée plus loin en sondant quelles voies moléculaires étaient nécessaires aux effets bénéfiques de la nicorandil. Lorsque les chercheurs ont administré des drogues qui renforcent la voie du monoxyde d'azote ou augmentent le GMP cyclique (un messager lié au monoxyde d'azote), ils ont partiellement atténué la capacité de la nicorandil à réduire la douleur et à normaliser certaines protéines clés. La nicorandil empêchait l'augmentation habituelle d'ERK1/2, membre de la famille des MAP kinases qui amplifie les signaux de douleur, et réduisait les niveaux de TRPV1, un canal qui rend les neurones plus sensibles à la chaleur et aux irritants chimiques. La stimulation de la signalisation du monoxyde d'azote ou du GMP cyclique inversait ces changements protecteurs, tandis que le blocage des enzymes produisant le monoxyde d'azote renforçait parfois l'effet antalgique de la nicorandil. De façon surprenante, le blocage des canaux potassiques que la nicorandil ouvre classiquement n'a pas éliminé ses effets antinociceptifs, ce qui suggère que, dans ce contexte, son pouvoir analgésique repose davantage sur la modulation du monoxyde d'azote, du stress oxydatif, de l'inflammation et des voies opioïdes que sur son action vasculaire classique.
Ce que cela pourrait signifier pour les personnes souffrant de douleur
Au total, les résultats présentent la nicorandil comme un modulateur de la douleur à cibles multiples : elle calme des voies nerveuses hyperactives en réduisant les dommages oxydatifs et les médiateurs inflammatoires, en silencant ERK1/2 et TRPV1 à l'intérieur des neurones sensoriels, et en interagissant avec la voie du monoxyde d'azote et le système opioïde endogène. Bien que ces résultats proviennent de modèles animaux et d'une administration à court terme, ils suggèrent qu'un médicament déjà utilisé en clinique pour les maladies cardiaques pourrait un jour être repositionné ou adapté pour traiter des douleurs neuropathiques et inflammatoires difficiles. Des études futures chez l'humain seront nécessaires pour déterminer les doses sûres, les effets à long terme et si les mêmes mécanismes protecteurs opèrent dans les nerfs humains.
Citation: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Mots-clés: douleur neuropathique, nicorandil, inflammation, stress oxydatif, signalisation du monoxyde d'azote