Clear Sky Science · fr
Déséquilibre de l’homéostasie du zinc réduit les niveaux d’acétylation des histones dans des cellules normales et tumorales
Quand un métal utile devient nuisible
Le zinc est surtout connu comme le nutriment présent dans les multivitamines qui soutient notre système immunitaire et la cicatrisation. Mais à l’intérieur des cellules, le zinc doit être maintenu dans une plage « juste comme il faut ». Cette étude montre que lorsque les niveaux de zinc dans les cellules deviennent trop élevés, ils peuvent silencieusement éteindre des gènes importants en resserrant l’empaquetage de l’ADN, et même pousser les cellules vers un processus d’auto‑nettoyage appelé autophagie. Comme les compléments de zinc, certains ingrédients anti‑pelliculaires et des médicaments anticancéreux expérimentaux peuvent tous modifier les niveaux de zinc, comprendre ce système de contrôle caché importe pour la santé quotidienne et pour des thérapies futures.
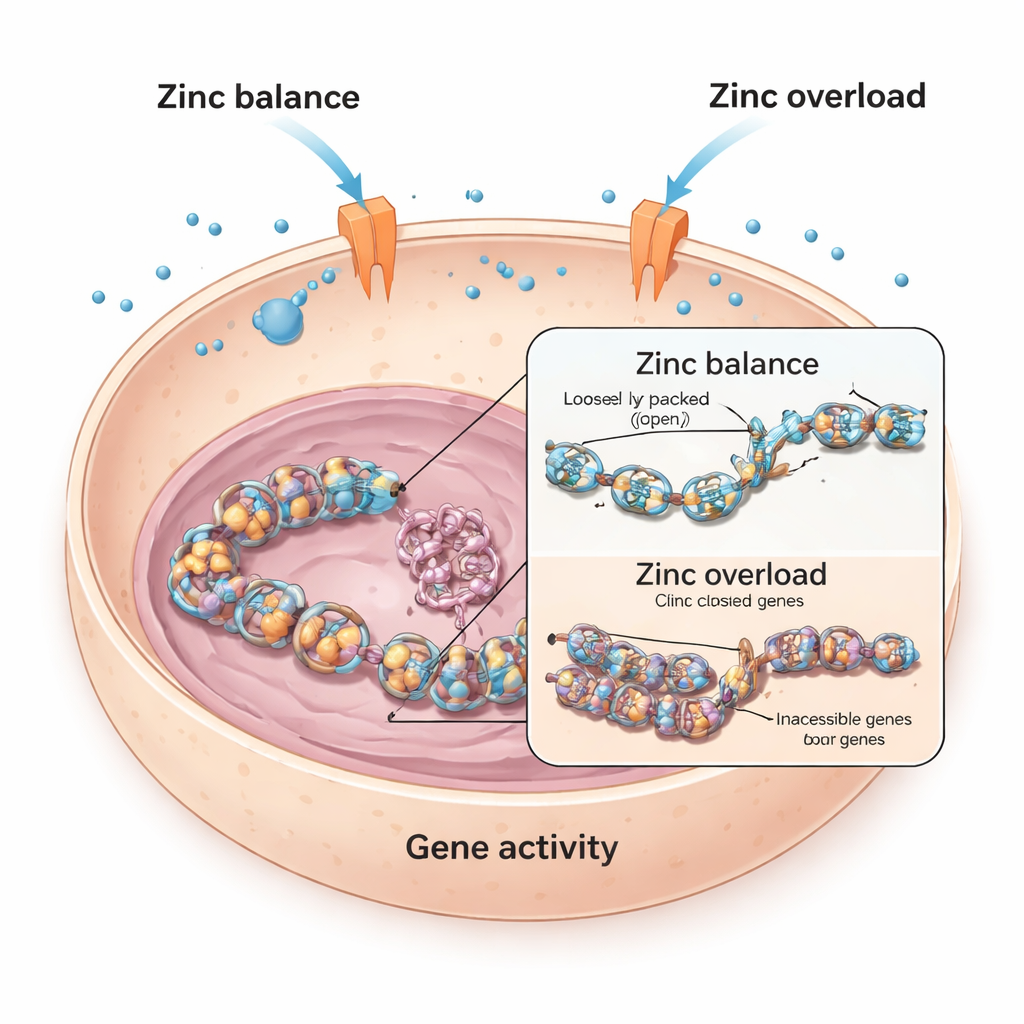
Équilibrer le zinc à l’intérieur des cellules vivantes
Chaque cellule dépend du zinc, qui aide des milliers de protéines à accomplir leur fonction. Pour éviter à la fois la pénurie et la surcharge, les cellules utilisent des « portes » spéciales dans leurs membranes, appelées transporteurs de zinc, pour faire entrer et sortir le zinc. Les chercheurs ont commencé par des cellules musculaires cardiaques de souris et d’humain, se demandant ce qui se passe quand ces cellules sont exposées à un excès de zinc. Ils ont constaté que dans les cellules cardiaques de souris, des niveaux élevés de zinc réduisaient fortement l’activité d’un gène clé lié au cœur appelé Bmp4, qui aide à guider le développement et la fonction cardiaques. En revanche, les cellules cardiaques humaines étaient beaucoup moins affectées, suggérant que différentes cellules se défendent contre la surcharge en zinc de manières distinctes.
Comment le zinc resserre l’empaquetage de l’ADN
Pour découvrir comment le zinc silencie des gènes comme Bmp4, l’équipe a étudié les histones, ces protéines enrouleuses autour desquelles l’ADN est enroulé. Quand de petites étiquettes chimiques appelées groupes acétyle sont ajoutées aux histones, l’ADN devient plus lâche et plus accessible ; quand ces étiquettes sont retirées, l’ADN se compacte et les gènes sont plus difficiles à activer. L’étude a montré qu’un excès de zinc dans les cellules cardiaques de souris entraînait une baisse de l’acétylation des histones à un site spécifique (connu sous le nom de H3K9), en parallèle de la chute d’activité de Bmp4. Des médicaments qui bloquent les enzymes déacétylantes des histones pouvaient annuler l’effet du zinc et restaurer Bmp4, ce qui suggère que le zinc faisait pencher l’équilibre de ce système d’étiquetage chimique.
Trop de zinc à l’intérieur, pas seulement à l’extérieur
Il s’est avéré que l’étape cruciale était le zinc présent dans le cytoplasme aqueux de la cellule, pas seulement dans le milieu environnant. En utilisant une sonde fluorescente qui s’allume en présence de zinc libre, les chercheurs ont observé une montée de zinc à l’intérieur des cellules cardiaques de souris après traitement. Lorsqu’ils ont utilisé une navette de zinc pour forcer l’entrée de zinc directement dans les cellules, ils ont constaté la même baisse d’acétylation des histones et d’activité génique, même avec des concentrations bien plus faibles de zinc dans le milieu externe. Chez les cellules cardiaques humaines, en revanche, les transporteurs à la membrane cellulaire s’ajustaient rapidement : certains importateurs de zinc se mettaient en pause et les exportateurs augmentaient, empêchant une forte hausse du zinc interne et protégeant l’acétylation des histones. Les cellules cardiaques de souris présentaient une réponse des transporteurs plus « mal câblée », laissant affluer davantage de zinc et perturbant le contrôle des gènes.
Du contrôle des gènes à l’auto‑nettoyage dans cellules normales et tumorales
Les investigateurs se sont ensuite demandé si ce resserrement de l’empaquetage de l’ADN induit par le zinc est propre aux cellules cardiaques. Ils ont testé plusieurs types de cellules humaines normales et des lignées tumorales de l’estomac, de l’utérus et de l’ovaire. Lorsque le zinc était laissé s’accumuler à l’intérieur à l’aide d’une navette, presque toutes ces cellules montraient une baisse nette de l’acétylation des histones. Dans certaines cellules tumorales, comme les cellules du cancer gastrique, cela se produisait à des doses de zinc particulièrement faibles, laissant penser que certains cancers sont exceptionnellement sensibles au déséquilibre en zinc. L’équipe a aussi relié la baisse d’acétylation à l’autophagie, un processus où les cellules recyclent des éléments usés. Des augmentations modérées du zinc intracellulaire stimulaient l’autophagie, mais un zinc très élevé finissait par l’affaiblir, ce qui suggère une fenêtre étroite où le zinc pourrait être utilisé pour régler finement cette voie d’auto‑nettoyage.
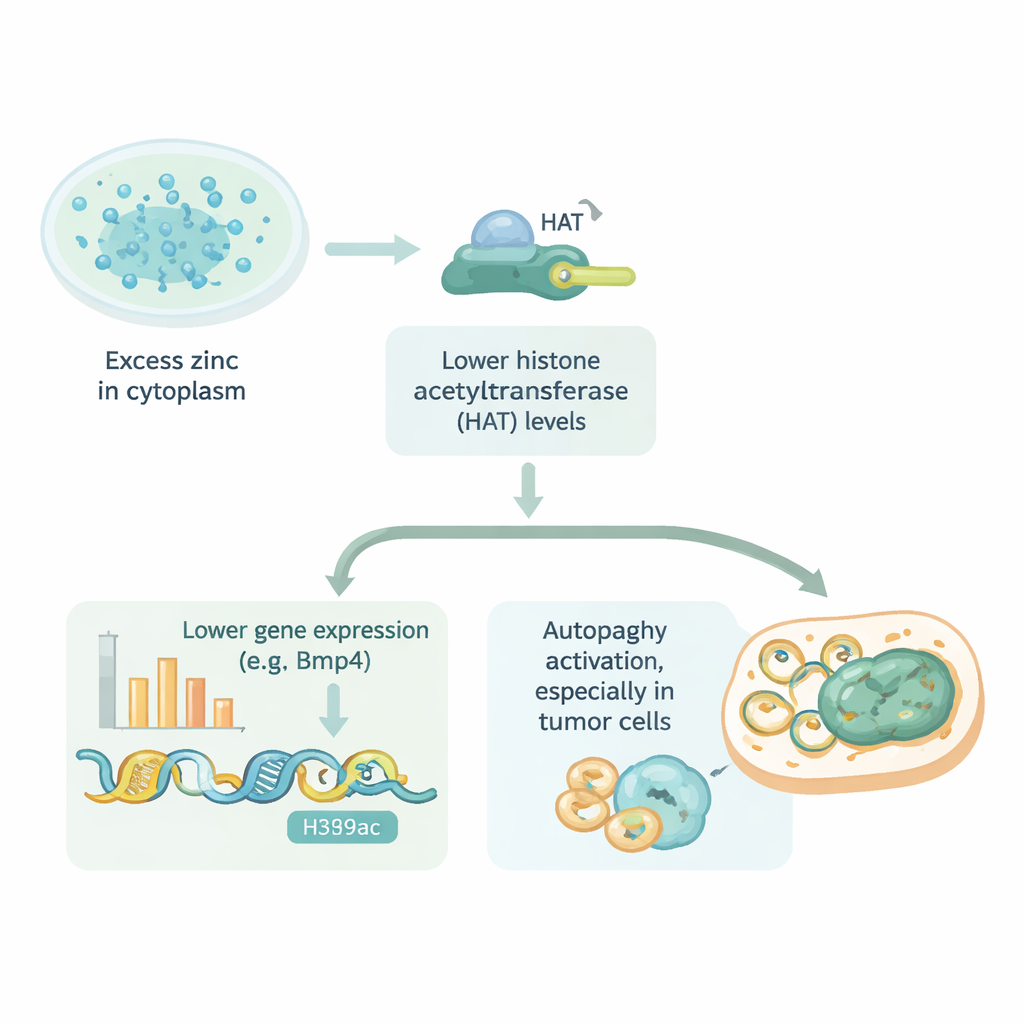
Que cela signifie pour la santé et le traitement
En termes simples, ce travail révèle qu’un excès de zinc à l’intérieur des cellules peut réduire l’expression des gènes en rendant l’ADN moins accessible, et que cette même voie peut influencer l’activité d’autonettoyage des cellules. L’effet ne se limite pas aux cellules cardiaques ; il apparaît dans différents types de cellules normales et tumorales, bien que certaines sachent mieux se défendre contre la surcharge en zinc que d’autres. Ces découvertes suggèrent que les minuscules « portes » transporteurs de zinc dans les membranes cellulaires pourraient être des cibles médicamenteuses prometteuses — soit pour protéger les tissus sains des dommages liés au zinc, soit pour pousser des cellules tumorales vulnérables vers la mort. Bien que les résultats proviennent d’expériences en culture cellulaire, ils offrent un nouvel éclairage sur la manière dont un nutriment du quotidien peut façonner l’activité génétique et la maladie lorsque son équilibre délicat est perturbé.
Citation: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Mots-clés: homéostasie du zinc, régulation des gènes, acétylation des histones, autophagie, cellules cancéreuses