Clear Sky Science · fr
Distribution variable des BMP dans différentes couches périostées contribuant à l’ostéoinductivité inconstante des produits à base de DBM
Pourquoi les matériaux de réparation osseuse ne fonctionnent pas toujours de la même façon
Quand des chirurgiens comblent un fragment d’os cassé ou manquant, ils ont souvent recours à la matrice osseuse déminéralisée (DBM) — de l’os de donneur transformé, censé déclencher la formation de nouvel os. Or, dans la pratique, ces produits peuvent se comporter très différemment, même s’ils semblent similaires sur l’étiquette. Cette étude pose une question simple mais importante : ces différences pourraient‑elles venir du fait que les protéines de réparation situées dans l’os sont réparties de façon inégale selon les couches d’un même os, et selon la manière dont on les mesure en laboratoire ?
La promesse des propres protéines réparatrices de l’os
La DBM agit parce qu’elle transporte des molécules naturelles formatrices d’os appelées protéines morphogénétiques osseuses, ou BMP. Ces protéines signalent aux cellules souches voisines de se différencier en cellules cartilagineuses et osseuses, aidant la zone endommagée à se reconstruire. Des travaux antérieurs ont montré que les préparations de DBM contenant davantage de BMP tendent à former plus d’os, mais ont aussi révélé une très grande variation entre produits commerciaux et même entre lots du même produit. Les auteurs de cette étude ont émis l’hypothèse qu’une source négligée de cette variation était l’origine, au sein d’un os long comme le fémur, du matériau de départ, et la façon dont les BMP sont extraits et quantifiés.
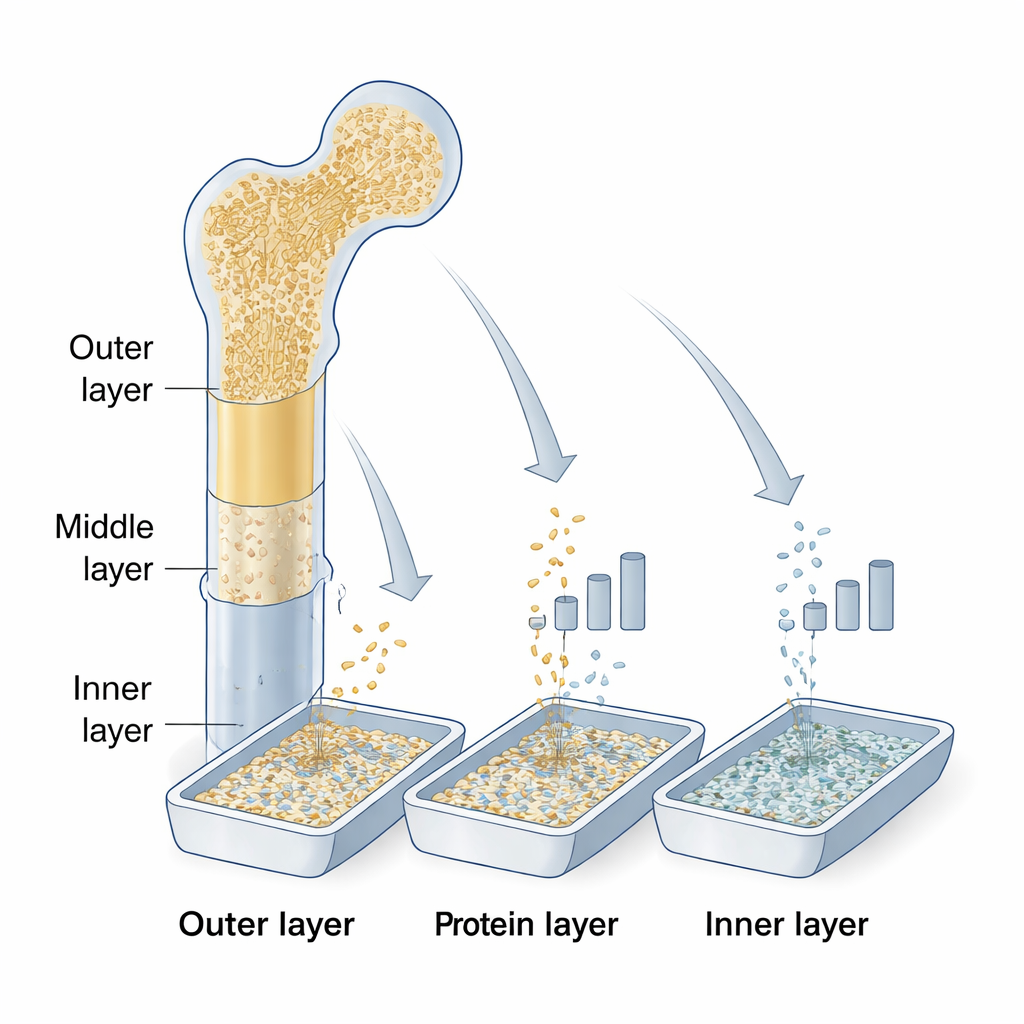
Découper un os en couches
À partir d’un seul fémur humain d’un donneur, l’équipe a découpé la diaphyse dure en trois couches égales : une couche externe près du périoste (la gaine fibreuse de l’os), une couche médiane et une couche interne près de l’endoste et de la moelle. Ils ont broyé chaque couche en petites particules. Certaines particules des couches externe et médiane ont été laissées minéralisées comme os cortical ordinaire, tandis que d’autres — ainsi que toutes les particules de la couche interne — ont été déminéralisées à l’acide pour créer de la DBM. Ce procédé élimine la majeure partie du calcium mais laisse la matrice organique qui contient les BMP et d’autres facteurs de croissance.
Mesurer les signaux ostéogéniques en laboratoire
Pour évaluer la quantité de BMP‑2 et BMP‑7 présente dans chaque échantillon, les scientifiques ont comparé deux méthodes d’extraction courantes en laboratoire. L’une utilisait le chlorhydrate de guanidine (GuHCl), un produit chimique puissant qui extrait les protéines de la matrice osseuse. L’autre utilisait la collagénase, une enzyme qui digère le collagène, la principale protéine structurelle de l’os. Après extraction, ils ont mesuré à la fois les protéines totales et les niveaux spécifiques de BMP à l’aide de dosages protéiques standard et de tests antigène‑anticorps très sensibles (ELISAs), puis ont comparé les résultats entre couches et méthodes.
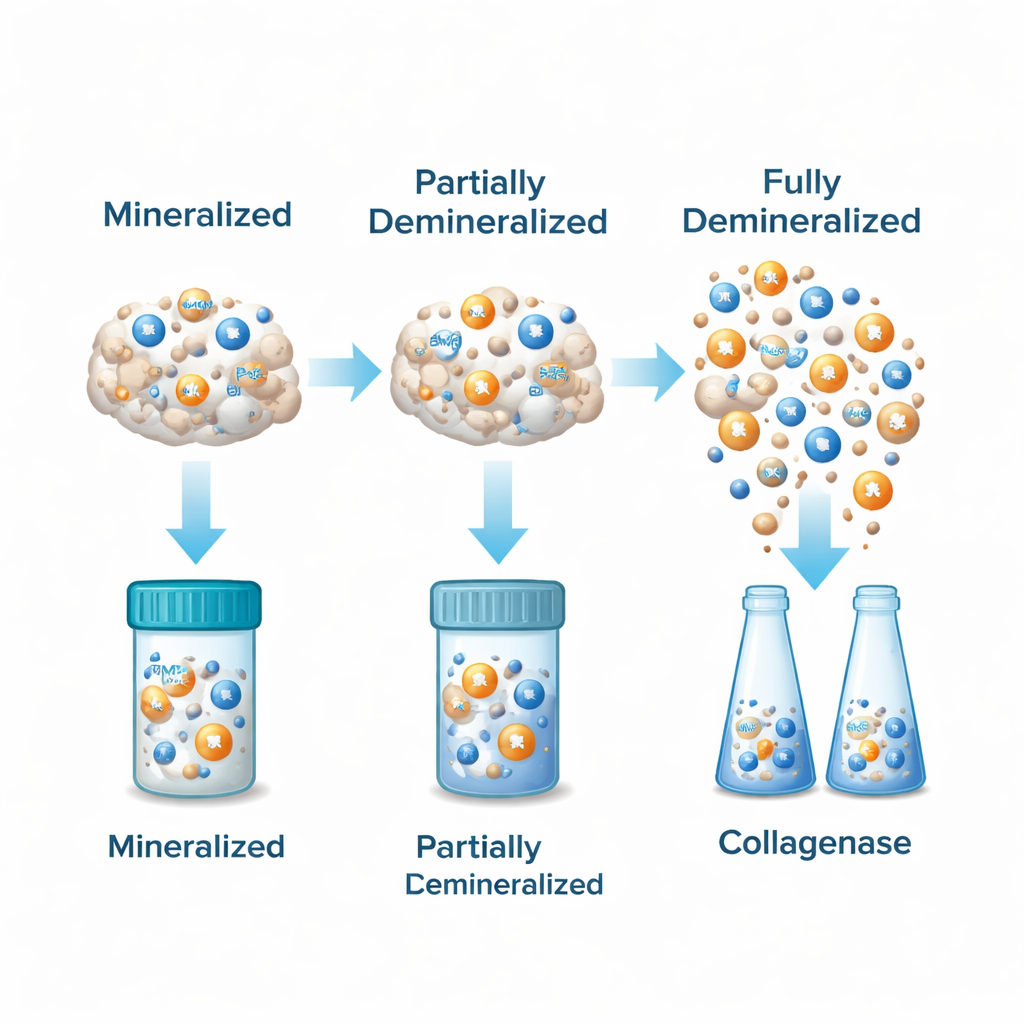
Cartographie inégale des protéines à l’intérieur d’un même os
La déminéralisation a induit une différence frappante : pour une même couche, les échantillons de DBM contenaient beaucoup plus de BMP‑2 et BMP‑7 détectables que les particules osseuses correspondantes minéralisées. Dans le groupe DBM, la couche externe présentait systématiquement les niveaux les plus élevés des deux BMP, la couche médiane en avait un peu moins et la couche interne les quantités les plus faibles. Ce schéma se vérifiait quel que soit le recours à GuHCl ou à la collagénase. Les deux BMP variaient de concert dans une forte relation linéaire — les échantillons riches en BMP‑2 contenaient presque toujours plus de BMP‑7 aussi — montrant que ces signaux clés de croissance tendent à covarier au sein de l’os.
Quand la méthode d’analyse change la réponse
La méthode d’extraction des protéines influençait également les résultats. GuHCl a extrait de façon spectaculaire davantage de BMP‑2 et de BMP‑7 que la collagénase, dans certains cas des différences de l’ordre de dix à cent fois, même si la collagénase donnait parfois plus de protéines totales. Cela signifie que les tests de routine en laboratoire peuvent sous‑estimer ou mal évaluer le potentiel ostéogénique d’un produit DBM s’ils s’appuient sur une méthode d’extraction moins efficace. Puisque les produits cliniques sont fabriqués à partir de mélanges d’os provenant de différentes couches et donneurs, une telle variabilité cachée du contenu en BMP peut se traduire directement par des performances imprévisibles une fois le matériau implanté chez les patients.
Ce que cela signifie pour les patients et les chirurgiens
Pour les non‑spécialistes, la conclusion est claire : tous les substituts de greffe osseuse ne se valent pas, même s’ils proviennent du même type d’os. Les régions externes des os longs contiennent naturellement davantage de protéines qui déclenchent la formation osseuse, et une extraction chimique puissante révèle bien plus de ces signaux que des méthodes enzymatiques plus douces. Ces différences intrinsèques aident à expliquer pourquoi les produits DBM permettent parfois de bien réparer des défauts osseux et parfois échouent. Un meilleur contrôle de l’origine du tissu osseux du donneur et des méthodes de test de son contenu protéique pourrait rendre les futurs matériaux de greffe osseuse plus fiables et efficaces.
Citation: Zhao, Yj., Xue, Y., Sun, S. et al. Various distribution of BMPs in different periosteal layers contributing to inconsistent osteoinductivity of DBM-based products. Sci Rep 16, 5279 (2026). https://doi.org/10.1038/s41598-026-35269-z
Mots-clés: greffe osseuse, matrice osseuse déminéralisée, protéine morphogénétique osseuse, guérison osseuse, chirurgie orthopédique