Clear Sky Science · fr
La reprogrammation métabolique renforce la résistance au stress oxydatif dans les cardiomyocytes en différenciation
Pourquoi la lutte des cellules cardiaques contre l’oxygène compte
Chaque battement de votre cœur dépend de cellules musculaires spécialisées appelées cardiomyocytes. Au cours de la croissance, ces cellules subissent une transformation radicale : elles passent d’un environnement hypoxique et alimenté par le glucose in utero à un milieu riche en oxygène après la naissance. L’oxygène est indispensable, mais il génère aussi des sous-produits nocifs susceptibles d’endommager l’ADN et de tuer les cellules. Cette étude analyse comment les cellules cardiaques en maturation réorganisent leur métabolisme pour tolérer davantage d’oxygène, produire plus d’énergie et se protéger du dommage oxydatif — des informations susceptibles d’éclairer de futurs traitements des maladies cardiaques et des approches de régénération.
D’ouvriers modestes à athlètes de l’énergie
Les cellules cardiaques immatures, appelées cardiomyoblastes, sont de petites cellules en division qui dépendent principalement de la dégradation du glucose pour produire de l’énergie. Lorsqu’elles se différencient en cardiomyocytes matures, elles cessent de se diviser et augmentent de volume, se fusionnant souvent pour former des cellules polynucléées et allongées mieux adaptées à une contraction puissante. À l’aide d’une microscopie à haute résolution, les chercheurs ont observé cette transformation sur dix jours dans un modèle cellulaire en laboratoire. Les marqueurs de prolifération cellulaire ont diminué, tandis que les cellules se sont étirées et réorganisées en structures fibreuses évoquant le tissu cardiaque, confirmant qu’elles avaient adopté un état plus adulte et contractile. 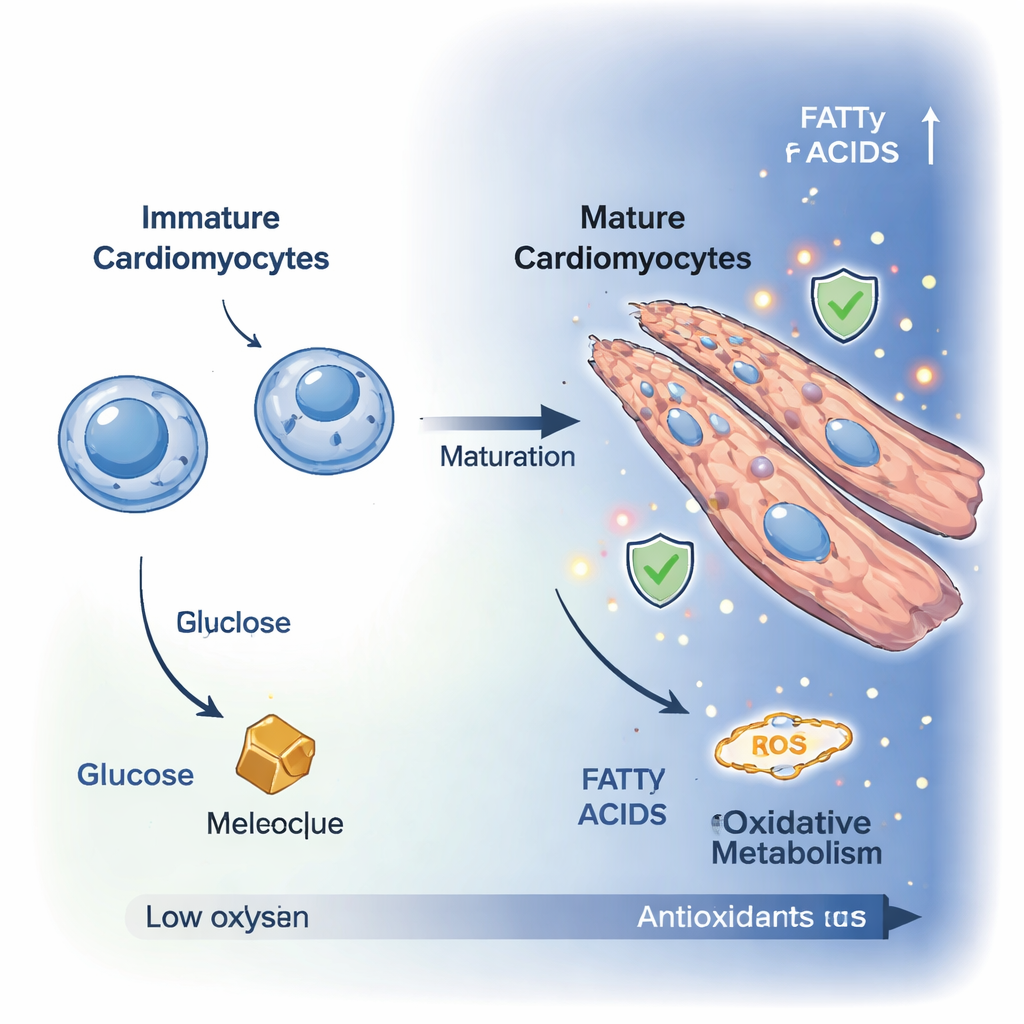
Changement de carburant et nouveaux circuits énergétiques
Pour comprendre ce qui se passe en interne, l’équipe a mesuré des centaines de petites molécules à l’intérieur des cellules et utilisé une imagerie avancée de la fluorescence naturelle cellulaire pour suivre l’utilisation de l’énergie en temps réel. Ces approches ont montré un basculement net d’un état glycolytique, où les cellules brûlent principalement du glucose, vers un état oxydatif dominé par la respiration mitochondriale. Les taux de glucose et de fructose ont diminué, tandis que les intermédiaires du cycle tricarboxylique (TCA) — tels que l’acide citrique, le malate et l’oxoglutarate — ont augmenté. L’analyse des voies métaboliques a révélé une activité renforcée des circuits qui alimentent les mitochondries, y compris la navette malate–aspartate et la dégradation des acides aminés, indiquant que les cardiomyocytes matures élargissent leurs sources énergétiques et canalisent plus efficacement l’énergie vers leurs centrales énergétiques.
Vivre avec plus d’oxygène — et plus de stress
Brûler le carburant plus efficacement dans les mitochondries a un coût : une production accrue d’espèces réactives de l’oxygène (ROS), des molécules chimiquement agressives pouvant endommager les lipides, les protéines et l’ADN. Les chercheurs ont constaté qu’à mesure que les cardiomyocytes mûrissaient, leurs mitochondries devenaient plus grandes et plus allongées, et que les marqueurs du stress oxydatif augmentaient. L’imagerie par fluorescence a révélé davantage de granules de type lipofuscine, un signe d’oxydation des lipides, et une sonde nucléaire a montré des niveaux plus élevés de ROS dans les cellules différenciées. La métabolomique a mis en évidence des modifications du métabolisme du glutathion, un système antioxydant central qui utilise la molécule glutathion — synthétisée à partir d’acides aminés tels que le glutamate et la glycine — pour neutraliser les ROS. Ces observations suggèrent que lorsque les cellules cardiaques intensifient le métabolisme oxydatif, elles ajustent parallèlement leurs voies antioxydantes pour limiter les dégâts. 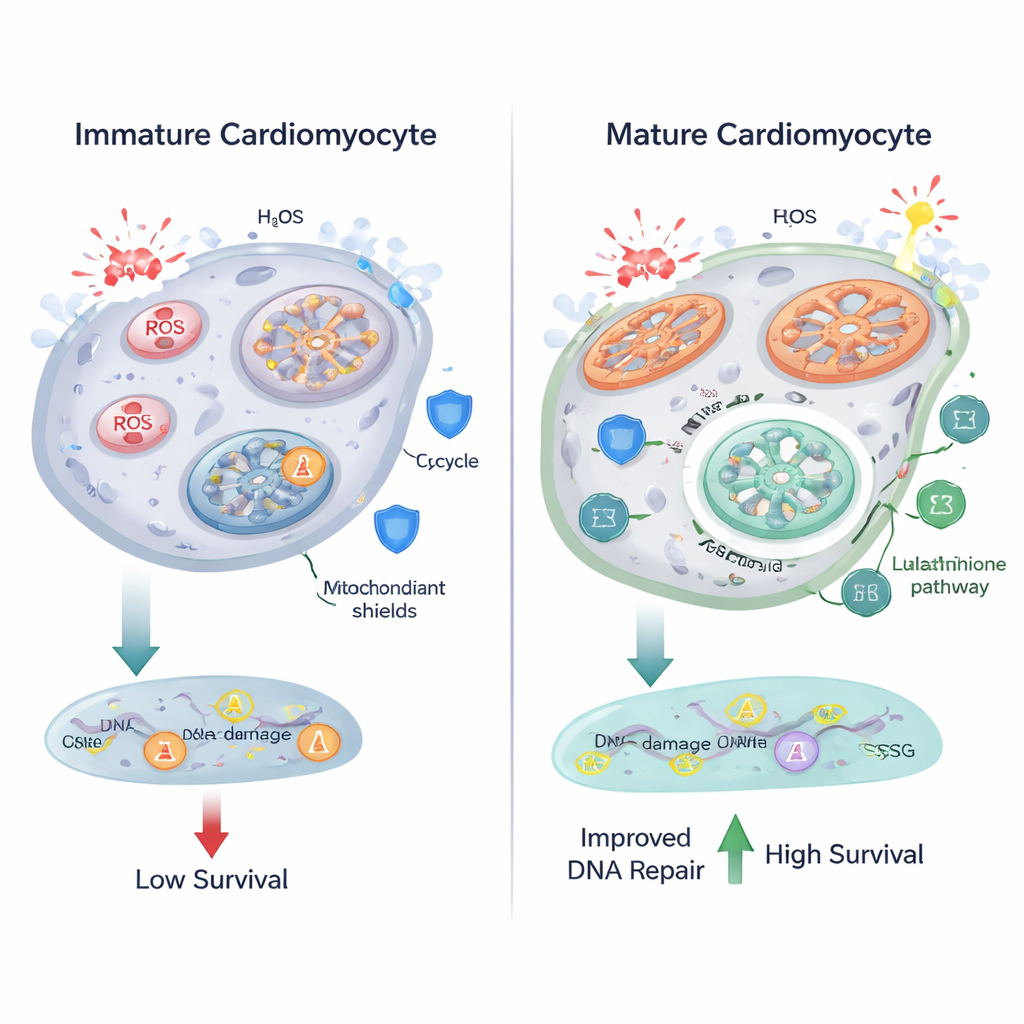
Dommages contenus, défenses renforcées
De manière surprenante, malgré l’augmentation des ROS, les cardiomyocytes différenciés n’ont pas présenté davantage de cassures d’ADN que leurs homologues immatures lorsqu’on a recherché les foyers γ-H2AX, un marqueur sensible des lésions de l’ADN. Lorsqu’ils ont exposé les cellules au peroxyde d’hydrogène, un oxydant puissant, tant les cellules immatures que matures ont accumulé des ROS et des cassures d’ADN — mais les cellules matures s’en sont mieux sorties. Elles ont montré proportionnellement moins de lésions d’ADN par rapport à leurs niveaux plus élevés de ROS, étaient moins enclines à activer des signaux liés à la mort cellulaire tels que PUMA, et présentaient des taux de survie nettement supérieurs. Ces résultats indiquent que les cardiomyocytes en maturation n’ajustent pas seulement leur métabolisme, mais renforcent aussi leurs mécanismes de réparation de l’ADN et de survie, leur permettant de résister à des conditions oxydatives plus sévères.
Ce que cela implique pour la protection du cœur
En termes simples, cette étude montre que, en mûrissant, les cellules cardiaques apprennent à fonctionner à plus haute intensité sans s’épuiser. Elles passent d’un mode de vie pauvre en oxygène et riche en sucre à un mode centré sur l’oxygène et piloté par les mitochondries, et construisent en parallèle de meilleurs boucliers et systèmes de réparation pour faire face au stress oxydatif. Comprendre cet équilibre finement réglé entre production d’énergie et auto-protection pourrait aider les chercheurs à concevoir des stratégies pour rendre les tissus cardiaques adultes endommagés plus résilients, ou pour orienter des cellules souches vers des cardiomyocytes plus sûrs et durables destinés à des thérapies régénératives.
Citation: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Mots-clés: différenciation des cardiomyocytes, stress oxydatif, mitochondries, métabolisme cellulaire, maladies cardiaques