Clear Sky Science · fr
La déglycosylation induit une nouvelle conformation distale dans le récepteur de la mannose CD206
Pourquoi les revêtements sucrés des capteurs immunitaires comptent
Nos cellules immunitaires s’appuient sur des « antennes » moléculaires pour détecter des menaces comme les micro‑organismes ou les cellules cancéreuses. L’une de ces antennes, appelée récepteur de la mannose CD206, aide les cellules immunitaires à saisir des molécules décorées de sucres et peut même les guider vers des tumeurs. Comme de nombreuses protéines, CD206 est elle‑même couverte de courtes chaînes sucrées. Cette étude pose une question apparemment simple mais aux grandes implications : que se passe‑t‑il pour la forme et la fonction de CD206 lorsque ces sucres sont retirés ?
Un bras flexible qui lit les signaux sucrés
CD206 se trouve à la surface de certains globules immunitaires, en particulier des macrophages qui patrouillent les tissus et les tumeurs. Il possède une longue structure articulée qui s’étend depuis la membrane cellulaire et se termine par plusieurs segments « lectines » reconnaissant les sucres des molécules en passage. CD206 peut aussi être libéré dans la circulation sanguine, où ses niveaux sont corrélés aux maladies inflammatoires et fibreuses, ce qui en fait un marqueur potentiel de pathologie. La protéine est fortement décorée de chaînes glycosylées N‑liées ; des travaux antérieurs ont montré que ces glycannes peuvent influencer la capacité des différents segments du récepteur à reconnaître les sucres. Beaucoup de ces sites glycosylés sont éloignés des poches de liaison principales, suggérant qu’ils pourraient agir davantage comme des interrupteurs distants que comme de simples bloqueurs.
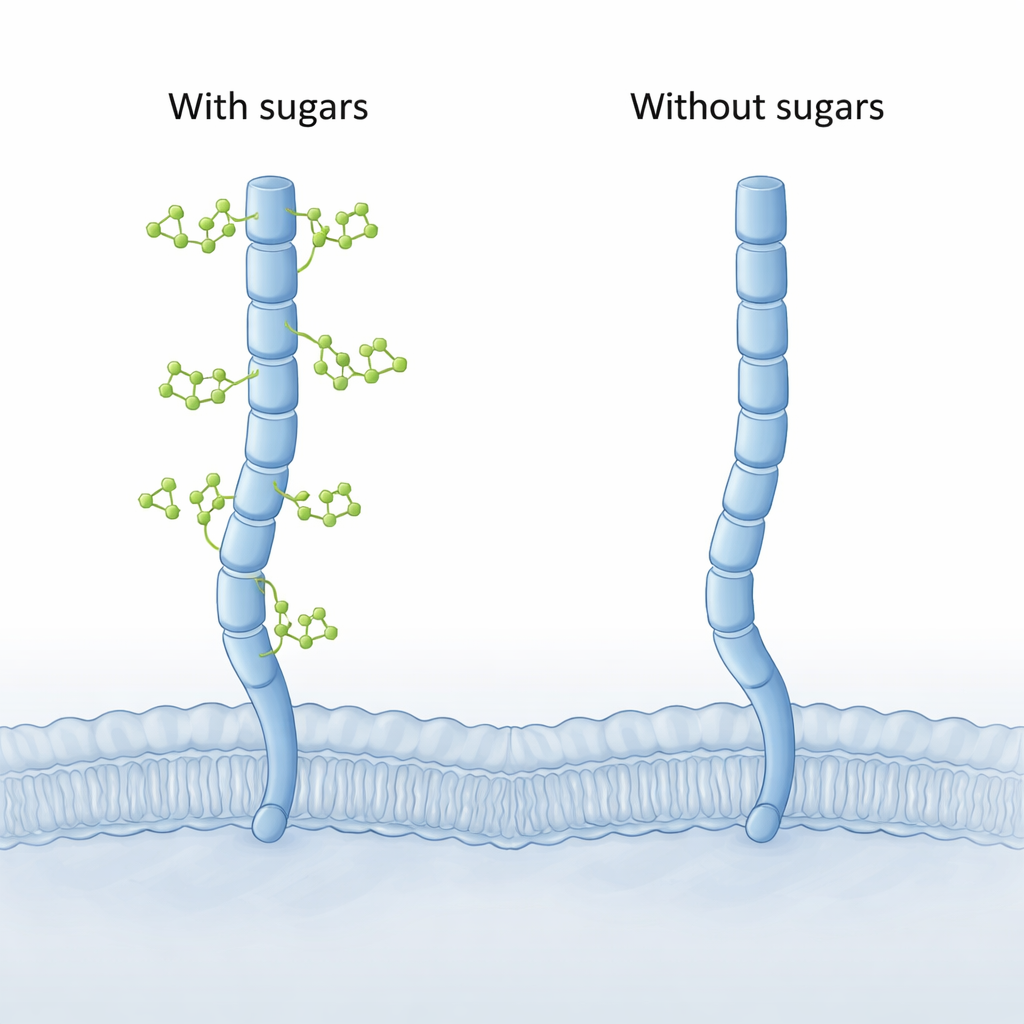
Les modèles informatiques révèlent une flexion cachée
Comme la structure 3D complète de CD206 n’a pas encore été obtenue expérimentalement, les auteurs ont eu recours à des outils computationnels modernes. Ils ont d’abord utilisé AlphaFold pour construire des modèles de la protéine en pleine longueur, puis réalisé de longues et détaillées simulations de dynamique moléculaire de CD206 avec et sans ses sucres attachés. Les deux versions se comportaient comme un bras moléculaire étendu, mais la forme « déglycosylée » a montré un mouvement nouveau et frappant à son extrémité. Les deux derniers segments lectines (dénommés CTLD7 et CTLD8) pouvaient se balancer vers l’intérieur pour former une pointe concave et repliée, une configuration jamais observée dans la version glycosylée, qui restait plutôt incurvée vers l’extérieur, ou convexe.
Comment un petit changement reconfigure le mouvement
Pour comprendre cette différence, l’équipe a analysé les mouvements dominants observés dans leurs simulations. Ils ont constaté que le mouvement principal distinguant les deux formes était cette flexion de la pointe distale, qui n’apparaissait que lorsque les sucres étaient absents. La suppression des glycannes rendait globalement le récepteur plus flexible, en particulier dans les segments lectines distaux et, dans une moindre mesure, près de l’extrémité N‑terminale. Des cartes de corrélation montrant comment différentes parties de la protéine bougent ensemble ont révélé que, sans sucres, les deux derniers segments lectines se déplacent de façon plus concertée et sont plus étroitement couplés à d’autres régions. Essentiellement, les sucres ne se contentent pas de rester à la surface ; ils contribuent à régler la façon dont tout le bras fléchit et communique le long de sa longueur.
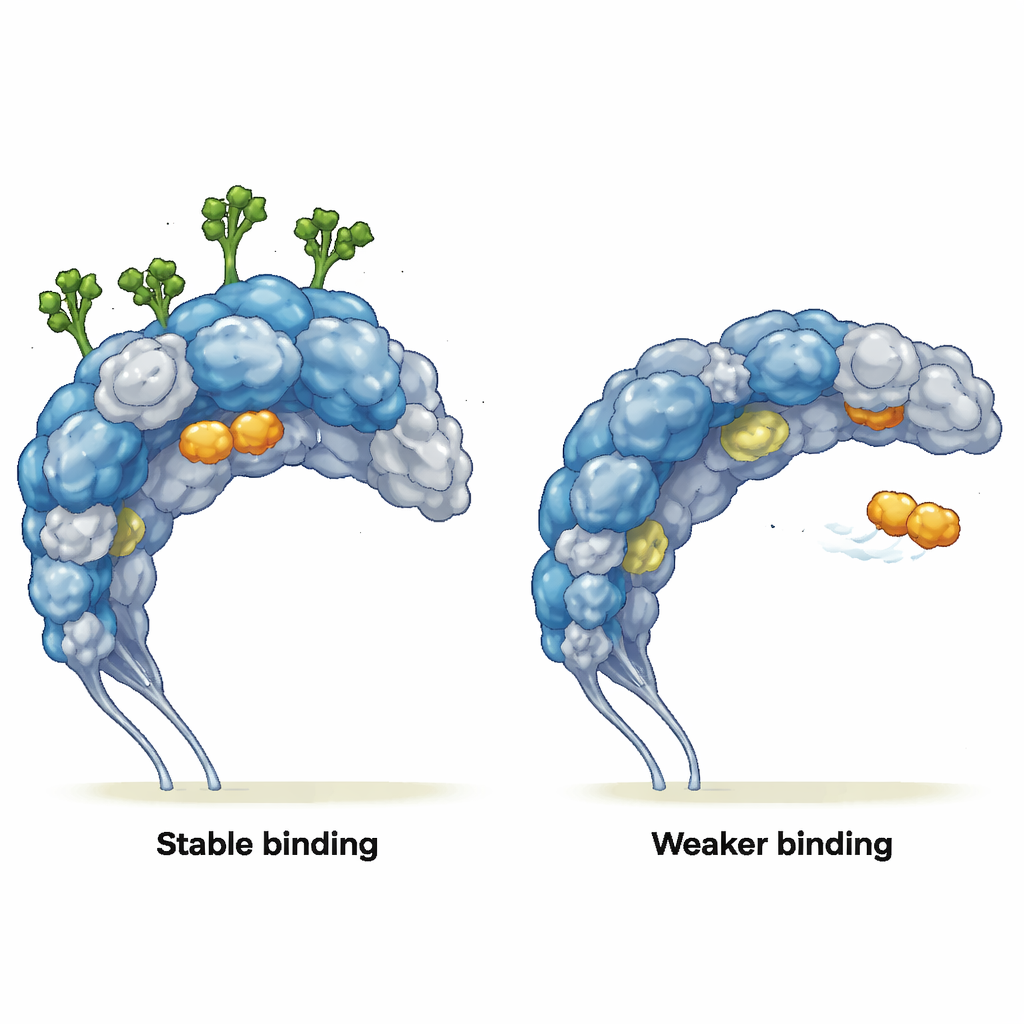
Modifier la façon dont les partenaires se lient
Les auteurs se sont ensuite demandé comment ce mouvement altéré affecte les partenaires de liaison réels. Ils ont simulé des interactions avec deux ligands : un sucre simple de type mannose (MMA), qui s’insère dans une poche bien définie, et un peptide homing tumoral appelé mUNO, qui cible les macrophages associés aux tumeurs exprimant CD206. Lorsque les sucres étaient présents, MMA restait bien calé dans sa poche de liaison pendant toute la simulation, conservant des contacts clés, même si la structure protéique voisine changeait à peine. Sans les glycannes, MMA a pu s’échapper de la poche, glissant à la surface de la protéine et ne formant que des contacts brefs et superficiels. Pour mUNO, le récepteur glycosylé présentait plusieurs poses de liaison stables avec des contacts fréquents et de longue durée. Dans le récepteur déglycosylé, la liaison de mUNO était plus faible et plus dispersée, et le peptide a aussi commencé à explorer des régions normalement masquées par les chaînes sucrées, révélant de nouveaux sites d’interaction auparavant cachés.
Ce que cela implique pour la maladie et la thérapie
Au total, ces résultats montrent que les sucres attachés à CD206 agissent comme des régulateurs à distance de sa conformation et de son adhérence. En limitant certaines flexions et en organisant la manière dont ses segments bougent ensemble, la glycosylation aide le récepteur à retenir certains ligands plus fermement et à orienter d’autres vers des points d’accrochage préférentiels, tout en masquant des portions de sa surface. Dans des maladies comme le cancer, où les profils glycosylationnels des protéines sont souvent altérés, CD206 peut adopter des formes et des comportements de liaison différents, modifiant la façon dont les cellules immunitaires perçoivent leur environnement. Comprendre cet « interrupteur conformationnel » dépendant des sucres éclaire non seulement le fonctionnement de CD206, mais suggère aussi de nouvelles voies pour concevoir des médicaments ou des agents d’imagerie exploitant son paysage changeant dans les tumeurs et autres conditions pathologiques.
Citation: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Mots-clés: récepteur de la mannose, glycosylation des protéines, reconnaissance immunitaire, macrophages associés aux tumeurs, dynamique moléculaire