Clear Sky Science · fr
La perte de Snhg5 perturbe la régulation du cycle cellulaire sans modifier la cystogenèse dans un modèle murin de polykystose rénale
Pourquoi un gène rénal au nom étrange compte
La maladie polykystique des reins (MPR) est une affection héréditaire fréquente dans laquelle d’innombrables sacs remplis de liquide envahissent progressivement les reins, conduisant souvent à l’insuffisance rénale. Les scientifiques savent que des anomalies dans deux gènes, PKD1 et PKD2, sont à l’origine de la maladie, mais de nombreux autres acteurs génétiques peuvent influencer la vitesse de progression. Cette étude se concentre sur un type inhabituel de gène appelé ARN long non codant, nommé Snhg5, et pose une question simple mais importante : cette molécule façonne-t-elle de manière significative le déroulement de la MPR, ou n’est-elle qu’un témoin ?
Un examen approfondi d’un messager génétique obscur
À la différence des gènes typiques qui fournissent des plans pour des protéines, les ARN longs non codants agissent davantage comme des organiseurs moléculaires ou des interrupteurs à l’intérieur des cellules. Des travaux antérieurs ont montré que Snhg5 est fortement augmenté dans des modèles murins de MPR et a été associé à plusieurs cancers et lésions rénales, laissant penser qu’il pourrait favoriser une croissance nuisible. Les chercheurs ont d’abord cartographié où et quand Snhg5 est actif chez la souris normale. Ils ont constaté qu’il est exprimé dans de nombreux organes, avec des niveaux particulièrement élevés dans l’intestin, et que son activité dans le rein chute fortement après la naissance, lorsque l’organe passe d’une phase de croissance rapide à un état plus stable et mature. Au sein des cellules rénales, presque toutes les molécules de Snhg5 se trouvent dans le noyau, le centre de commande qui contient l’ADN, ce qui suggère que Snhg5 aide à réguler l’activité des gènes plutôt qu’à produire directement des protéines.
Les schémas observés dans les reins malades ne racontent pas toute l’histoire
L’équipe a ensuite comparé les niveaux de Snhg5 dans une gamme de modèles murins de MPR. Dans les modèles à évolution rapide, où les kystes se forment rapidement, Snhg5 était augmenté de deux à trois fois dans les reins malades, et l’imagerie au niveau de la cellule unique montrait de forts signaux nucléaires dans les cellules bordant les kystes et les tissus voisins. De façon surprenante, lorsqu’ils ont examiné un modèle murin plus lent et plus bénin, qui reproduit mieux le long cours de la MPR humaine, Snhg5 n’était pas augmenté. Plus frappant encore, dans des tissus rénaux provenant de personnes atteintes d’une MPR autosomique dominante avancée, l’équivalent humain du gène, appelé SNHG5, était en réalité réduit de plus de 90 %. Ensemble, ces résultats suggèrent que les modifications de cet ARN accompagnent la formation des kystes, mais que la direction et le moment de cette variation diffèrent selon les espèces et les stades de la maladie, ce qui remet en question l’idée que Snhg5 soit à lui seul un moteur évident de la croissance kystique.
Que se passe-t-il lorsque le gène est supprimé
Pour aller au-delà de la corrélation, les chercheurs ont utilisé l’édition génomique CRISPR pour supprimer complètement le gène Snhg5 chez la souris, créant une lignée globale « knockout ». Contrairement aux craintes selon lesquelles la suppression d’une molécule aussi fortement altérée pourrait être nocive, les souris dépourvues de Snhg5 sont nées selon des proportions normales, ont vécu une durée de vie normale et avaient des reins qui ressemblaient et fonctionnaient comme ceux de leurs congénères sains. L’examen microscopique a révélé une structure rénale normale sans cicatrisation ni inflammation, et les analyses sanguines n’ont montré aucun signe d’altération de la filtration rénale. Au niveau moléculaire, toutefois, des changements plus subtils sont apparus : les reins de souris et les cellules tubulaires rénales cultivées dépourvus de Snhg5 présentaient des modifications cohérentes de l’activité de gènes liés à la division cellulaire et à la réplication de l’ADN. En culture cellulaire, davantage de cellules s’arrêtaient à des stades tardifs du cycle cellulaire et dans un état endommagé dit sub-G1. Une protéine en particulier, ARPC5, composant d’un complexe qui aide les cellules à se diviser en réarrangeant leur échafaudage interne, était réduite en l’absence de Snhg5, suggérant une chaîne possible de cause à effet.
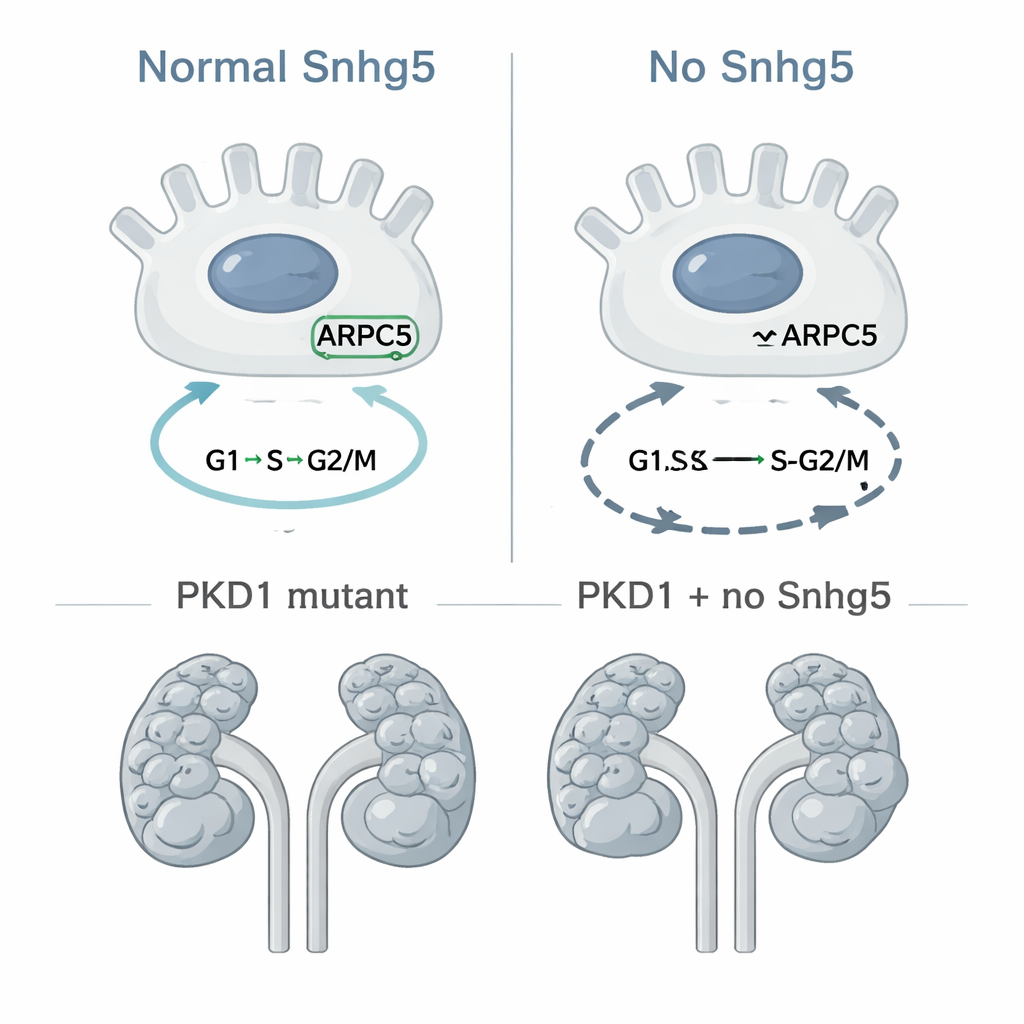
Tester directement son rôle dans la croissance des kystes
Comme la division cellulaire incontrôlée est une caractéristique centrale de la MPR, l’équipe a ensuite demandé si la suppression de Snhg5 ralentirait la formation de kystes dans un modèle murin bien établi où le gène PKD1 est inactivé spécifiquement dans les cellules du canal collecteur, source de nombreux kystes. Ils ont obtenu des animaux où certains portaient uniquement la mutation PKD1, tandis que d’autres étaient dépourvus à la fois de PKD1 et de Snhg5. À l’examen des animaux à 10 jours, les deux groupes présentaient des reins sévèrement kystiques, et des mesures précises de la taille des reins, de la surface kystique et du nombre de kystes n’ont révélé aucune protection significative liée à la suppression de Snhg5. Au mieux, les souris doublement mutées avaient tendance à présenter une charge kystique légèrement plus importante, bien que la différence fût faible et non significative sur le plan statistique. En d’autres termes, même si Snhg5 influence les gènes du cycle cellulaire dans les cellules rénales, son absence ne modifie pas de façon notable la vitesse d’apparition ou d’agrandissement des kystes dans ce modèle particulier de MPR.
Ce que cela signifie pour les traitements futurs
Pour les patients et les développeurs de médicaments, l’enseignement principal est que Snhg5, malgré son statut de signal génétique fortement modifié dans la MPR murine, n’est pas un pivot de la formation des kystes — du moins pas dans la phase précoce et à croissance rapide de la maladie d’origine tubulaire collectrice. Le gène semble toutefois moduler finement la progression des cellules rénales dans le cycle de division, probablement via son impact sur des facteurs comme ARPC5, mais cette influence est suffisamment subtile pour que sa perte complète laisse le développement rénal et la progression précoce de la MPR essentiellement inchangés. Ces résultats soulignent une leçon plus générale : toute modification moléculaire spectaculaire dans un tissu malade n’est pas nécessairement une cible thérapeutique prometteuse. Démêler la cause de la conséquence exigera de tester des ARN longs non codants comme Snhg5 à travers plusieurs modèles de la maladie et à différents instants avant de les envisager avec confiance comme candidats médicamenteux.
Citation: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Mots-clés: maladie polykystique des reins, ARN long non codant, Snhg5, cycle cellulaire, kystes rénaux