Clear Sky Science · fr
Classification par intelligence artificielle des néoplasies rectales par analyse endoscopique de la perfusion par fluorescence
Pourquoi c’est important pour les patients et les médecins
Pour les personnes présentant de gros polypes rectaux, l’une des questions majeures est de savoir si la lésion est bénigne ou si elle est déjà en train de devenir un cancer. Aujourd’hui, les médecins ne peuvent souvent en être sûrs qu’après avoir retiré la lésion en entier, ce qui peut entraîner des interventions plus lourdes que nécessaire ou des retards de prise en charge. Cette étude examine si une technique d’imagerie intelligente, combinée à l’intelligence artificielle, peut repérer un cancer caché pendant l’intervention elle‑même en observant la façon dont le sang circule dans le tissu.
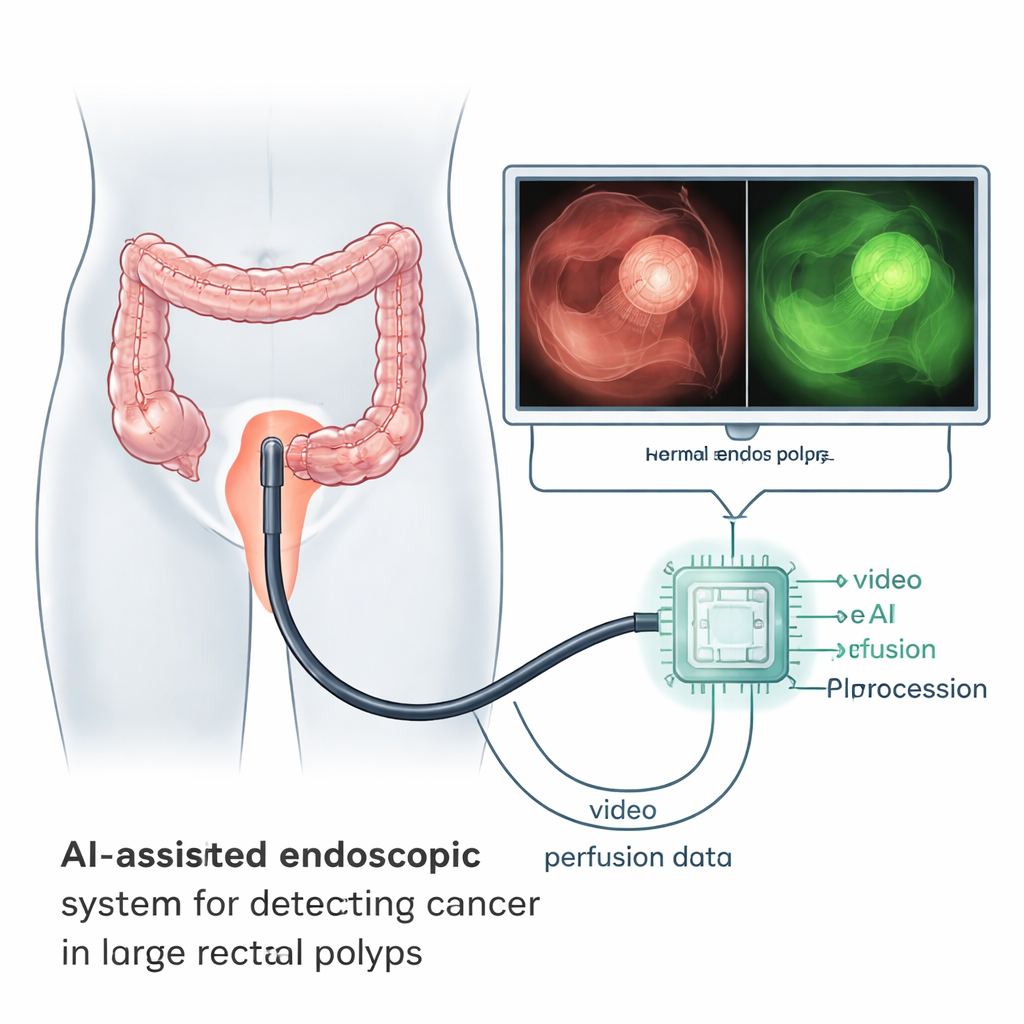
Écouter comment une tumeur est alimentée
Les cancers ne se développent pas comme les tissus normaux. Ils stimulent la formation de nouveaux vaisseaux sanguins anormaux qui fuient et se ramifient de manière désorganisée. Ces modifications créent des motifs distinctifs dans la façon dont le sang, et les colorants injectés, pénètrent et se retirent d’une tumeur. Les chercheurs ont utilisé un colorant appelé indocyanine verte, qui brille sous lumière proche infrarouge, et ont enregistré de courtes vidéos pendant des interventions endoscopiques chez des patients porteurs de gros polypes rectaux et de cancers rectaux précoces. En suivant la luminosité de la fluorescence sur plusieurs minutes, ils ont pu capturer une sorte de « signature de perfusion » pour les zones suspectes et saines chez un même patient.
Transformer les motifs de fluorescence en données
Chaque vidéo a été analysée par un logiciel personnalisé qui divisait la région visible de la paroi intestinale en une grille de petits carrés et les suivait dans le temps, même lorsque la caméra et les tissus bougeaient. Pour chaque carré, le programme mesurait l’intensité maximale de la fluorescence, la rapidité d’apparition du pic et la vitesse d’atténuation. Il nettoyait ensuite et normalisait ces courbes pour les rendre comparables directement. À partir de ces traces temporelles, l’équipe a extrait des caractéristiques numériques simples comme le signal maximal et la baisse du signal à des moments précis après le pic. Ils ont aussi évalué l’hétérogénéité de ces valeurs dans la région anormale, à l’aide d’une statistique capturant la variation au sein de la tumeur par rapport aux tissus sains voisins.
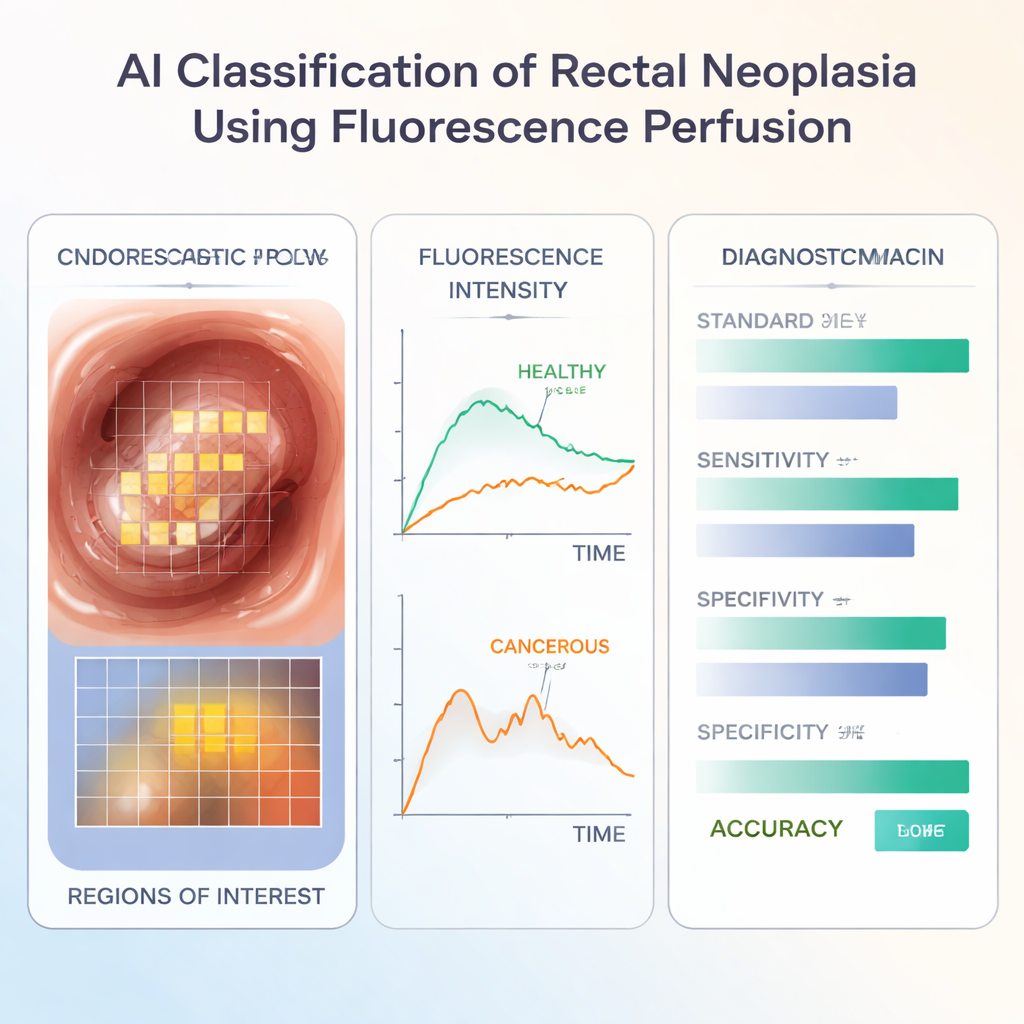
Entraîner l’intelligence artificielle
Le groupe a étudié 190 vidéos provenant de 182 patients traités dans six hôpitaux de quatre pays ; environ trois patients sur cinq ont finalement eu un cancer confirmé au microscope. Ils ont entraîné un modèle d’apprentissage automatique (un classificateur XGBoost) pour apprendre la différence entre lésions bénignes et cancéreuses en se basant uniquement sur les caractéristiques d’écoulement du colorant, sans utiliser les images couleur normales. Lorsqu’on l’a appliqué à de nouveaux cas, le modèle a correctement identifié le cancer chez une large majorité de patients, avec des performances comparables ou légèrement supérieures à celles de nombreux outils standard utilisés en pratique, comme les biopsies endoscopiques, les IRM préopératoires et l’impression visuelle de chirurgiens experts.
Ajouter des indices cliniques du monde réel
Dans la pratique, les médecins s’appuient rarement sur un seul test. Les chercheurs ont donc combiné la sortie de l’IA avec des informations déjà disponibles : les comptes rendus d’IRM et le jugement du chirurgien opérateur. Lorsqu’elles ont été intégrées dans le même pipeline informatique, les capacités de détection du cancer se sont améliorées, en particulier pour écarter correctement la maladie dans les lésions bénignes. Dans le meilleur scénario, le système combiné a détecté environ 86 % des cancers tout en évitant des faux positifs dans approximativement 71 % des cas non cancéreux. L’approche a également bien fonctionné dans des sous‑groupes de patients plus typiques de maladies précoces et localement résécables.
Ce que cela pourrait signifier pour les soins futurs
L’étude montre que les cancers présents dans de gros polypes rectaux laissent une signature détectable dans la façon dont le sang et le colorant les traversent, et que cette signature peut être repérée automatiquement par une IA. Bien que le travail ait jusqu’ici été réalisé sur des vidéos enregistrées et doive encore être validé dans des essais cliniques en temps réel, il ouvre la voie à un avenir où le coloscopiste pourrait être averti, pendant l’intervention, qu’un polype apparemment bénin cache probablement un cancer invasif. Cette information pourrait guider le choix des sites de biopsie, décider de l’exérèse locale de la lésion ou d’un renvoi pour une chirurgie plus étendue, réduisant à la fois les cancers manqués et les opérations majeures inutiles.
Citation: Boland, P.A., MacAonghusa, P., Singaravelu, A. et al. Artificial intelligence classification of rectal neoplasia by endoscopic fluorescence perfusion analysis. Sci Rep 16, 4761 (2026). https://doi.org/10.1038/s41598-026-35233-x
Mots-clés: cancer du rectum, imagerie endoscopique, perfusion par fluorescence, intelligence artificielle, apprentissage automatique